Clear Sky Science · pl
Hydrożelowy rezerwuar komórek samoorganizujący się in situ do sterowania wieloetapową radioimmunoterapią
Przekształcanie promieniowania w inteligentniejszą broń przeciwnowotworową
Terapia promieniowaniem jest jednym z najczęściej stosowanych zabiegów w leczeniu raka, ale guzy często przetrwają, ukrywając się przed układem odpornościowym i rozwijając w warunkach niskiego natlenienia (hipoksji), co osłabia działanie promieniowania. W tym badaniu opisano wstrzykiwalny „inteligentny" hydrożel, który tworzy się bezpośrednio w guzie i działa jak miniaturowa fabryka leków oraz generator tlenu. Dostarczając guzowi zarówno promieniowanie, jak i precyzyjnie zsynchronizowane sygnały pobudzające odporność, system ma na celu przekształcenie trudno leczącego się nowotworu w cel, który własne mechanizmy obronne organizmu będą mogły rozpoznać i zniszczyć.
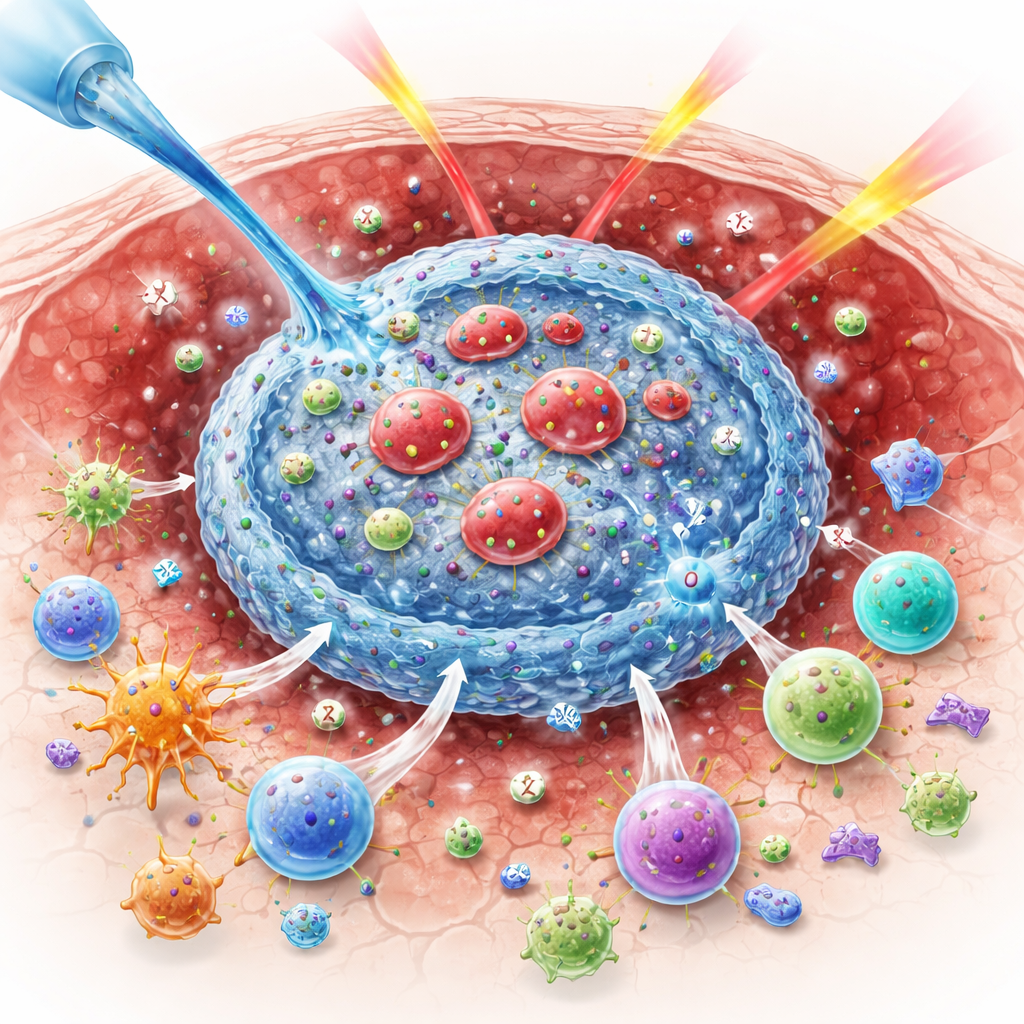
Dlaczego tlen ma znaczenie w walce z guzami
Promieniowanie zabija komórki nowotworowe częściowo poprzez wytwarzanie wysoko reaktywnych cząsteczek tlenu, które uszkadzają DNA. Gdy guzy są pozbawione tlenu, ta chemia działa słabiej, więc więcej komórek nowotworowych przeżywa. Jednocześnie promieniowanie wysyła do układu odpornościowego sprzeczne sygnały. Może odsłaniać białka nowotworu, które oznaczają go jako zagrożenie, ale także wzmacniać „hamulce" w komórkach odpornościowych, takie jak białko kontrolne CTLA-4, oraz sprzyjać komórkom T regulatorowym tłumiącym atak. Te przeciwstawne efekty częściowo wyjaśniają, dlaczego łączenie promieniowania z lekami immunologicznymi nie zawsze przyniosło w pacjentach tak dobre wyniki, jak w badaniach na myszach.
Żywy żel zbudowany wewnątrz guza
Naukowcy zaprojektowali materiał, który sam składa się tylko w kwaśnym środowisku guza. Składa się on z trzech kluczowych składników: naturalnego polimeru cukrowego zwanego alginianem, proszku nieorganicznego — nadtlenku baru, oraz krwinek czerwonych delikatnie zmodyfikowanych tak, by niosły dwa leki immunologiczne. Po wstrzyknięciu mieszanki do guza kwaśne warunki powodują rozkład nadtlenku baru, uwalniając jony baru i nadtlenek wodoru. Jony baru natychmiast sieciują alginian, tworząc miękki hydrożel, który unieruchamia zmodyfikowane krwinki czerwone i zapobiega spłukiwaniu leków. Jednocześnie enzymy naturalnie obecne w krwinkach czerwonych przekształcają nadtlenek wodoru w tlen, pomagając złagodzić hipoksję guza i przygotować go do skuteczniejszego działania promieniowania.
Skontrolowane w czasie uwalnianie podwójnych sygnałów immunologicznych
Prawdziwa siła systemu polega na tym, jak rozłożone jest w czasie uwalnianie dwóch czynników immunologicznych: przeciwciała blokującego CTLA-4 oraz cytokininy zwanej interleukiną-12 (IL-12). Przeciwciało jest załadowane wewnątrz krwinek czerwonych, natomiast IL-12 jest zakotwiczona na ich powierzchni. W miarę jak generowany jest tlen, w błonie krwinek czerwonych powstają pory, co pozwala przeciwciału blokującemu CTLA-4 szybko się uwolnić. Ten wczesny wyrzut znosi supresję immunologiczną, zachęca komórki dendrytyczne do przenoszenia antygenów nowotworowych do pobliskich węzłów chłonnych i pomaga aktywować komórki T specyficzne dla guza. IL-12 natomiast sączy się powoli w miarę stopniowego luzowania struktury hydrożelu. Ten późniejszy sygnał pobudza komórki T i komórki NK do produkcji interferonu gamma, napędza dalszy napływ zabójczych komórek odpornościowych do guza i wzmacnia dodatnie sprzężenie zwrotne między strażnikami a efektorami układu odpornościowego.
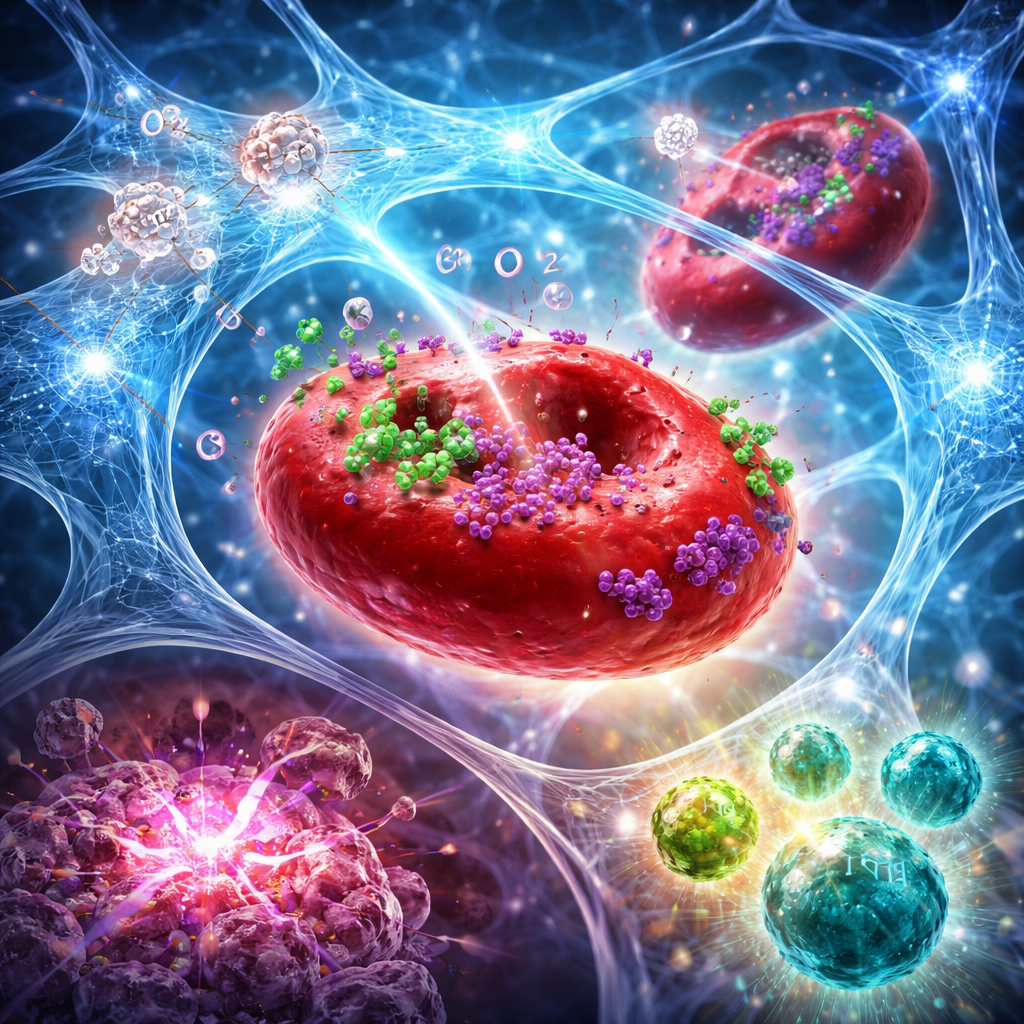
Od miejscowego wstrzyknięcia do ogólnoustrojowego ataku immunologicznego
W modelach mysich agresywnych raków piersi i trzustki połączenie tego hydrożelu ze skupionym promieniowaniem zrobiło więcej niż tylko zmniejszyć leczony guz. Metoda ta podwyższyła poziom tlenu w guzach na kilka dni, wzmocniła uszkodzenia DNA wywołane promieniowaniem i wywołała silniejszą formę śmierci komórkowej, która naturalnie oznacza guzy do rozpoznania przez układ odpornościowy. Cytometria przepływowa i barwienia tkanek wykazały wyraźne przesunięcie w mikrośrodowisku guza: więcej cytotoksycznych komórek CD8 i komórek NK, mniej komórek T regulatorowych oraz wyższy stosunek komórek „efektorowych" do „tłumiących". Zwiększyła się też liczba wyspecjalizowanych komórek dendrytycznych w węzłach chłonnych, co wskazuje na lepsze prezentowanie antygenów. Wiele myszy doświadczyło całkowitej regresji guza, a niektóre były chronione przed ponownym wzrostem guza po ponownym wprowadzeniu komórek nowotworowych kilka tygodni później, co sugeruje powstanie trwałej pamięci immunologicznej.
Bezpieczeństwo, praktyczność i kierunki na przyszłość
Ponieważ żel tworzy się lokalnie i trzyma swoje ładunki, tylko niewielkie ilości IL-12 i przeciw-CTLA-4 przedostają się do krwiobiegu, zmniejszając ryzyko poważnych działań niepożądanych, takich jak burze cytokinowe czy uszkodzenia narządów, które w przeszłości ograniczały zastosowanie tych środków. Składniki budulcowe — alginian, krwinki czerwone i nadtlenek baru — są stosunkowo tanie i możliwe do wdrożenia na skalę, co daje nadzieję, że tę strategię będzie można dostosować do różnych nowotworów. Wciąż pozostają wyzwania związane z wytwarzaniem, kontrolą jakości i dostarczaniem żelu do głęboko położonych lub szeroko rozproszonych guzów, jednak praca ta pokazuje obiecującą metodę synchronizowania promieniowania z precyzyjnie zaplanowaną aktywacją immunologiczną, przekształcając fizyczne leczenie nowotworu w potężny impuls dla ogólnoustrojowej odpowiedzi przeciwnowotworowej.
Co to może oznaczać dla pacjentów
Mówiąc prosto, badanie to sugeruje, że zamiast podawać promieniowanie i leki immunologiczne oddzielnie i liczyć na ich współdziałanie, można zapakować je w inteligentny materiał, który osadza się w guzie, wytwarza własny tlen i uwalnia sygnały immunologiczne w starannie wyreżyserowanym porządku. U zwierząt podejście to nie tylko zwiększyło śmiertelność promieniowania wobec komórek nowotworowych, ale także wytrenowało układ odpornościowy do rozpoznawania i zapamiętania guza, co pomaga zapobiegać jego nawrotom. Jeśli podobne wyniki uda się osiągnąć u ludzi, takie hydrożele mogłyby pewnego dnia przekształcić trudno leczące się guzy w cele, które własne mechanizmy obronne organizmu będą w stanie niezawodnie odnaleźć i zniszczyć.
Cytowanie: Chen, Y., Chen, Q., Ma, Y. et al. In situ self-assembled cell reservoir hydrogel for maneuvering multistage radioimmunotherapy. Nat Commun 17, 1784 (2026). https://doi.org/10.1038/s41467-026-68490-5
Słowa kluczowe: radioimmunoterapia, hydrożel, immunoterapia przeciwnowotworowa, mikrośrodowisko guza, radioterapia