Clear Sky Science · pl
Ciągle regulowana wielostabilność w sieciach replikacji DNA
Od prostych przełączników do wielu możliwych stanów
Systemy biologiczne, od dzielących się komórek po rozwijające się zarodki, rzadko działają jak proste włączniki światła, będące jedynie w pozycji włączonej lub wyłączonej. Częściej utrzymują liczne trwałe stany, jak ściemniacz, który może zatrzymać się w niezliczonych pozycjach. W artykule opisano sieć chemiczną opartą na DNA, która zachowuje się bardziej jak taki ściemniacz: potrafi stabilnie utrzymywać nie tylko kilka rozróżnialnych stanów, lecz w zasadzie dowolny skład wzdłuż ciągłego spektrum. Ta zdolność może stać się solidną podstawą przyszłych inteligentnych materiałów, molekularnych pamięci i komputerów biochemicznych przetwarzających informacje w sposób analogowy, a nie tylko cyfrowy.
Dlaczego wielostabilność ma znaczenie
Wiele decyzji komórkowych — czy komórka macierzysta dojrzeje, czy komórka ulegnie samozniszczeniu, czy sieć genowa zapamięta poprzedni sygnał — zależy od „wielostabilności”, czyli możliwości pozostawania w więcej niż jednym stabilnym wzorze aktywności w tych samych warunkach. Tradycyjne syntetyczne wersje takich systemów budowano z obwodów genowych, enzymów lub nici DNA, które wzajemnie się włączają i wyłączają. Te projekty zwykle dają kilka dyskretnych wyników, jak klasyczne przełączniki bistabilne z dwoma długotrwałymi stanami. Skalowanie tej idei jest trudne: system o N stanach może wymagać rzędu N×(N−1) starannie dostrojonych powiązań hamujących, a i tak system przeskakuje jedynie między małym zbiorem punktów stałych, zamiast oferować gładki kontinuum możliwości.
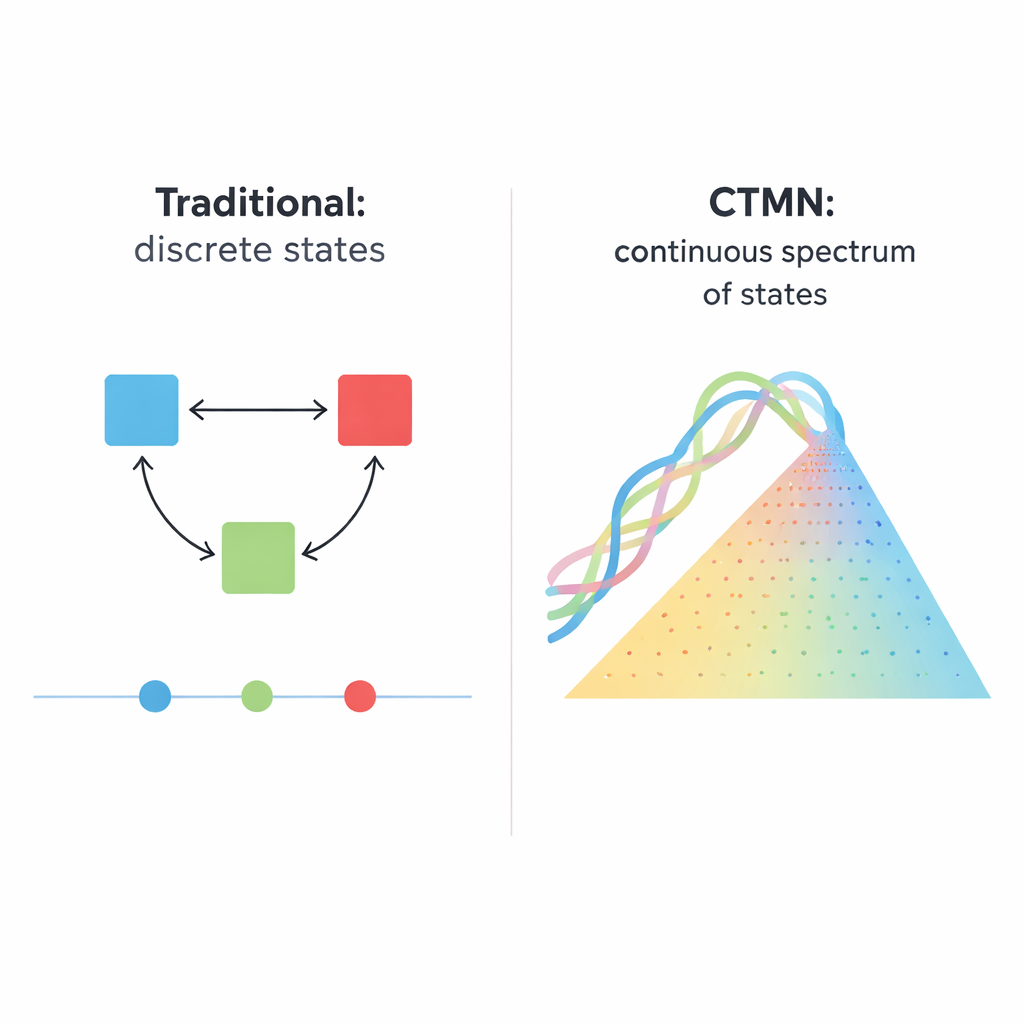
Nowy typ sieci DNA: ciągle regulowana
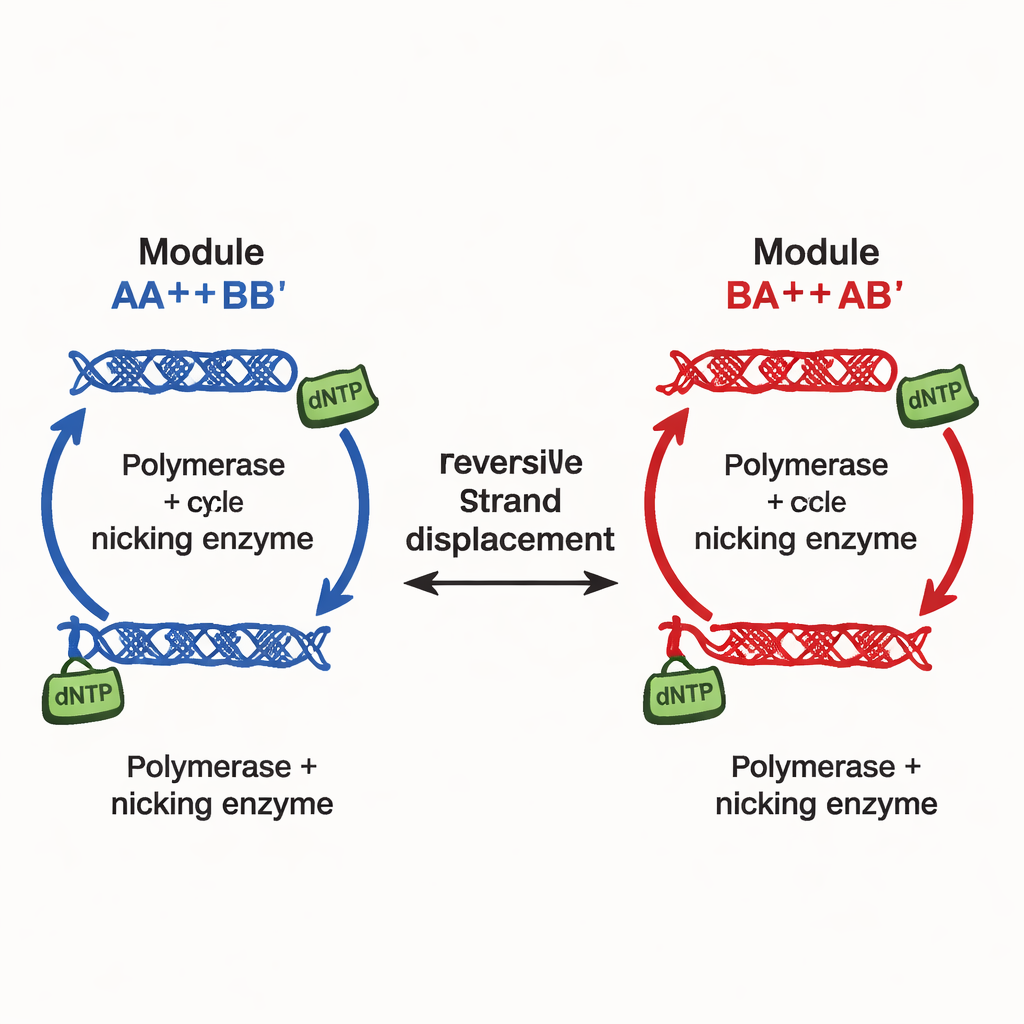
Autorzy wprowadzają inny zasadniczy projekt, zaimplementowany w tym, co nazywają sieciami wielostabilności ciągle regulowanej (CTMN). Zamiast polegać na wielu oddzielnych sygnałach hamujących, stosują bezpośrednią konkurencję między modułami replikacji DNA połączonymi odwracalnymi reakcjami wymiany nici. Każdy moduł składa się z zaprojektowanych dupleksów DNA, które zarówno biorą udział w wymianie nici, jak i służą jako matryce dla polimerazy DNA, wspomaganej przez enzym tnący (nicking), który przecina i odtwarza kluczowe fragmenty. Paliwem chemicznym są nukleotydy (dNTP), które napędzają ciągłą polimeryzację i cięcie, utrzymując system daleko od równowagi. W tych warunkach konkurujące moduły w praktyce „zamrażają się” w tych względnych proporcjach, z którymi występowały początkowo, dając nie tylko dwa lub trzy wyniki, lecz całą ciągłą linię (lub, dla większej liczby modułów, płaszczyznę) długotrwałych stanów.
Jak maszyny molekularne utrwalają pamięć
W najprostszej sieci dwu‑modułowej, CTMN‑1, zespół wykazuje eksperymentalnie i za pomocą szczegółowego modelowania kinetycznego, że system może osiągnąć rodzinę stabilnych mieszanin obejmującą niemal pełen zakres od „przeważająco moduł A” do „przeważająco moduł B”. Polimeryzacja przekształca aktywne dupleksy w formy wydłużone, które są tymczasowo wyłączone z konkurencji wymiany nici; cięcie następnie je przywraca, zamykając pętlę autoregulacyjną. Gdy oba moduły dzielą taką pętlę, silnie tłumią wzajemną konwersję, tak że system pozostaje zablokowany blisko składu początkowego przez wiele godzin, pod warunkiem dostępności paliwa. Analiza stabilności liniowej równań opisujących układ ujawnia całą rozmaitość stanów — w praktyce kontinuum — punktów stacjonarnych, w przeciwieństwie do pojedynczego punktu stałego obserwowanego po usunięciu enzymów lub paliwa.
Programowalne odpowiedzi i molekularna pamięć
Ponieważ stan sieci jest przechowywany w składach DNA, można nim sterować i go odczytywać w sposób programowalny. Autorzy projektują krótkie wyzwalacze RNA, które tymczasowo wiążą specyficzne nici DNA, faworyzując konkurencję i przesuwając sieć w kierunku nowego składu. Nawet po rozłożeniu RNA przez enzym, nowy stan utrzymuje się, działając jako forma molekularnej pamięci. Powtarzane lub silniejsze bodźce przesuwają system płynnie po kontinuum stanów, zamiast przełączać go między prostymi pozycjami włącz/wyłącz. Co więcej, produkty replikacji DNA można dostosować tak, by działały jako sygnały dla procesów dalszych etapów: w demonstracjach różne stany CTMN‑1 selektywnie aktywowały jeden z dwóch katalizatorów opartych na DNA lub przesuwały transkrypcję RNA w stronę jednego z dwóch mRNA, nie zakłócając podstawowej wielostabilności.
Skalowanie do złożonych molekularnych „ściemniaczy”
Aby pokazać, że strategia jest skalowalna, badacze zbudowali sieć trójmodułową, CTMN‑2, dodając więcej zaprojektowanych dupleksów DNA, które dzielą wspólną domenę wymiany, lecz kodują różne matryce replikacji. Teraz możliwe stany stacjonarne wypełniają obszar dwuwymiarowy, jak punkty na trójkątnym diagramie fazowym, zamiast prostoliniowego kontinuum. Eksperymenty ponownie potwierdzają, że wiele odmiennych składów jest stabilnych, dopóki dostępne są paliwo i enzymy, a wszystkie zapadają do pojedynczego punktu równowagi po usunięciu dopływu energii. Ponieważ dodanie nowych modułów wymaga jedynie nowych konstrukcji DNA wpasowujących się w tę samą ramę wymiany nici, ogólne okablowanie nie rozrasta się tak skomplikowanie jak w tradycyjnych projektach.
Co to oznacza dla przyszłych technologii molekularnych
Dla laika kluczowy wniosek jest taki, że autorzy przekształcili sieć replikacji DNA w wysoce elastyczne, analogowe urządzenie pamięciowe. Zamiast wybierać spośród kilku wcześniej ustawionych opcji, ich system może niezawodnie utrzymać jeden z dziesiątek eksperymentalnie rozróżnialnych stanów, zdefiniowany przez udział poszczególnych modułów DNA, i potrafi przekształcać przejściowe impulsy chemiczne w długotrwałe przesunięcia wzdłuż tego kontinuum. Ponieważ nici wyjściowe DNA są programowalne i odseparowane od mechanizmu stabilizującego, ta sama struktura może w zasadzie regulować szeroki zakres reakcji biochemicznych lub właściwości materiałów z drobną, gradacyjną kontrolą. Praca ta wskazuje więc drogę do molekularnych urządzeń, które obliczają, pamiętają i adaptują się bardziej jak systemy analogowe — sieci nerwowe lub mechaniczne — niż jak proste przełączniki cyfrowe.
Cytowanie: Zhong, R., Fu, Y., Jiang, S. et al. Continuously tunable multistability in DNA replication networks. Nat Commun 17, 1782 (2026). https://doi.org/10.1038/s41467-026-68488-z
Słowa kluczowe: wielostabilność DNA, molekularna pamięć, syntetyczne sieci biochemiczne, wymiana nici DNA (strand displacement), analogowe przetwarzanie molekularne