Clear Sky Science · pl
Solidne i interpretowalne przewidywanie markerów genowych i typów komórek z danych przestrzennej transkryptomiki
Przekształcanie rutynowych preparatów tkankowych w mapy molekularne
Gdy pobiera się biopsję, lekarze zwykle widzą tylko to, co ujawnia mikroskop: kształty i wzory komórek w różowo-fioletowych barwieniach. Jednak pod tymi kolorami kryje się ukryty świat genów włączających się i wyłączających, wpływających na to, jak nowotwór rośnie i reaguje na leczenie. W tym badaniu przedstawiono STimage, nowy system sztucznej inteligencji (SI), który ma na celu odczytywać ten molekularny skrypt bezpośrednio ze standardowych obrazów patologicznych, co potencjalnie pozwala na szybsze i tańsze wnioski bez dodatkowych badań laboratoryjnych.
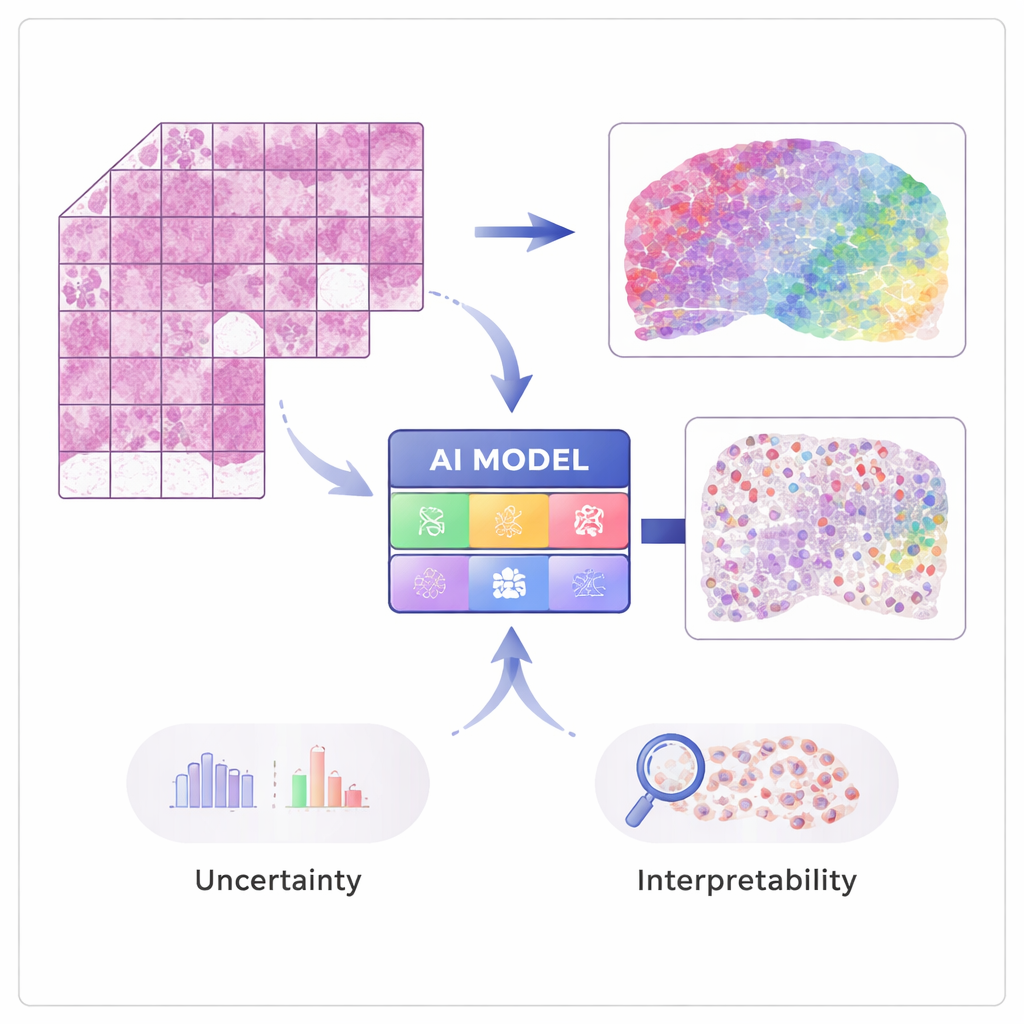
Od obrazu do aktywności genów
Nowoczesne techniki „przestrzennej transkryptomiki” potrafią mierzyć aktywność dziesiątek tysięcy genów, zachowując jednocześnie informację o pochodzeniu sygnału w tkance. Metody te są potężne, ale kosztowne i jeszcze nie powszechne w szpitalach. STimage jest trenowany na umiarkowanej liczbie takich przestrzennych zestawów danych, w których każdy obraz tkanki jest sparowany z dokładnymi pomiarami genów w wielu drobnych punktach. SI uczy się kojarzyć lokalne wzory wizualne na barwionych preparatach hematoksyliną i eozyną (H&E) — na przykład gęstość czy nieregularność jąder komórkowych — z ukrytą aktywnością genów, tak aby później móc przewidywać ekspresję genów i typy komórek jedynie na podstawie zwykłych obrazów.
Budowanie bardziej godnego zaufania patologicznego SI
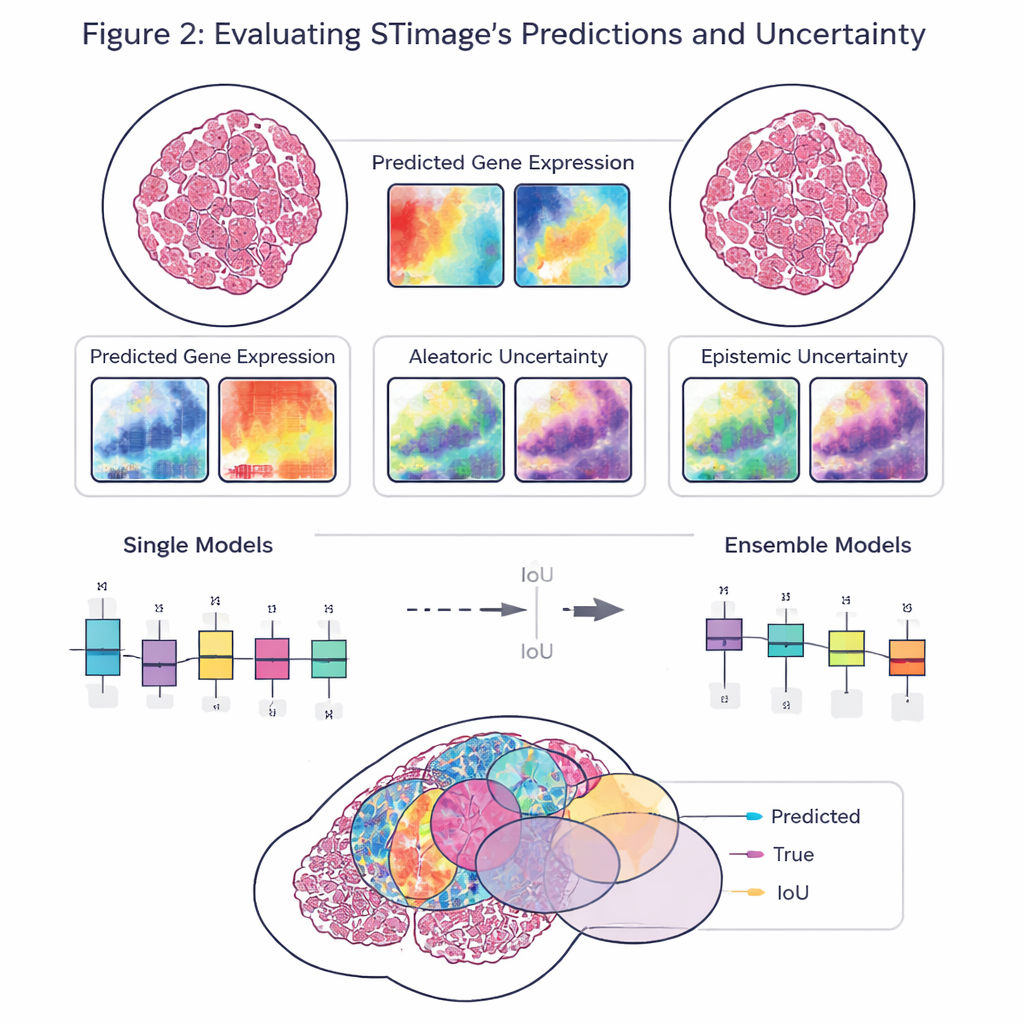
Kluczowym celem pracy jest nie tylko dokładność, lecz także niezawodność i wyjaśnialność. Zamiast zwracać pojedynczą liczbę dla każdego genu, STimage przewiduje pełny rozkład prawdopodobieństwa, opisujący prawdopodobny zakres aktywności genów w danej lokalizacji. Rozdziela też dwa rodzaje niepewności: jedną spowodowaną hałasem lub zmiennością danych, a drugą odzwierciedlającą własny brak wiedzy modelu. Trenując wiele nieznacznie różnych wersji modelu i uśredniając ich wyniki — podejście typu „ensemble” — badacze zarówno poprawiają wydajność, jak i uzyskują jaśniejsze wyobrażenie o tym, gdzie system ma pewność, a gdzie jej brak, co jest kluczowe dla decyzji klinicznych.
Testowanie w różnych nowotworach, technologiach i szpitalach
Zespół oceniał STimage na zróżnicowanych zbiorach danych z nowotworów piersi, skóry i nerek, a także w chorobie wątroby związanej z układem odpornościowym. Nauczył się przewidywać ważne markery nowotworowe i immunologiczne, często odpowiadające rzeczywistym przestrzennym wzorom widzianym w niezależnych eksperymentach. Model sprawdzał się także w obliczu danych z różnych laboratoriów, metod przygotowania próbek, a nawet różnych technologii podstawowych, w tym platform o rozdzielczości pojedynczej komórki i starszych systemów o niższej rozdzielczości. W porównaniach bezpośrednich z kilkoma istniejącymi narzędziami SI, STimage i jego warianty ensemble zwykle wypadały lepiej, szczególnie gdy oceniano, jak dobrze przewidywane wzory odpowiadają rzeczywistemu rozkładowi aktywności genów w tkance.
Wgląd w guzy: komórki, przeżywalność i odpowiedź na leki
STimage idzie dalej niż prognozowanie genów i wnioskuje, które typy komórek zajmują poszczególne rejony, wykorzystując dane o wysokiej rozdzielczości, gdzie tożsamość każdej komórki jest znana. Model potrafił odróżnić komórki nowotworowe od komórek układu odpornościowego i komórek podporowych oraz odwzorować ich rozmieszczenie na preparacie. Autorzy następnie zastosowali STimage do dużych zbiorów rutynowych obrazów nowotworowych z The Cancer Genome Atlas. Nawet bez przestrzennych pomiarów, przewidywane profile genowe SI były ściśle zbieżne z rzeczywistymi danymi zbiorczymi (bulk). Te przewidywania były wystarczająco silne, by grupować pacjentów na kategorie o wyższym i niższym ryzyku oraz pomagać w odróżnieniu tych, którzy mają większe szanse na pełną odpowiedź na niektóre terapie raka piersi.
Dlaczego to ma znaczenie dla przyszłych pacjentów
Dla pacjentów i klinicystów obietnica STimage to coś w rodzaju „nakładki molekularnej” na dobrze znany preparat patologiczny. Zamiast zlecać wiele kosztownych badań, pojedynczy zeskanowany obraz mógłby pewnego dnia ujawniać, gdzie aktywne są agresywne programy genowe, jak rozmieszczone są komórki odpornościowe oraz które markery wskazują na lepsze lub gorsze rokowanie albo różne odpowiedzi na leki. Choć metoda jest wciąż udoskonalana, a korelacja z rzeczywistymi pomiarami nie jest idealna, jej zdolność do wychwytywania wzorów przestrzennych, szacowania własnej niepewności i wskazywania, które komórki napędzają przewidywania, stanowi praktyczny krok w stronę bardziej informacyjnej i przejrzystej patologii cyfrowej.
Cytowanie: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
Słowa kluczowe: patologia cyfrowa, przestrzenna transkryptomika, markery nowotworowe, uczenie głębokie, mikrośrodowisko guza