Clear Sky Science · pl
PTRAMP, CSS i Ripr tworzą zachowany kompleks niezbędny do inwazji merozoitów Plasmodium do erytrocytów
Dlaczego to ma znaczenie w walce z malarią
Pasożyty malarii muszą wniknąć do naszych czerwonych krwinek, by wywołać chorobę. To badanie ujawnia niewielki zestaw białek, które tworzą wspólny „most wsiadaniowy” wykorzystywany przez kilka głównych gatunków malarii, w tym te infekujące ludzi. Pokazując, jak ten most jest zbudowany i jak przeciwciała mogą czasem go blokować, praca wskazuje nowe drogi projektowania szczepionek, które mogłyby jednocześnie chronić przed więcej niż jednym rodzajem malarii. 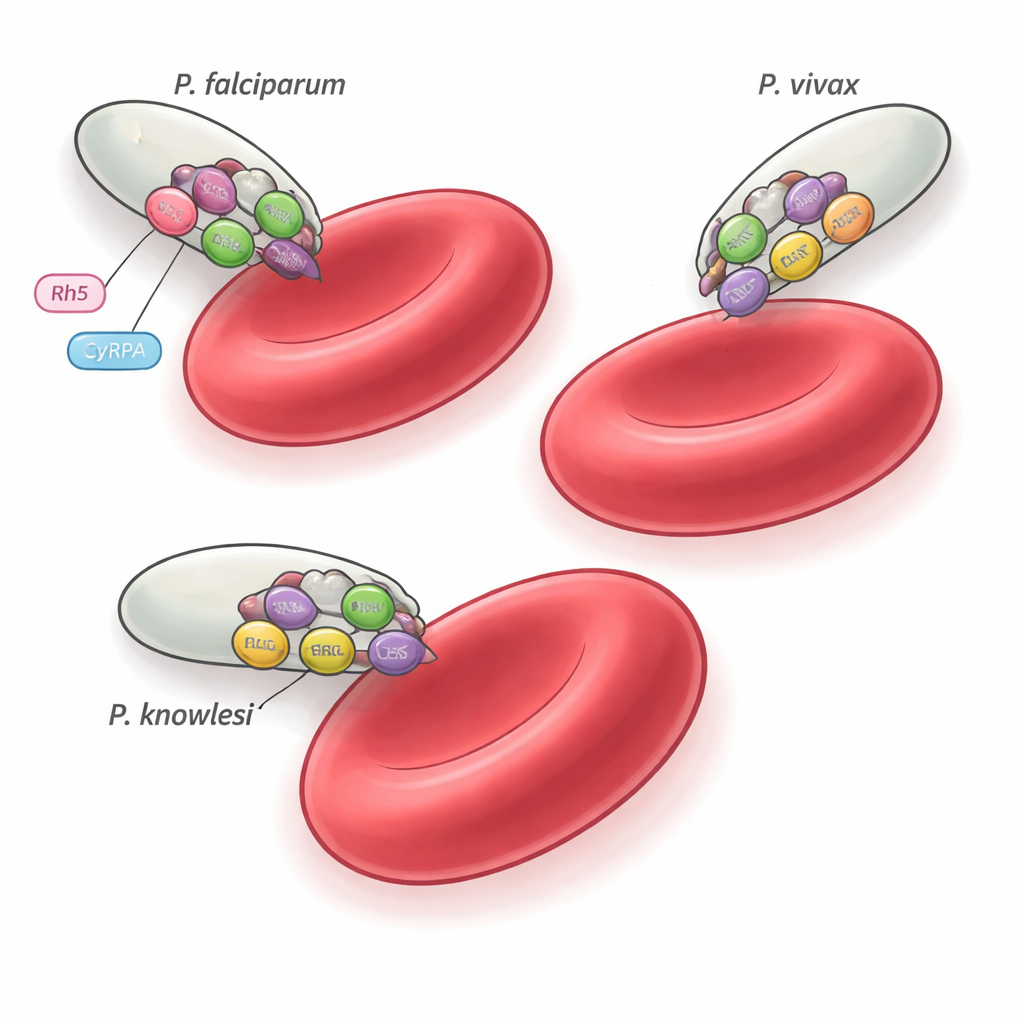
Wspólny zestaw narzędzi u wielu pasożytów malarii
Istnieje ponad 200 gatunków Plasmodium, ale tylko garstka, takich jak P. falciparum, P. vivax i P. knowlesi, infekuje ludzi. Gatunki te leżą na różnych gałęziach drzewa rodowego pasożytów i preferują różne typy czerwonych krwinek, a mimo to wszystkie muszą z wyjątkową precyzją wniknąć do erytrocytów. Wcześniejsze badania w P. falciparum zidentyfikowały pięcioczęściowy zespół, kompleks PCRCR, który jest niezbędny do inwazji i wiąże się z receptoriem czerwonej krwinki zwanym basiginą. Jeden element tego kompleksu, białko o nazwie Rh5, występuje tylko u P. falciparum i jego bliskich krewnych, co rodzi pytanie: czego używają inne gatunki malarii? Obecne badanie skupia się na trzech towarzyszących białkach — PTRAMP, CSS i Ripr — które są zachowane w całym rodzaju i sprawdza, czy tworzą uniwersalną maszynę inwazyjną.
Budowanie trójskładnikowego mostu inwazyjnego
Na podstawie przeszukań sekwencji w wielu genomach pasożytów autorzy pokazują, że PTRAMP, CSS i Ripr występują we wszystkich głównych liniach Plasmodium, w przeciwieństwie do Rh5, który jest ograniczony do jednej podgrupy. Predykcja struktury za pomocą AlphaFold, połączona ze szczegółowymi pomiarami biochemicznymi, ujawnia, że PTRAMP i CSS łączą się, tworząc stabilną parę, spajaną przez specyficzny mostek disiarczkowy między dwiema zachowanymi cysteinami. Ta dwubiałkowa platforma zaciska się następnie na końcowym fragmencie Ripr, tworząc trójskładnikowy kompleks PTRAMP–CSS–Ripr (PCR). Eksperymenty z białkami z P. falciparum, P. vivax i P. knowlesi pokazują, że kompleks ten tworzy się we wszystkich trzech gatunkach z wysokim powinowactwem, a tylko niewielki region na końcu C‑terminalnym Ripr jest potrzebny do silnego wiązania. 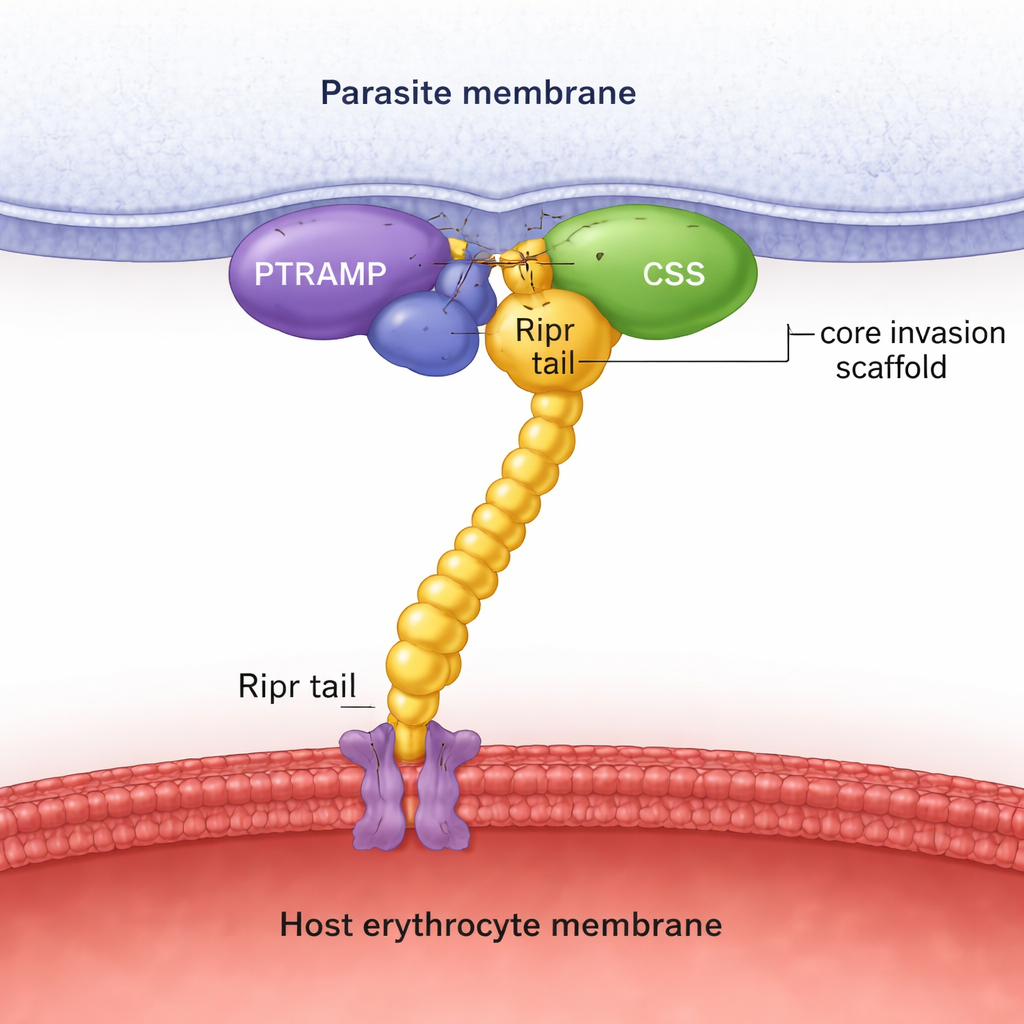
Obserwacja struktury w skali atomowej
Aby wyjść poza przewidywania, zespół rozwiązał struktury krystaliczne i zebrał obrazy za pomocą kriotransmisyjnej mikroskopii elektronowej. Struktura krystaliczna pary PTRAMP–CSS z P. vivax pokazuje dokładnie, jak krótki fragment PTRAMP przeplata się przez CSS i tworzy kluczowe wiązanie disiarczkowe. Inna struktura ukazuje silne przeciwciało związane z dwoma domenami przypominającymi czynniki wzrostu Ripr, mapując epitop hamujący na ogonie Ripr. Analiza cryo‑EM kompleksu PCR z P. knowlesi potwierdza ogólny kształt przewidywany przez AlphaFold: PTRAMP i CSS leżą blisko błony pasożyta i uchwycają Ripr, którego wydłużone ciało sięga w stronę komórki gospodarza. Te strukturalne migawki wspierają koncepcję, że trójka PCR tworzy sztywny ruszt, który fizycznie rozciąga się między pasożytem a czerwoną krwinką podczas inwazji.
Przeciwciała rozpoznające więcej niż jeden gatunek
Ponieważ te białka są zachowane, autorzy zapytali, czy infekcje u ludzi naturalnie generują przeciwciała krzyżowo reagujące między gatunkami. Osocze pacjentów zakażonych P. falciparum, P. vivax lub P. knowlesi wykazywało silne reakcje przeciwciał przeciwko CSS i Ripr z wielu gatunków, co sugeruje, że ludzie rozwijają przeciwciała przeciw wspólnym regionom kompleksu PCR. Zespół następnie wytworzył przeciwciała monoklonalne i nanoprzeciwciała skierowane przeciw PTRAMP, CSS i Ripr z P. vivax i przetestował, czy potrafią one zablokować wzrost pasożytów w hodowli. Niektóre przeciwciała, zwłaszcza jedno nazwane 5B3, które wiąże ogon Ripr, były w stanie hamować inwazję P. knowlesi i przy wyższych stężeniach P. falciparum. Zaskakująco, te same przeciwciała nie zatrzymywały P. vivax ani blisko spokrewnionego pasożyta małp P. cynomolgi, chociaż mogły wiązać białka z tych gatunków.
Wspólny ruszt z gatunkowo‑specyficznymi dodatkami
Testy funkcjonalne pokazują, że sam kompleks PCR nie przyczepia się bezpośrednio do czerwonych krwinek; raczej pełni prawdopodobnie rolę zachowanego rusztu strukturalnego, do którego każdy gatunek podłącza własnych partnerów wiążących receptory. W P. falciparum, na przykład, trio PCR współpracuje z CyRPA i Rh5, aby zaangażować basiginę na ludzkich erytrocytach. W P. vivax i P. knowlesi równoważne białka wiążące receptory i docelowe struktury gospodarza pozostają nieznane, ale ta sama oś PTRAMP–CSS–Ripr wydaje się organizować maszynerię inwazyjną. Fakt, że niektóre przeciwciała krzyżowo reagują, a jednak hamują tylko wybrane gatunki, podkreśla, jak subtelne różnice w składaniu kompleksu i czasie jego działania mogą zmieniać podatność na atak immunologiczny.
Co to oznacza dla przyszłych szczepionek przeciwko malarii
Dla osoby nietechnicznej najważniejszy wniosek jest taki, że pasożyty malarii bardzo różnych gatunków dzielą wspólny „wtyk”, którego używają do wejścia do czerwonych krwinek — złożony z białek PTRAMP, CSS i Ripr — chociaż łączą ten wtyk z różnymi receptorami na powierzchni komórki. Ten zachowany wtyk jest teraz zmapowany strukturalnie i w niektórych przypadkach może być trafiony przez przeciwciała działające między gatunkami. Choć potrzebne są dalsze badania, by zidentyfikować pełny zestaw białek‑partnerów i ulepszyć przeciwciała hamujące, odkrycie uniwersalnego rusztu inwazyjnego otwiera drogę do projektów szczepionek, które mogłyby chronić przed kilkoma rodzajami malarii zamiast jednego.
Cytowanie: Seager, B.A., Lim, P.S., Xiao, X. et al. PTRAMP, CSS and Ripr form a conserved complex required for merozoite invasion of Plasmodium species into erythrocytes. Nat Commun 17, 1780 (2026). https://doi.org/10.1038/s41467-026-68486-1
Słowa kluczowe: inwazja malarii, białka Plasmodium, wejście merozoitu, szczepionka międzygatunkowa, infekcja erytrocytów