Clear Sky Science · pl
Tomografia krioelektronowa ujawnia sprzężoną replikację, pączkowanie i dojrzewanie flawiwirusów
Jak wirusy atakujące mózg przejmują błony komórkowe
Flawiwirusy, duża grupa wirusów obejmująca sprawców gorączki denga i kleszczowego zapalenia mózgu, potrafią zainwadować mózg i wywołać poważne choroby. Jednak to, w jaki sposób te maleńkie patogeny kopiują swój materiał genetyczny i składają nowe cząstki wirusa wewnątrz naszych komórek, pozostawało w dużej mierze ukryte. W badaniu wykorzystano zaawansowane trójwymiarowe obrazowanie elektroniczne w niskich temperaturach, aby obserwować flawiwirusy przenoszone przez kleszcze w działaniu wewnątrz komórek ludzkich i tkanki mózgowej myszy, ujawniając zaskakująco ścisłe sprzężenie między kopiowaniem genomu, składaniem wirusa i jego dojrzewaniem.
Fabryki wirusowe ukryte w błonach komórkowych
Flawiwirusy nie unoszą się w komórce podczas replikacji. Zamiast tego przebudowują system błonowy komórki zwany retikulum endoplazmatycznym (ER), tworząc wyspecjalizowane kieszonki znane jako organella replikacyjne. Wyglądają one jak drobne wpuklenia na powierzchni ER i pełnią rolę chronionych przestrzeni, w których kopiowane są genomy wirusowego RNA. Przy użyciu tomografii krioelektronowej — techniki tworzącej trójwymiarowe migawki komórek szybko zamrażanych w stanie bliskim naturalnemu — badacze zobrazowali te wpuklenia w ludzkich komórkach płuc zakażonych flawiwirusem przenoszonym przez kleszcze, spokrewnionym z wirusem kleszczowego zapalenia mózgu. Stwierdzili, że ER wokół zakażonych obszarów pęcznieje i jest wypełnione skupiskami tych organelli replikacyjnych; niektóre są puste, inne zaś wypełnione gęstym, nitkowatym RNA.
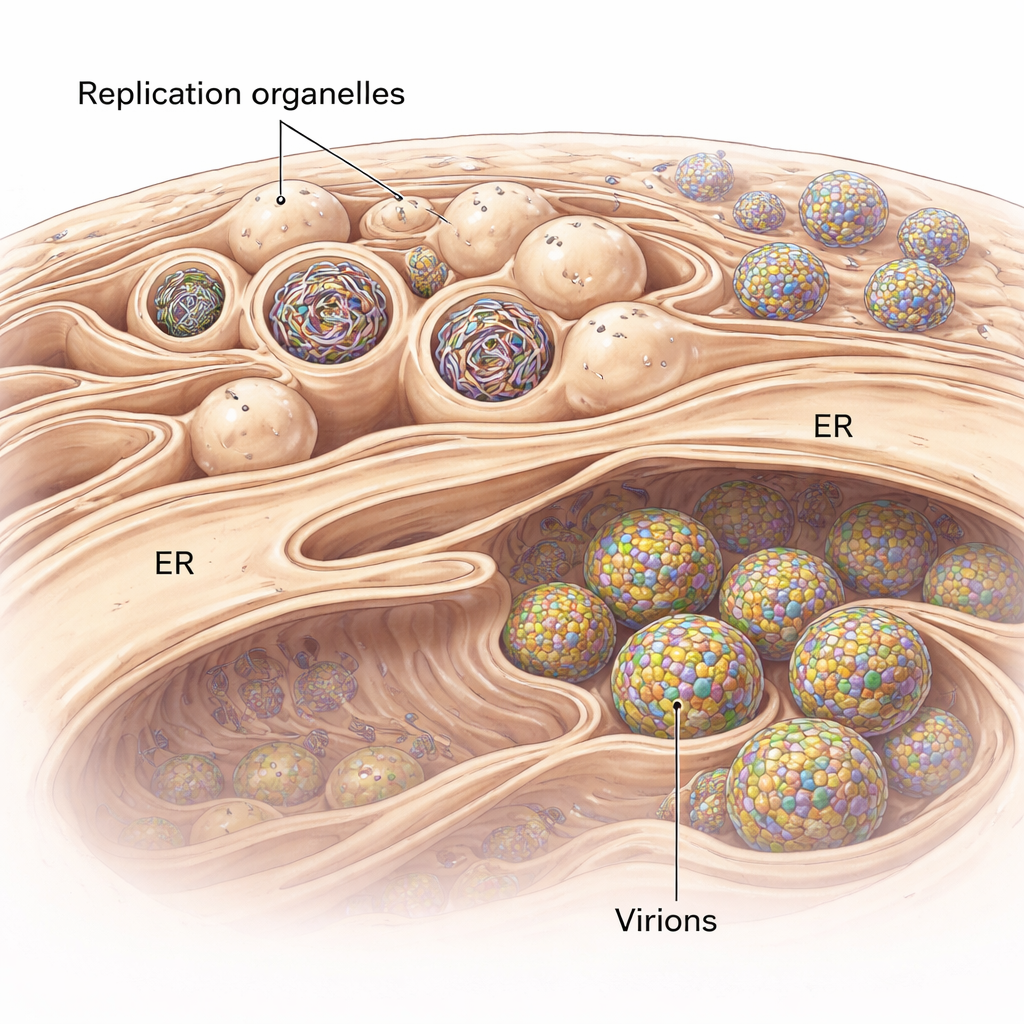
Budowanie perfekcyjnej wirusowej bańki
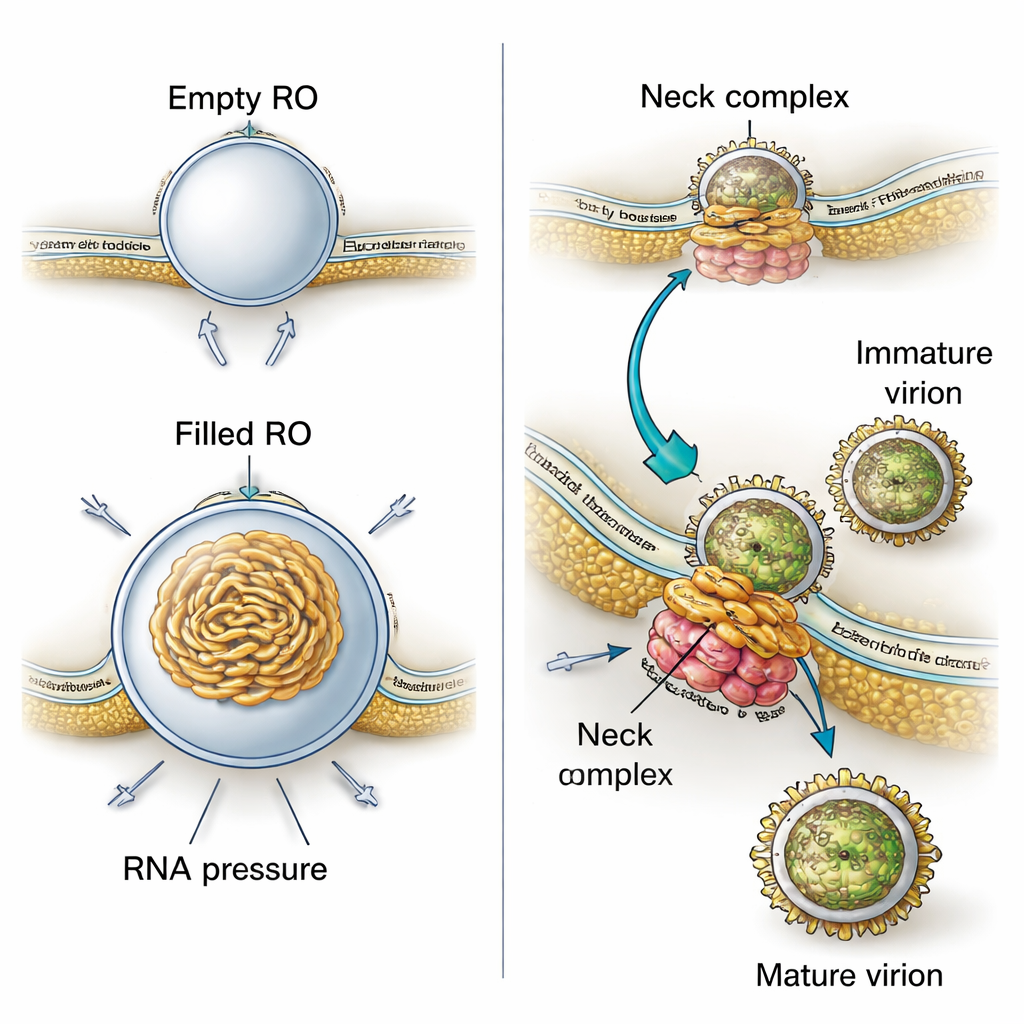
Dlaczego te błonowe kieszonki mają tak precyzyjny, pączkowy kształt? Łącząc obrazy 3D z modelowaniem fizycznym, autorzy pokazują, że działają dwie siły. Po pierwsze, błona organelli replikacyjnej jest konsekwentnie grubsza niż zwykłe ER, co sugeruje, że białka wirusowe lub zmienione lipidy usztywniają i nadają błonie krzywiznę, formując stabilne wpuklenie jeszcze przed wejściem RNA. Po drugie, gdy wirusowe RNA jest obecne, zwija się wewnątrz kieszonki i wypycha ją na zewnątrz, zwiększając rozmiar pączka. Obliczenia oparte na mierzonej wielkości wskazują, że każde wypełnione organellum zawiera ciśnienie odpowiadające mniej więcej jednej kopii genomu wirusa w postaci dwuniciowej. Oznacza to, że wirus wykorzystuje zarówno uprzednio ukształtowaną błonę, jak i fizyczny nacisk własnego materiału genetycznego do budowy i stabilizacji swoich miniaturowych fabryk.
Linia montażowa: od kopiowania genomu do nowych wirusów
Badanie ukazuje także, jak blisko produkcja wirusów związana jest z tymi miejscami replikacji. W widokach 3D badacze często obserwowali nowe cząstki wirusa tworzące się tuż obok organelli replikacyjnych, pączkujące do pobliskich przestrzeni przypominających ER. Cząstki niedojrzałe miały kolczastą powierzchnię, podczas gdy bardziej dojrzałe sprawiały wrażenie gładkich. Pomiary odległości w tomogramach pokazały, że niedojrzałe cząstki leżą bliżej organelli replikacyjnych niż dojrzałe, co sugeruje, że przemieszczając się zaledwie na krótką odległość przez splecione przegrody błonowe, przechodzą strukturalne zmiany niezbędne do uzyskania zakaźności. Duży kompleks białkowy w wąskiej „szyjce”, gdzie każde wpuklenie replikacyjne łączy się z cytoplazmą, wydaje się kotwiczyć organellum replikacyjne do sąsiedniej błony, w której zachodzi pączkowanie. Ten kompleks prawdopodobnie działa jak molekularny zamek błyskawiczny koordynujący produkcję RNA z pakowaniem tego RNA do nowych cząstek wirusa.
Dostrajanie dojrzewania jednym aminokwasem
Aby zrozumieć, jak kontrolowane jest dojrzewanie wirusa, zespół porównał dwie wersje chimerycznego wirusa różniące się tylko jednym aminokwasem w miejscu rozpoznawanym przez enzym gospodarza zwanego furyną. Enzym ten przecina białko powierzchniowe wirusa, pomagając przekształcić niedojrzałe kolczaste cząstki w gładkie, dojrzałe. W testach cięcia in vitro i w zakażonych komórkach wariant z argininą w tej pozycji był szybciej cięty niż wariant z glutaminą. W obrazach z tomografii krioelektronowej szybciej cięty wirus wytwarzał wyższy odsetek dojrzałych cząstek w pobliżu organelli replikacyjnych. Pomimo tych mikroskopowych różnic, oba warianty wykazywały podobny wzrost i przebieg choroby w modelu myszy, co sugeruje, że wirus toleruje zakres efektywności dojrzewania, zachowując przy tym zakaźność.
Bezpośrednie obserwowanie infekcji w mózgu
Większość badań strukturalnych wirusów opiera się na liniach komórkowych, ale ta praca sięga do tkanki żywej. Badacze wyizolowali strukturę mózgową zwaną splotem naczyniówkowym od zakażonych myszy i przygotowali ją do tomografii krioelektronowej przy użyciu szybkiego zamrażania pod wysokim ciśnieniem oraz frezowania wiązką zogniskowanych jonów. Nawet w tym złożonym środowisku obserwowali te same charakterystyczne cechy: skupiska organelli replikacyjnych, pogrubione błony i pobliskie pęcherzyki wypełnione dojrzałymi cząstkami wirusa. To dowodzi, że przebudowa błon i ściśle sprzężona sekwencja replikacja–składanie–dojrzewanie widziana w hodowlach komórek zachodzi również w mózgu, gdzie te wirusy wywołują chorobę.
Dlaczego te ukryte procesy mają znaczenie
Dla osób spoza specjalności kluczowy przekaz jest taki, że wirusy te prowadzą wysoko zorganizowaną linię montażową wewnątrz naszych komórek. Modelują błony komórkowe w drobne sprężone bańki, w których kopiowane są genomy, łączą te bańki bezpośrednio z miejscami, gdzie pączkują nowe cząstki, a nawet rozpoczynają końcowe etapy dojrzewania w zasięgu ręki od pierwotnego miejsca replikacji. Identyfikacja pogrubionych błon replikacyjnych, kompleksu białkowego rozciągającego się przez szyjkę i ściśle splecionych przedziałów dojrzewania nie tylko wyjaśnia, jak flawiwirusy replikują się tak wydajnie, lecz także wskazuje nowe cele dla leków przeciwwirusowych mających na celu zakłócenie ukrytych fabryk i torów montażowych wirusa.
Cytowanie: Dahmane, S., Schexnaydre, E., Zhang, J. et al. Cryo-electron tomography reveals coupled flavivirus replication, budding and maturation. Nat Commun 17, 828 (2026). https://doi.org/10.1038/s41467-026-68483-4
Słowa kluczowe: flawiwirus, tomografia krioelektronowa, organella replikacyjne, dojrzewanie wirusa, encefalitis przenoszona przez kleszcze