Clear Sky Science · pl
Spektroelektrochemiczny wgląd w katalizatory miedź-kobalt do współelektroredukcji CO2 i azotynu do mocznika
Przekształcanie gazów odpadowych w nawóz
Nawóz mocznikowy stanowi podstawę współczesnego rolnictwa, jednak jego konwencjonalna produkcja jest energochłonna i emisyjna. W tym badaniu zbadano zupełnie inne podejście: wykorzystanie energii elektrycznej do przekształcenia dwutlenku węgla (CO2) i azotowego odpadku (np. azotynu z spalin lub ścieków) bezpośrednio w mocznik. Dla czytelnika nieprofesjonalnego zaleta jest oczywista: droga do kluczowego nawozu, która mogłaby zmniejszyć emisje, wykorzystać strumienie odpadów jako surowce i w przyszłości być zasilana odnawialną energią elektryczną.
Dlaczego warto przemyśleć produkcję mocznika?
Obecnie mocznik produkuje się głównie przez najpierw wytworzenie amoniaku z azotu i wodoru pochodzącego z paliw kopalnych (proces Habera–Boscha), a następnie reakcję amoniaku z CO2 w wysokich temperaturach i ciśnieniach. Ten łańcuch reakcji jest scentralizowany, kapitałochłonny i emituje prawie tonę CO2 na tonę wyprodukowanego mocznika. Wraz ze wzrostem globalnego zapotrzebowania na nawozy rosną też koszty środowiskowe. Alternatywą jest pominięcie paliw kopalnych przez napędzanie kluczowych etapów chemicznych prądem, najlepiej z odnawialnych źródeł, oraz wykorzystanie CO2 i tlenków azotu (NOx), które obecnie traktowane są jako odpady.
Nowa rola miedzi i kobaltu
Autorzy zaprojektowali cienkowarstwowe katalizatory powstałe w wyniku współrozpylania (co‑sputtering) miedzi (Cu) i kobaltu (Co) na podłożu z włókniny węglowej, precyzyjnie regulując stosunek Cu:Co. Skoncentrowali się na jednoczesnej elektroredukcji CO2 i azotynu (NO2⁻) w wodzie o obojętnym pH — warunku sprzyjającym subtelnemu tworzeniu wiązań węgiel–azot (C–N) niezbędnych do powstania mocznika. Wyróżniającym się składem okazała się mieszanina Cu i Co w stosunku 1:1, która osiąga szybkość produkcji mocznika około 61 mmol na godzinę na gram katalizatora przy umiarkowanym napięciu. Mikroskopia i pomiary rentgenowskie pokazują, że metale są ściśle zmieszane na skali atomowej i pozostają w dużej mierze metaliczne podczas pracy, tworząc odporną platformę, na której zarówno CO2, jak i azotyn mogą efektywnie reagować. 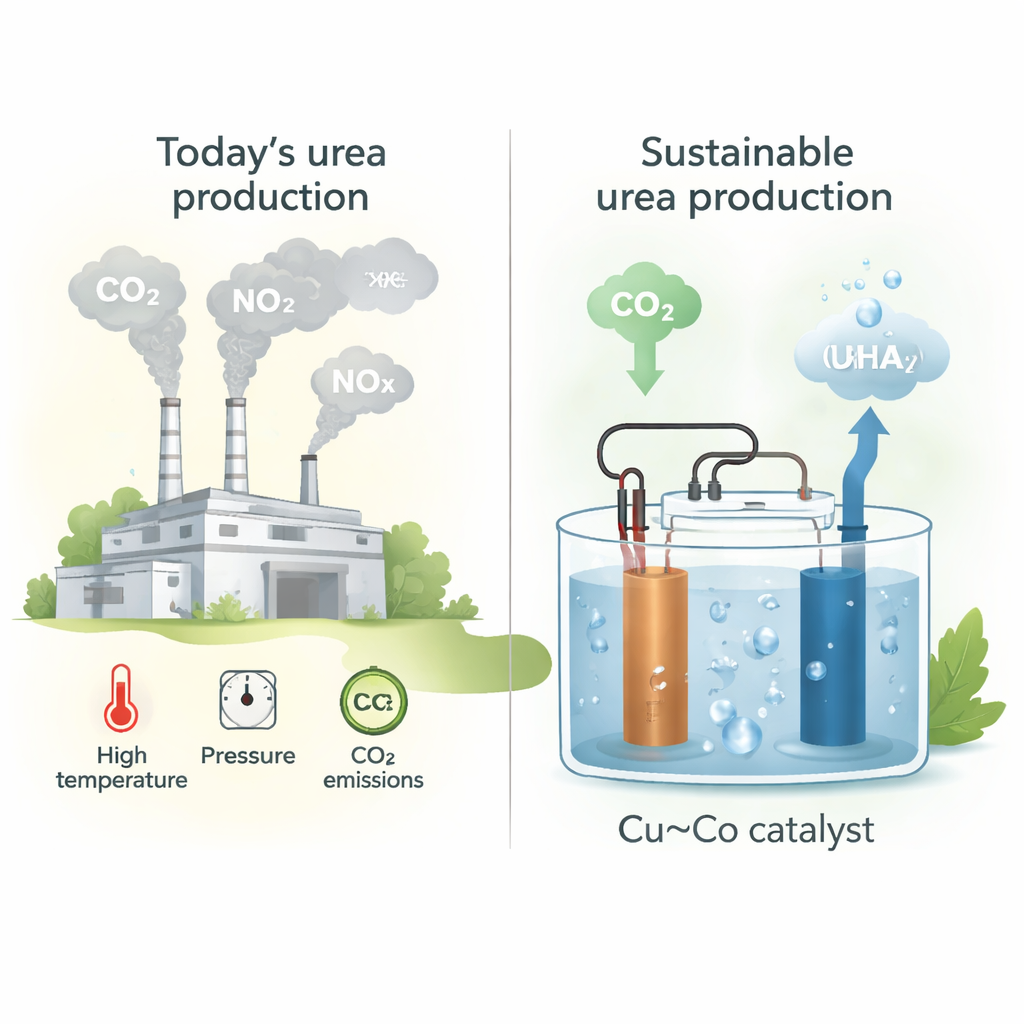
Jak katalizator dzieli i wykonuje pracę
Uzyskanie mocznika tą metodą jest trudne, ponieważ konkurują z nią prostsze reakcje — jak wytwarzanie wodoru czy redukcja CO2 lub azotynu osobno. Klucz, jak ustalili badacze, leży w podziale zadań między miejscami aktywnymi miedzi i kobaltu działającymi wspólnie. Testy elektrochemiczne pokazują, że sama miedź głównie przekształca CO2 w paliwa i związki węglowe, podczas gdy sam kobalt głównie redukuje azotyn do amoniaku, bez powstawania mocznika w żadnym z tych przypadków. Dopiero gdy atomy Cu i Co są blisko wymieszane, obserwuje się istotne tworzenie mocznika. Spektroskopowe „migawki” wykonywane w trakcie reakcji wykrywają charakterystyczne fragmenty związane z powierzchnią: gatunki węglowe pochodzące z CO2 (*CO i *COOH), które preferują powierzchnie miedzi, oraz gatunki azotowe pochodzące z azotynu (*NH2 i pokrewne), które preferują kobalt. Na granicach między Cu i Co te fragmenty mogą się spotkać i sprzęgać, tworząc szkielet C–N mocznika.
Znajdowanie właściwych warunków do tworzenia wiązań
Badanie pokazuje, że sam skład to za mało; otaczający roztwór i membrana także muszą być dostrojone. Mocznik pojawia się tylko w obojętnym elektrolitycie wodorowęglanowym, który utrzymuje wystarczającą ilość rozpuszczonego CO2 i dostarcza odpowiednią ilość protonów (jonów wodorowych) do napędzania etapów „sprzężonego przeniesienia proton–elektron” bez zalania powierzchni reakcją ewolucji wodoru. W warunkach silnie kwaśnych lub silnie zasadowych mocznik albo nie powstaje, albo szybko rozkłada się do prostszych produktów. Doświadczenia z różnymi źródłami azotu pokazują, że azotyn jest szczególnie efektywny do tworzenia mocznika, przewyższając azotan i hydroksyloaminę. Testy przeprowadzone przez wiele godzin wskazują, że folie Cu–Co są stosunkowo stabilne, z jedynie umiarkowanymi stratami metali i utrzymującą się produkcją mocznika.
Zajrzenie pod maskę za pomocą teorii
Aby zrozumieć, dlaczego ten tandemowy katalizator działa tak dobrze, zespół wykorzystał symulacje komputerowe oparte na teorii funkcjonału gęstości. Obliczenia wspierają koncepcję, że miedź sprzyja wiązaniu gatunków pochodzących z CO2, podczas gdy kobalt lepiej aktywuje azotyn i stabilizuje fragmenty zawierające azot. Symulacje wskazują na konkretny etap jako energetyczne wąskie gardło: sprzęgnięcie fragmentu *NH2 (z azotynu) z fragmentem *COOH (z CO2) w celu utworzenia przejściowego połączenia czasem zapisywanego jako *NH2CO. Gdy ten element powstanie, kolejne kroki prowadzące do mocznika są względnie łatwe. Interfejs Cu–Co obniża koszt energetyczny tego kluczowego sprzęgnięcia w porównaniu z czystą miedzią lub czystym kobaltem, co wyjaśnia obserwowany eksperymentalnie wzrost wydajności mocznika w układzie bimetalicznym. 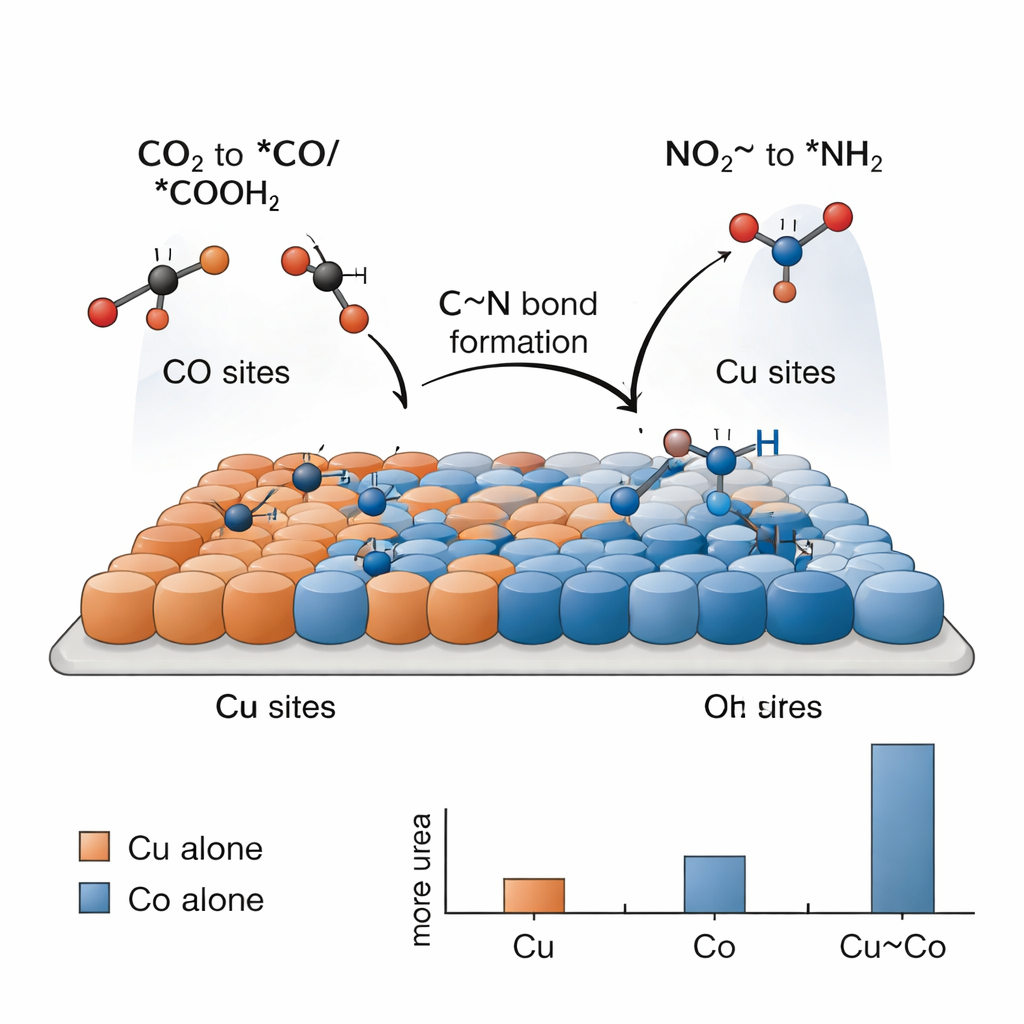
Od laboratoryjnego wglądu do bardziej zielonego nawozu
W praktycznym ujęciu ta praca jeszcze nie zastępuje dzisiejszych gigantycznych zakładów produkujących mocznik, ale wyjaśnia, jak można zaprojektować przyszłą drogę elektrochemiczną. Pokazując, że miedź i kobalt mogą działać w tandemie — jeden dostarczając aktywowane gatunki węglowe, drugi aktywowane gatunki azotowe, obie strony działające przy starannie kontrolowanych warunkach protonowych — badanie wyznacza realistyczną ścieżkę ku czystszej, potencjalnie zdecentralizowanej produkcji mocznika, wykorzystującej CO2 i odpady azotowe jako zasoby zamiast zanieczyszczeń.
Cytowanie: Ramadhany, P., Trần-Phú, T., Yuwono, J.A. et al. Spectroelectrochemical insight into copper cobalt catalysts for CO2 and nitrite co-electroreduction to urea. Nat Commun 17, 1776 (2026). https://doi.org/10.1038/s41467-026-68481-6
Słowa kluczowe: elektrochemiczna synteza mocznika, katalizator miedź-kobalt, zagospodarowanie CO2, redukcja azotynu, wiązanie C–N