Clear Sky Science · pl
Strukturalne podstawy selektywnej inhibicji ludzkiego transportera GABA GAT3
Dlaczego uspokajanie sygnałów mózgowych ma znaczenie
Nasz mózg opiera się na delikatnej równowadze między sygnałami pobudzającymi a tymi uspokajającymi. Kluczowym „uspokajającym” przekaźnikiem jest GABA, substancja chemiczna, która pomaga zapobiegać niekontrolowanej aktywności związanej z takimi schorzeniami jak padaczka, uszkodzenia po udarze czy choroba Alzheimera. W tej pracy skupiono się na białku zwanym GAT3, które usuwa GABA z przestrzeni wokół komórek nerwowych. Ukazując w szczegółach atomowych, jak nowa cząsteczka łączy się z GAT3 i go wyłącza, autorzy dostarczają strukturalnej mapy drogowej do projektowania kolejnej generacji leków, które mogłyby delikatnie wzmocnić naturalny hamulec mózgu.
Własny hamulec mózgu
GABA jest głównym hamującym, czyli uspokajającym, neuroprzekaźnikiem w ośrodkowym układzie nerwowym. Po uwolnieniu z zakończeń nerwowych musi być szybko usunięty, by obwody mózgowe mogły się zresetować. Za porządkowanie odpowiadają białkowe transportery, które pompują GABA z powrotem do komórek. Dwa z tych transporterów dominują w mózgu: GAT1, występujący głównie na neuronach, oraz GAT3, obecny w komórkach pomocniczych zwanych astrocytami. Chociaż lek blokujący GAT1 (tiagabina) stosowany jest od dekad w leczeniu padaczki, porównywalne środki celujące w GAT3 pozostawały w tyle. GAT3 budzi jednak szczególne zainteresowanie, ponieważ kontroluje poziomy GABA poza synapsami i kształtuje długotrwałe, tło hamowania, które może subtelnie regulować aktywność mózgu. 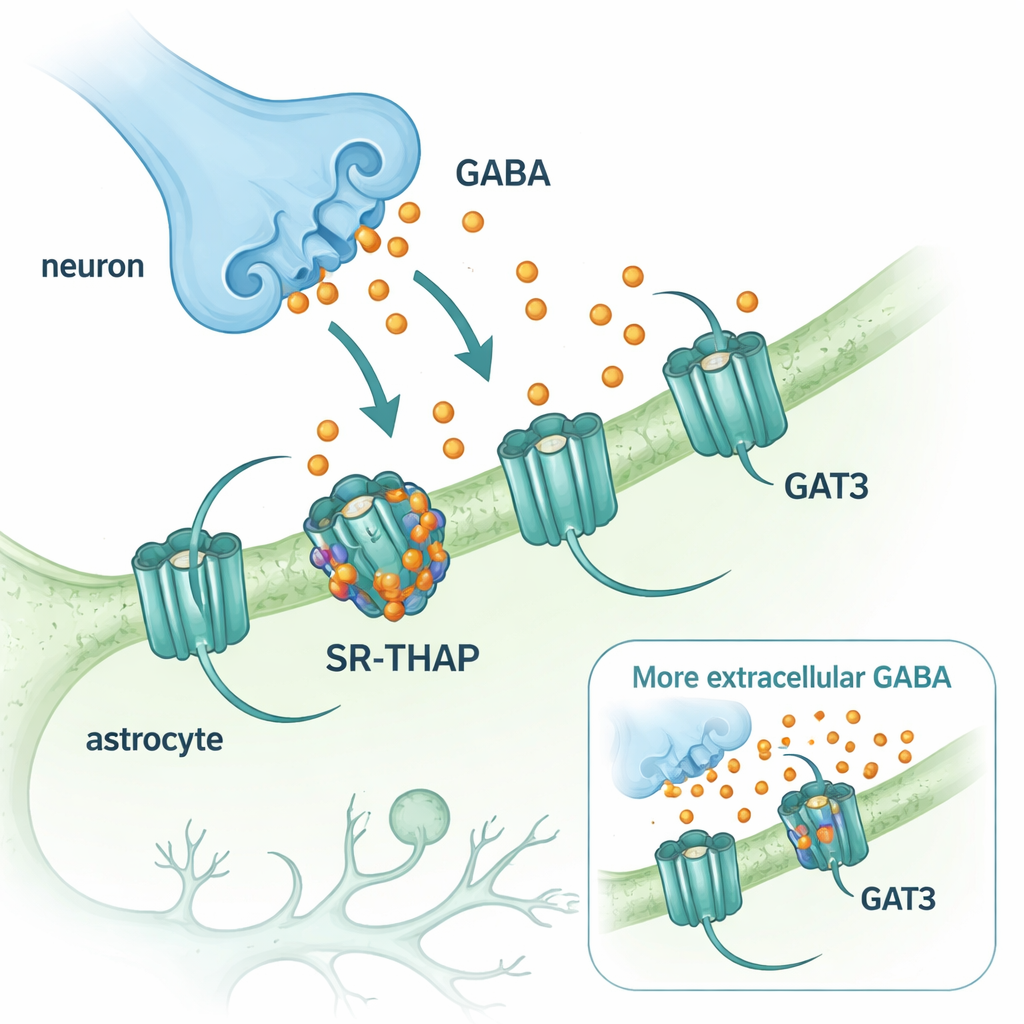
Projektowanie precyzyjniejszego molekularnego zamka
Próby zahamowania GAT3 utrudniał brak szczegółowych informacji strukturalnych. Wiele wcześniejszych związków powstawało metodą prób i błędów, często przez dodawanie masywnych modyfikacji znanym cząsteczkom podobnym do GABA. Jeden z lepiej znanych, (S)-SNAP-5114, okazał się chemicznie niestabilny i trudny w użyciu u żywych zwierząt. Bazując na stabilniejszym krewnym tej cząsteczki, autorzy opracowali SR-THAP, nową małą cząsteczkę zaprojektowaną tak, by lepiej dopasować się do GAT3 i być bardziej odporna na rozkład. Eksperymenty na hodowlach komórek ludzkich wykazały, że SR-THAP silnie blokuje GAT3 i robi to w sposób niekonkurencyjny: zamiast jedynie konkurować z GABA o zwykłe miejsce wiązania, zmienia sposób działania transportera, zmniejszając jego maksymalną zdolność transportową.
Oglądanie GAT3 z rozdzielczością bliską atomowej
Aby zrozumieć dokładnie, jak działa SR-THAP, zespół sięgnął po krioelektronową mikroskopię, technikę obrazowania błyskowo zamrożonych białek przy użyciu elektronów i rekonstrukcji ich trójwymiarowego kształtu. Rozwiązali trzy wersje ludzkiego GAT3: związane z SR-THAP, związane z GABA oraz w stanie bez substratu. Wszystkie trzy ukazują typową architekturę widzianą w pokrewnych transporterach neuroprzekaźników: 12 ściśle upakowanych helis przecinających błonę i tworzących centralną drogę dla GABA oraz towarzyszących mu jonów sodu i chloru. W strukturze związanej z GABA transporter znajduje się w stanie „zamkniętym od zewnątrz i wewnątrz” (inward-occluded) — GABA i jon sodu są zatrzaśnięte w środku, odizolowane zarówno od zewnątrz, jak i od wnętrza. Kluczowe aromatyczne aminokwasowe reszty tworzą wyspecjalizowaną interakcję z grupą aminową GABA, co pomaga wyjaśnić, jak GAT3 rozpoznaje swój substrat.
Jak SR-THAP klinuje transporter w pozycji otwartej
W wyraźnym kontraście, struktura związana z SR-THAP ukazuje GAT3 w stanie „otwartym do wnętrza” (inward-open), z wewnętrzną stroną białka szeroko otwartą w kierunku wnętrza komórki. SR-THAP siedzi głęboko w tej wewnętrznej jamie, zaklinowany między kilkoma helisami, które normalnie poruszają się podczas cyklu transportu. Zajmuje trzy małe kieszenie o odmiennym charakterze chemicznym, nawiązując sieć wiązań wodorowych i hydrofobowych kontaktów. To położenie skutecznie blokuje transporter, uniemożliwiając GABA i jonów ukończenie ich podróży. Autorzy pokazują, że kilka specyficznych aminokwasów wyściełających tę jamę różni się między GAT3 a jego bliskimi krewnymi; zamiana jednego z tych reszt zmienia zarówno aktywność transportową, jak i skuteczność SR-THAP, co pomaga wyjaśnić, dlaczego inhibitor jest znacznie bardziej selektywny względem GAT3 niż GAT1 czy pokrewne transportery. 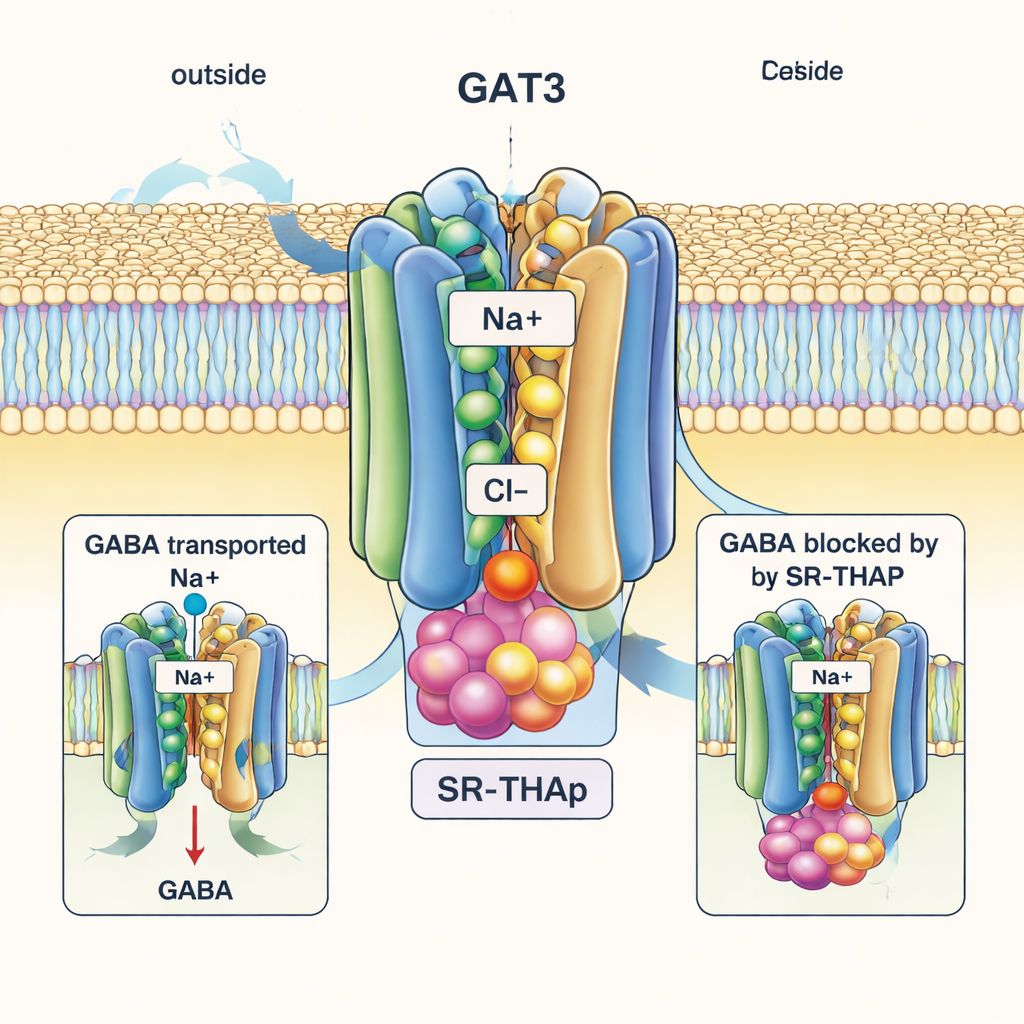
Otwieranie drzwi do nowych leków na padaczkę i poprawę zdrowia mózgu
Wspólnie te struktury ukazują, jak GAT3 przechodzi między różnymi kształtami, by przemieszczać GABA, oraz jak SR-THAP wykorzystuje mniej zachowaną wewnętrzną kieszeń, by zatrzymać ten cykl. Dla osób nietechnicznych kluczowy wniosek jest taki, że badanie dostarcza szczegółowego molekularnego planu wyłączania GAT3 w sposób wysoce selektywny. Takie związki mogłyby podnieść poziomy uspokajającego GABA w sposób bardziej precyzyjny niż istniejące leki, co potencjalnie prowadzi do nowych terapii lub narzędzi badawczych w przypadku padaczki, rekonwalescencji po udarze, choroby Alzheimera i innych schorzeń, w których zaburzone jest hamujące przekazywanie sygnałów.
Cytowanie: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
Słowa kluczowe: Transporter GABA, GAT3, padaczka, cryo-EM, hamowanie neuroprzekaźnika