Clear Sky Science · pl
Mechanizm stochastyczny napędza szybką translokację substratu w maszynie AAA+ ClpB
Jak komórkowe maszyny utrzymują ruch białek
W każdej komórce maleńkie maszyny molekularne nieustannie ciągną, popychają i przebudowują białka, aby zapobiegać ich zlepianiu się i naprawiać uszkodzenia. Jedną z takich maszyn jest ClpB, który pomaga ratować poplątane białka — zadanie niezbędne do przeżycia komórki w warunkach stresu. To badanie stawia proste, lecz dogłębne pytanie: jak ClpB przekształca chemiczne paliwo ATP w pracę mechaniczną polegającą na przeciągnięciu łańcucha białkowego przez centralny kanał i czy odbywa się to w uporządkowanych, krokowych ruchach, czy w bardziej przypadkowy, dyfuzyjny sposób?
Ring ratunkowy białka w akcji
ClpB należy do dużej rodziny enzymów zwanych maszynami AAA+, które składają się w struktury pierścieniowe z centralnym tunelem. Wiele z nich zostało odwzorowanych z dużą szczegółowością za pomocą kriomikroskopii elektronowej, co doprowadziło do popularnego modelu „ręka po ręce”: każde zhydrolizowane ATP miałoby napędzać mały, precyzyjny krok, jak zespół osób ciągnących linę kolejno po sobie. Inne eksperymenty jednak sugerowały, że ClpB może przemieszczać białka znacznie szybciej niż wynikałoby to z jego wolnego tempa hydrolizy ATP. Aby rozwiązać tę zagadkę, autorzy zaobserwowali pojedyncze cząsteczki ClpB w czasie rzeczywistym, gdy przeciągały elastyczne białko testowe, κ-casein, przez swój kanał.
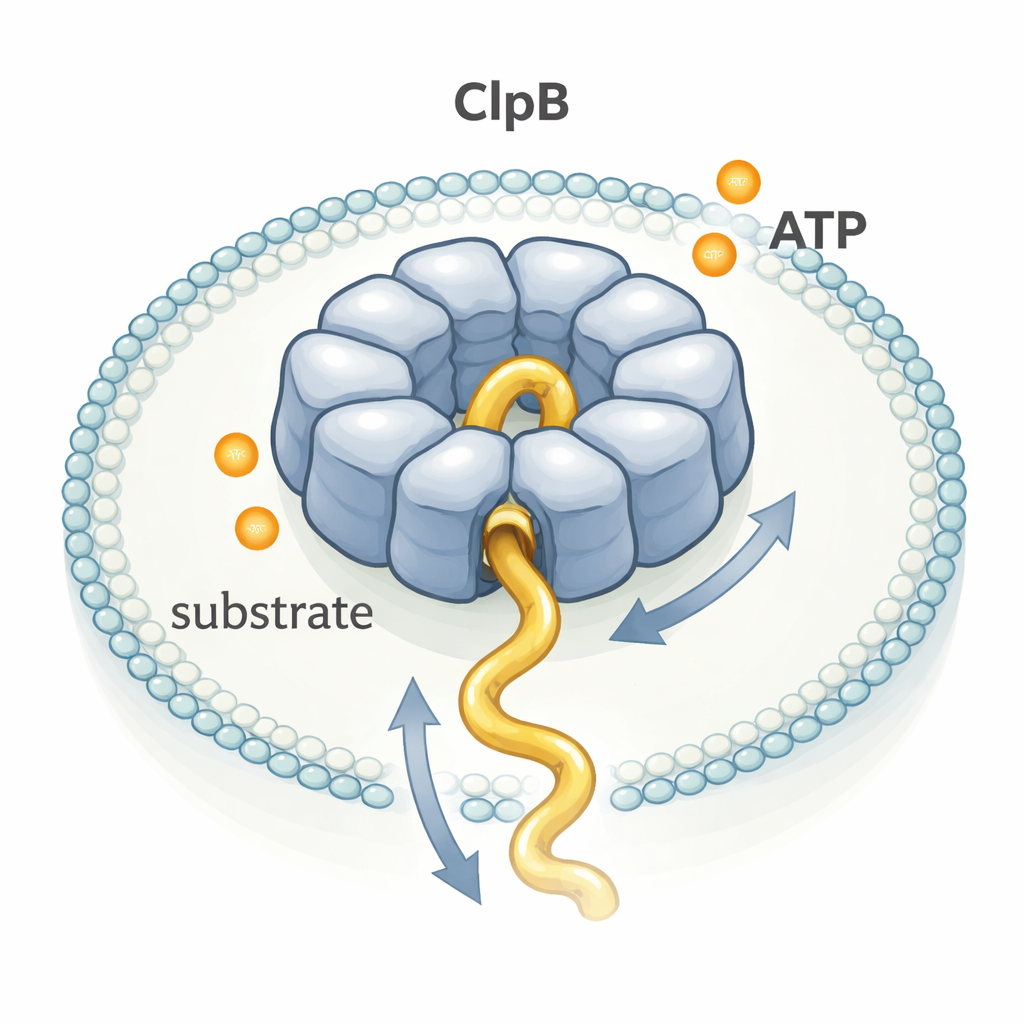
Obserwacja pojedynczej cząsteczki
Naukowcy uwięzili pojedyncze pierścienie ClpB i pojedyncze cząsteczki κ-casein wewnątrz malutkich pęcherzyków lipidowych przylegających do szklanej powierzchni. Przyłączyli barwniki fluorescencyjne w określonych miejscach na ClpB i na łańcuchu białkowym, a następnie użyli FRET pojedynczych cząsteczek — techniki raportującej zmiany odległości między barwnikami na skali nanometrów. Gdy κ-casein wsuwał się do kanału ClpB, barwniki zbliżały się, a FRET gwałtownie wzrastał w krótkim impulsie; gdy łańcuch opuszczał kanał, sygnał spadał. Mierząc czas trwania i wysokość tysięcy takich impulsów, mogli wywnioskować, jak szybko i na jaką odległość segmenty białka przewlekały się przez kanał.
Szybkie, słabo zasilane i niemal niezależne od temperatury
Niespodziewanie zdarzenia translokacji były niezwykle szybkie: znakowany segment κ-casein zwykle przebywał kilka nanometrów kanału w około 1–2 milisekund — w przybliżeniu tysiąc razy szybciej niż średni czas między zdarzeniami hydrolizy ATP w ClpB. Większość zdarzeń miała tak krótki czas trwania i podlegała szerokiemu rozkładowi potęgowemu, zamiast jednemu charakterystycznemu skalowi czasowemu. Zmiana temperatury z 10 do 32 °C ledwie spowolniła te ruchy, co sugeruje, że bariera energetyczna dla przemieszczania jest bardzo mała w porównaniu z klasycznymi „uderzeniowymi” motorami, takimi jak kinezyna. Podobnie obniżenie stężenia ATP silnie zmniejszało częstość występowania zdarzeń, ale prawie nie wpływało na długość trwania pojedynczego zdarzenia. Innymi słowy, ATP kontrolowało momenty, w których ClpB angażował się i jak często działał, bardziej niż prędkość poszczególnych wyskoków przewlekania.
Ruch tam i z powrotem z przewagą do przodu
Aby sprawdzić, czy łańcuchy poruszają się zawsze w jednym kierunku, zespół przeprowadził bardziej złożone eksperymenty trójkolorowego FRET, barwiąc oba końce kanału i substrat. Pozwoliło to rozróżnić, czy κ-casein wchodził od góry czy od dołu pierścienia oraz czy przeszedł cały kanał, czy się wycofał. Odkryli sześć odrębnych wzorców: kompletne przewleczenia do przodu i do tyłu, dłuższe „częściowe” wizyty, gdzie łańcuch próbował oba końce kanału przed opuszczeniem, oraz krótkie spotkania przy jednym tylko końcu. Około trzy czwarte zdarzeń kompletnych przebiegało w kierunku do przodu, ale znaczna część cofała się, co ujawniło, że ClpB dopuszcza dwukierunkową dyfuzję substratu z tylko umiarkowaną przewagą ruchu do przodu. Gdy ATP zastąpiono analogiem wolno hydrolizowanym, zdarzenia stały się rzadkie i znacznie wolniejsze, a preferencja do przodu praktycznie zniknęła.
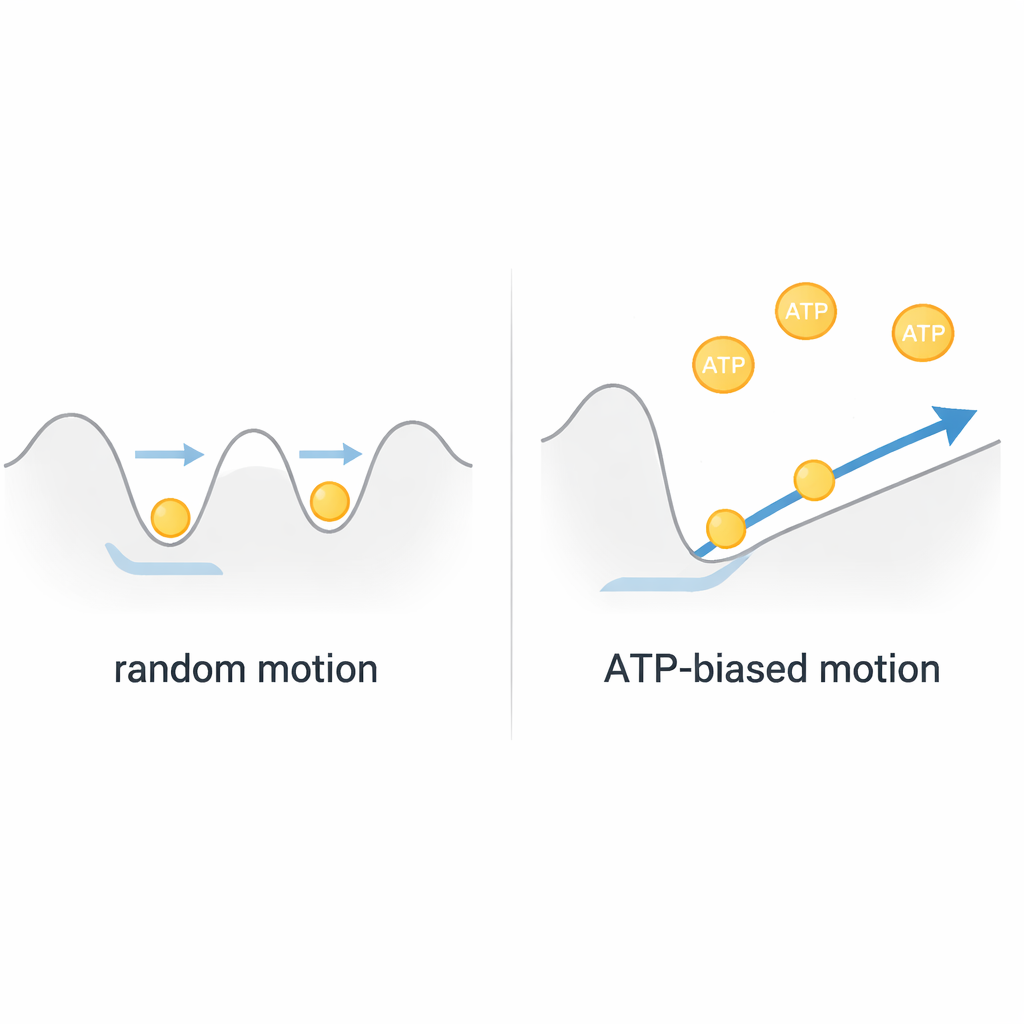
Silnik Browna, a nie prosty wyciąg
Składając te obserwacje razem, autorzy dochodzą do wniosku, że ClpB działa bardziej jak silnik Browna niż sztywny, paliwowy wyciąg. Łańcuch białkowy drga termicznie w płytkim pejzażu energetycznym wewnątrz kanału, poruszając się szybko tam i z powrotem. ATP nie napędza bezpośrednio dużych, dyskretnych pociągnięć; zamiast tego kształtuje ten pejzaż poprzez szybkie ruchy wewnętrznych „pętli kanałowych”, subtelnie faworyzując ruch w jednym kierunku. Ponieważ każde kompletne przewleczenie koreluje z jedynie około jednym lub dwoma zużytymi cząsteczkami ATP, ClpB osiąga wyjątkowo wydajny, szybki transport przez prostowanie losowego ruchu zamiast walki z nim. Taka wizja zmienia nasze myślenie o wielu maszynach AAA+, sugerując, że nanomotory biologiczne często wykorzystują przypadkowość zamiast jej eliminować.
Cytowanie: Casier, R., Levy, D., Riven, I. et al. A stochastic mechanism drives fast substrate translocation in the AAA+ machine ClpB. Nat Commun 17, 1773 (2026). https://doi.org/10.1038/s41467-026-68478-1
Słowa kluczowe: translokacja białka, maszyna AAA+, silnik Browna, czaperon molekularny, FRET pojedynczych cząsteczek