Clear Sky Science · pl
Identyfikacja termotolerancyjnych niekanonicznych PAM-ów dla niezawodnej, jednoprobówkowej detekcji CRISPR-Cas12a
Podkręcanie temperatury w testach DNA
Szybkie i dokładne testy wykrywające infekcje i zmiany genetyczne są kluczowe w medycynie, jednak współczesne testy DNA często wymagają złożonego sprzętu laboratoryjnego i mogą nie wychwycić rzadkich lub subtelnych celów. W tym badaniu pokazano, że prostsze podniesienie temperatury w teście opartym na CRISPR otwiera dostęp do wielu dodatkowych użytecznych „uchwytów” w DNA, dzięki czemu diagnostyka w jednej probówce staje się szybsza, bardziej czuła i zdolna odróżnić nawet pojedyncze zmiany liter w kodzie genetycznym. 
Dlaczego CRISPR potrzebuje „kodów pocztowych”
Narzędzia CRISPR, takie jak Cas12a, działają, lokalizując konkretne odcinki DNA przy pomocy krótkiego RNA pełniącego rolę wyszukiwarki. Mogą się jednak przyłączyć i zacząć działać tylko jeśli w pobliżu znajduje się czteroznakowy znacznik, zwany PAM, o odpowiedniej sekwencji — tradycyjnie wąskim zbiorem zaczynającym się od „TTT”. To jak konieczność posiadania numeru domu, zanim dostawca dostarczy list: gdy właściwy numer brak, przesyłka nie dociera. Wymóg PAM ogranicza więc miejsca, które CRISPR może zbadać, co stanowi poważne ograniczenie, gdy lekarze muszą wykryć konkretne mutacje, markery oporności na leki lub warianty wirusów, które nie leżą obok tych klasycznych znaczników.
Odkrywanie nowych „drzwi” w wyższej temperaturze
Naukowcy systematycznie przetestowali wszystkie 256 możliwych kombinacji czteroznakowych PAM, aby sprawdzić, jak dobrze napędzają one aktywność „kolateralnego” cięcia Cas12a — jego zdolność do rozcinania wielu pobliskich fragmentów DNA po znalezieniu celu, co stanowi podstawę sygnału diagnostycznego CRISPR. W normalnej temperaturze ciała (37 °C) tylko kilka niestandardowych PAM działało równie dobrze jak klasyczne. Jednak po podniesieniu temperatury reakcji do około 45 °C zaszło coś uderzającego: 82 różne niekanoniczne PAMy nagle wywołały silną aktywność przecinającą sygnał, dorównując znanym znacznikom. Zespół przypuszcza, że dodatkowe ciepło rozluźnia lokalną strukturę DNA i czyni kompleks Cas12a bardziej elastycznym, obniżając barierę rozpoznawania wcześniej „słabych” PAM-ów.
Mocny sygnał, delikatne traktowanie matrycy
Cas12a ma dwa tryby cięcia. W trybie „cis” tnie ono konkretne DNA, które ma rozpoznać; w trybie „trans”, po aktywacji, szybko degraduje dowolne pobliskie nici niosące sygnał, co daje odczyt testu. Badacze odkryli, że w wyższych temperaturach niekanoniczne PAMy wywoływały bardzo silne cięcie trans — idealne dla jasnego i szybkiego sygnału — przy jednoczesnym stosunkowo słabym cięciu cis głównej matrycy DNA. Ta kombinacja jest wymarzona dla testów jednoprobówkowych, gdzie DNA musi najpierw zostać amplifikowane bez jego zniszczenia. Wykazali także, że w cieplejszych warunkach Cas12a staje się znacznie bardziej wybredny względem niezgodności między RNA przewodnika a celem: nawet pojedyncza błędna litera może wyłączyć sygnał, szczególnie przy użyciu niekanonicznych PAM-ów. 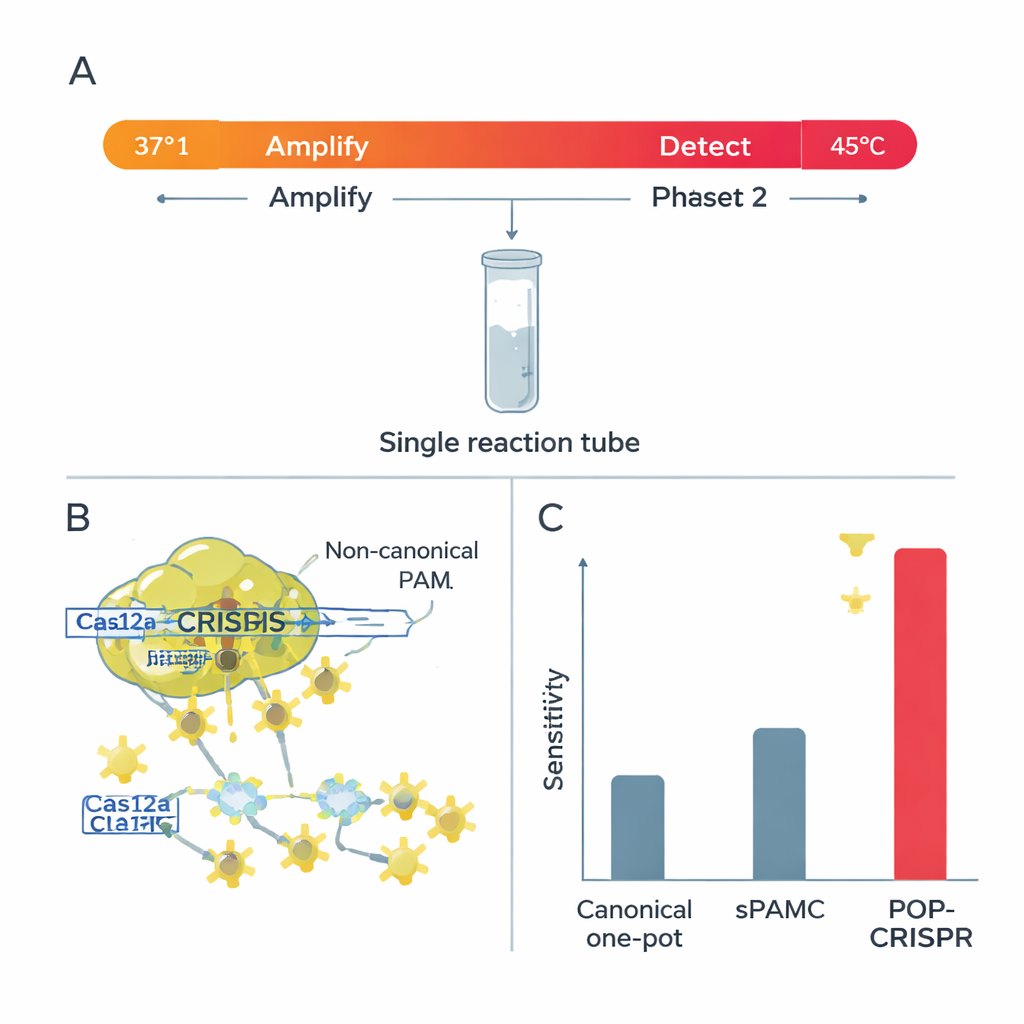
Sprytniejszy test w jednej probówce: POP-CRISPR
Wykorzystując te wnioski, zespół opracował POP-CRISPR, jednoprobówkowy test „poikilotermiczny” (o zmiennej temperaturze). Reakcja zaczyna się w okolicach 37 °C, gdzie izotermiczna metoda amplifikacji cicho rozmnaża każdy docelowy DNA lub RNA, podczas gdy Cas12a jest stosunkowo nieaktywny. Po około 10 minutach mieszaninę podgrzewa się do około 45 °C — optymalnego punktu, w którym Cas12a, kierowane teraz do niekanonicznych miejsc PAM, włącza silne cięcie trans i generuje intensywny sygnał fluorescencyjny. Ten prosty program dwustopniowy zwiększył czułość detekcji w przybliżeniu dziesięciokrotnie w porównaniu z wcześniejszymi jednoprobówkowymi metodami CRISPR, które także wykorzystywały słabsze PAMy, i wyraźnie przewyższał klasyczne formaty jednoprobówkowe o kanonicznych PAM-ach.
Z laboratorium do łóżka pacjenta w kilkanaście minut
System POP-CRISPR przetestowano na rzeczywistych próbkach klinicznych. Wykrywał czułe wirusa brodawczaka ludzkiego (HPV-16) w wymazach pochwy oraz Mycoplasma pneumoniae w wymazach z dróg oddechowych, w tym bardzo niskie przypadki „strefy szarej”, które stanowią wyzwanie dla standardowych metod. Co ważne, POP-CRISPR potrafił odróżnić szczepy Mycoplasma oporne na leki niosące pojedynczą zmianę literową w genie rybosomalnym, mimo że w pobliżu tej mutacji nie znajdował się klasyczny PAM — zadanie, które paraliżuje wiele istniejących testów Cas12a. Aby uczynić podejście przydatnym w terenie, autorzy połączyli szybki, dwuminutowy etap lizowania ciepłem i Chelexem (unika się pełnej ekstrakcji DNA) z przenośnym czytnikiem fluorescencji wielkości dłoni sterowanym smartfonem. Razem ten proces może przekształcić surowy wymaz w cyfrowy wynik tak/nie w około 20 minut.
Co to oznacza dla codziennych testów
Podnosząc temperaturę reakcji i wykorzystując znacznie szerszy zestaw PAM-owych „drzwi”, ta praca przekształca Cas12a w bardziej elastyczny i precyzyjny czujnik. POP-CRISPR zapewnia szybszą, bardziej czułą i bardziej specyficzną detekcję kwasów nukleinowych w pojedynczej zamkniętej probówce, a jednocześnie poszerza zakres miejsc genetycznych, które można celować — w tym mutacje pojedynczych nukleotydów związane z opornością na leki lub rakiem. Dla pacjentów może to przełożyć się na szybszą diagnostykę na miejscu i lepiej dopasowane leczenie; dla naukowców i twórców testów daje potężny nowy sposób projektowania diagnostyki CRISPR, która jest zarówno bardziej odporna, jak i bardziej dyskryminująca.
Cytowanie: Tian, T., Zhang, T., Zhang, W. et al. Identification of thermotolerant non-canonical PAMs for robust one-pot CRISPR-Cas12a detection. Nat Commun 17, 1771 (2026). https://doi.org/10.1038/s41467-026-68476-3
Słowa kluczowe: Diagnostyka CRISPR, Cas12a, Miejsca PAM, testy przyłóżkowe, detekcja kwasów nukleinowych