Clear Sky Science · pl
Mechanizmy strukturalne hamowania i aktywacji kanału potasowego SK2 aktywowanego Ca2+ o małej przewodności u człowieka
Dlaczego drobne kanały potasowe mają znaczenie
Każda myśl i każdy uderzenie serca zależą od sygnałów elektrycznych w komórkach. Te sygnały kształtują mikroskopijne pory, zwane kanałami jonowymi, które pozwalają na przepływ naładowanych atomów. Jedna z rodzin — kanały potasowe o małej przewodności aktywowane wapniem (kanały SK) — pomaga kontrolować, jak neurony wyładowują się i jak serce utrzymuje rytm. Artykuł ten ujawnia, w detalach atomowych, jak różne leki i jad pszczeli mogą albo zamykać, albo wzmacniać ważnego przedstawiciela tej rodziny, kanał SK2 u człowieka — informacje, które mogą naprowadzić na nowe terapie schorzeń od migotania przedsionków po drżenia i zaburzenia pamięci.
Jak kanały SK2 działają jak hamulec komórkowy
Kanały SK2 znajdują się w błonie komórkowej i pełnią rolę drobnych hamulców aktywności elektrycznej. Gdy wewnątrz komórki podczas sygnału elektrycznego krótkotrwale wzrasta stężenie jonów wapnia, białko pomocnicze zwane kalmoduliną wyczuwa ten wzrost. Kalmodulina jest przyczepiona od strony wewnętrznej do SK2 i po związaniu wapnia pociąga za część kanału niczym linkę, otwierając bramę, przez którą wypływają jony potasu. Ten wypływ pomaga uciszyć komórkę po wyładowaniu, kształtując częstotliwość przekazywania sygnałów przez neurony i stabilność rytmu serca. Ponieważ kanały SK1–3 występują szeroko w mózgu i sercu, a SK2 jest szczególnie ważnym podtypem, poznanie dokładnego mechanizmu ich otwierania, zamykania i reakcji na leki jest kluczowe dla projektowania precyzyjnych terapii.
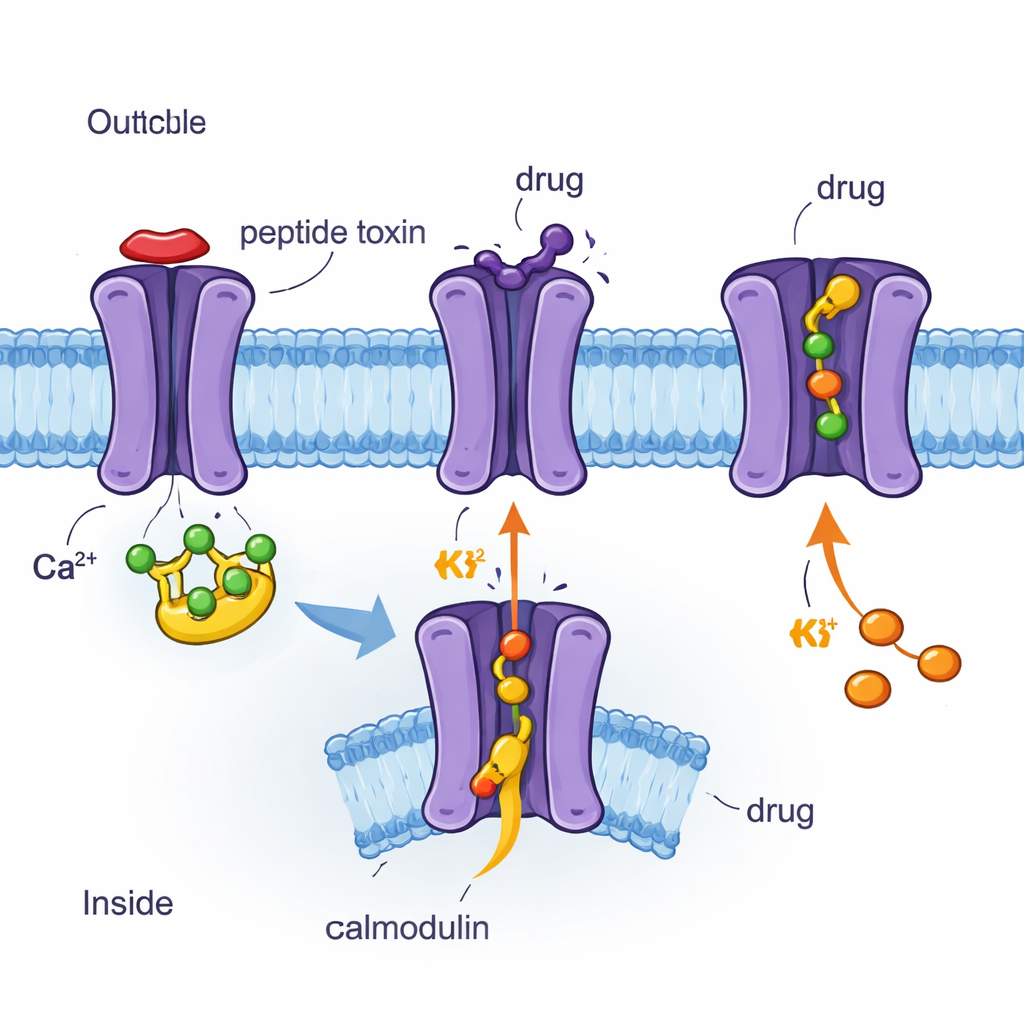
Użycie cryo‑EM do oglądania kanałów i leków atom po atomie
Autorzy zastosowali kriomikroskopię elektronową (cryo‑EM), technikę obrazowania zamrożonych białek zbliżonych do rozdzielczości atomowej, aby określić cztery struktury trójwymiarowe ludzkiego kanału SK2 związane z kalmoduliną i różnymi cząsteczkami. Były to peptyd jadu pszczół apamina, syntetyczny bloker UCL1684, kliniczny inhibitor AP30663 oraz kliniczny aktywator CAD‑1883. Wszystkie cztery struktury pokazują SK2 jako czteroczęściowy zespół przechodzący przez błonę, z kalmoduliną przyczepioną od środka. Porównanie tych migawki ujawniło, które części kanału są sztywne, które elastyczne, i jak porusza się kalmodulina, gdy kanał jest w stanie zamkniętym lub otwartym. Badacze połączyli też te obrazy z pomiarami elektrycznymi w komórkach, testując, jak konkretne zmiany aminokwasowe wpływają na reakcję kanału na każdy związek.
Jad pszczoły i związek laboratoryjny zatyka zewnętrzne ujście
Apamina, mały peptyd z jadu pszczelego, od dawna jest znana jako wyjątkowo silny i selektywny bloker SK2 używany w badaniach. Nowe struktury pokazują, że apamina wiąże się jak korek na zewnętrznym ujściu poru SK2. Osadza się w miseczkowatym przedsionku utworzonym przez krótki pętlę między dwiema helisami (łącznik S3–S4), która jest dobrze uporządkowana w SK2, lecz luźna w spokrewnionym kanale SK4, co tłumaczy, dlaczego SK4 jest niewrażliwy na apaminę. Kluczowe dodatnio naładowane reszty apaminy sięgają pomiędzy cztery aromatyczne łańcuchy boczne kanału, tworząc silne oddziaływania elektrostatyczne i typu stacking, które całkowicie uszczelniają drogę potasu. UCL1684, syntetyczny związek bis‑chinoliniowy, zajmuje w zasadzie tę samą zewnętrzną kieszeń i również blokuje ujście jonów, ale jego mniejszy rozmiar pozwala mu siedzieć głębiej, naśladując pozycję krytycznych dodatnich ładunków apaminy. Mutacje reszt kanału kształtujących ten przedsionek znacząco zmniejszają wrażliwość na apaminę, a w mniejszym stopniu na UCL1684, potwierdzając, że ukształtowana zewnętrzna pętla jest głównym elementem determinującym działanie toksyny i leku.
Centralna zatyczka i wewnętrzny klin regulują aktywność
W przeciwieństwie do tego, kandydat kliniczny AP30663 wiąże się wewnątrz centralnej jamy SK2, tuż poniżej filtra selektywności, który wybiera jony potasu. Działa tam jak fizyczna zatyczka, klinując się między określonymi łańcuchami bocznymi wyściełającymi por. Zmiany tych reszt wyściełających osłabiają zdolność AP30663 do hamowania SK2, a porównania sekwencyjne wyjaśniają, dlaczego jego bliskie analogi potrafią rozróżniać SK1–3 od SK4. CAD‑1883, modulator dodatni opracowany dla zaburzeń ruchowych, wykorzystuje jeszcze inną strategię. Wsuwając się do kieszeni na styku między N‑płatem kalmoduliny a krótkim łącznikiem (S4–S5), który sprzęga ruch kalmoduliny z bramką kanału, wzmacnia kontakty w tej kieszeni. CAD‑1883 skutecznie skleja kalmodulinę i SK2 w konfiguracji, która pociąga wewnętrzną bramkę otwartą i poszerza por. Porównania strukturalne pokazują, że stan związany z CAD‑1883 przypomina w pełni otwarty kanał, chociaż filtr selektywności może przyjąć formę inaktywowaną po przedłużonym otwarciu.
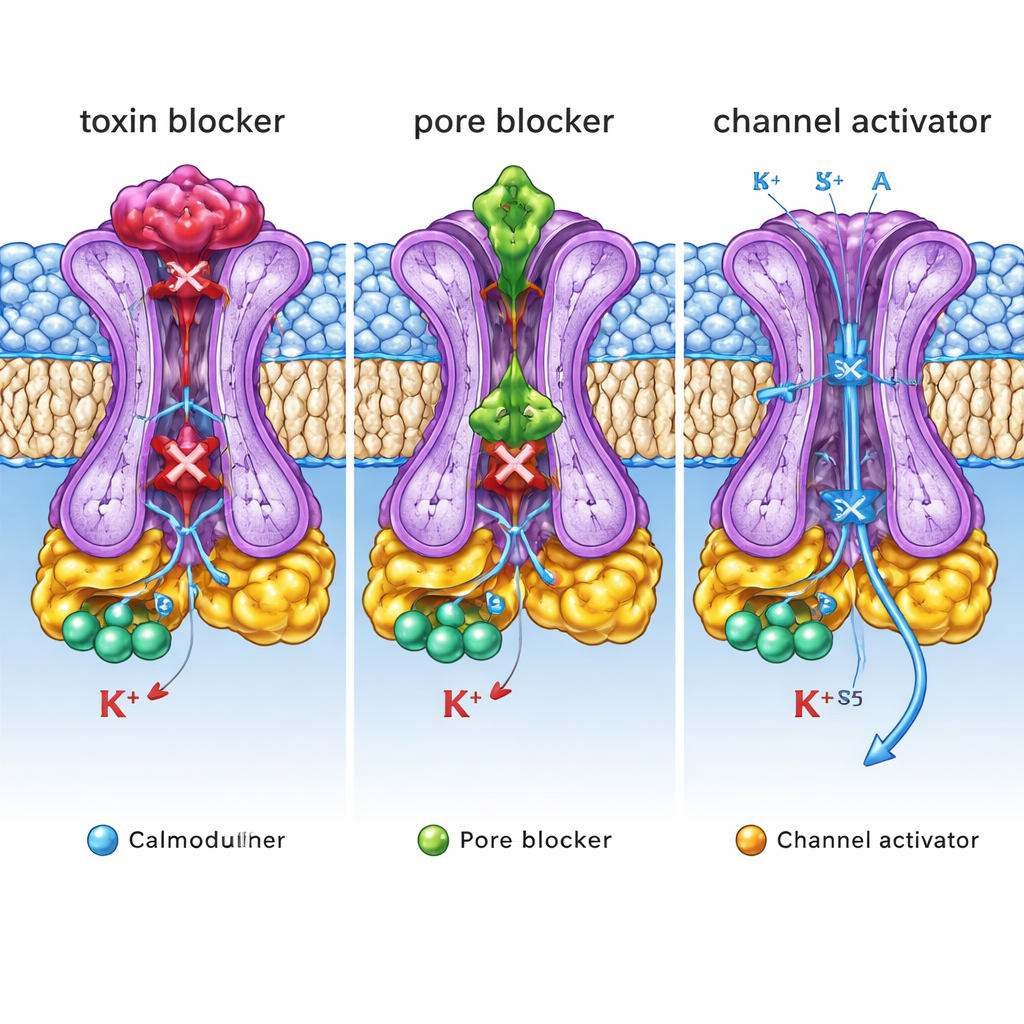
Co te strukturalne plany znaczą dla medycyny
W sumie te struktury ujawniają trzy odrębne „pokrętła kontrolne” na pojedynczym kanale SK2: zewnętrzną pokrywę, gdzie osiadają toksyny i niektóre blokery; wewnętrzną jamę poru, gdzie inni inhibitory zatykają przepływ; oraz boczną kieszeń, gdzie aktywatory stabilizują otwarcie. Dla osoby niezaznajomionej ze specjalistycznym żargonem kluczowy przekaz jest taki, że ten sam kanał jonowy można wyregulować w górę lub w dół za pomocą leków chwytających zupełnie inne strukturalne uchwyty. Mapując te uchwyty z precyzją atomową i wiążąc je z efektami funkcjonalnymi, praca ta dostarcza szczegółowego planu do projektowania molekuł następnej generacji, które selektywnie stłumią lub wzmocnią aktywność SK2. Takie szyte na miarę leki mogłyby pewnego dnia pomóc normalizować nieprawidłowe rytmy mózgowe, łagodzić drżenia lub korygować nieregularne bicia serca przy mniejszych działaniach niepożądanych.
Cytowanie: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
Słowa kluczowe: kanały potasowe SK2, kanały aktywowane wapniem, struktury cryo‑EM, modulatory kanałów jonowych, migotanie przedsionków i drżenie