Clear Sky Science · pl
Zaburzona migracja i podziały komórek macierzystych w dystrofii mięśniowej Duchenne’a ujawnione dzięki obrazowaniu na żywo
Dlaczego ta historia o mięśniach ma znaczenie
Dystrofia mięśniowa Duchenne’a (DMD) to śmiertelna choroba dziecięca, która stopniowo niszczy mięśnie. Przez dekady większość badań skupiała się na dużych włóknach mięśniowych, które ulegają rozpadowi w DMD. Niniejsze badanie pokazuje jednak, że drugi, cichszy uczestnik także ma problemy: własne komórki macierzyste mięśnia, które normalnie naprawiają uszkodzenia. Obserwując te komórki na żywo w mięśniach myszy i na pojedynczych włóknach, autorzy ujawniają, w jaki sposób komórki macierzyste w DMD gubią orientację, co daje nowe pomysły na terapie mogące poprawić zdolność mięśni do regeneracji.
Wbudowana załoga naprawcza mięśnia
Każde włókno mięśnia szkieletowego otoczone jest kilkoma rezydującymi komórkami macierzystymi, zwanymi satelitarnymi komórkami mięśniowymi. W zdrowym mięśniu te komórki przez większość czasu pozostają uśpione. Gdy dojdzie do urazu, budzą się, dzielą i albo wytwarzają nowe komórki macierzyste uzupełniające rezerwę, albo produkują wyspecjalizowane komórki, które łączą się z uszkodzonymi włóknami. Ten delikatny balans między samoodnową a różnicowaniem utrzymuje tkankę mięśniową w dobrej kondycji przez całe życie. W DMD jednak włókna mięśniowe wielokrotnie pękają z powodu braku dystrofiny, kluczowego białka strukturalnego, co rodzi pytanie, czy sama załoga naprawcza nie zostaje wyczerpana lub zdezorientowana.
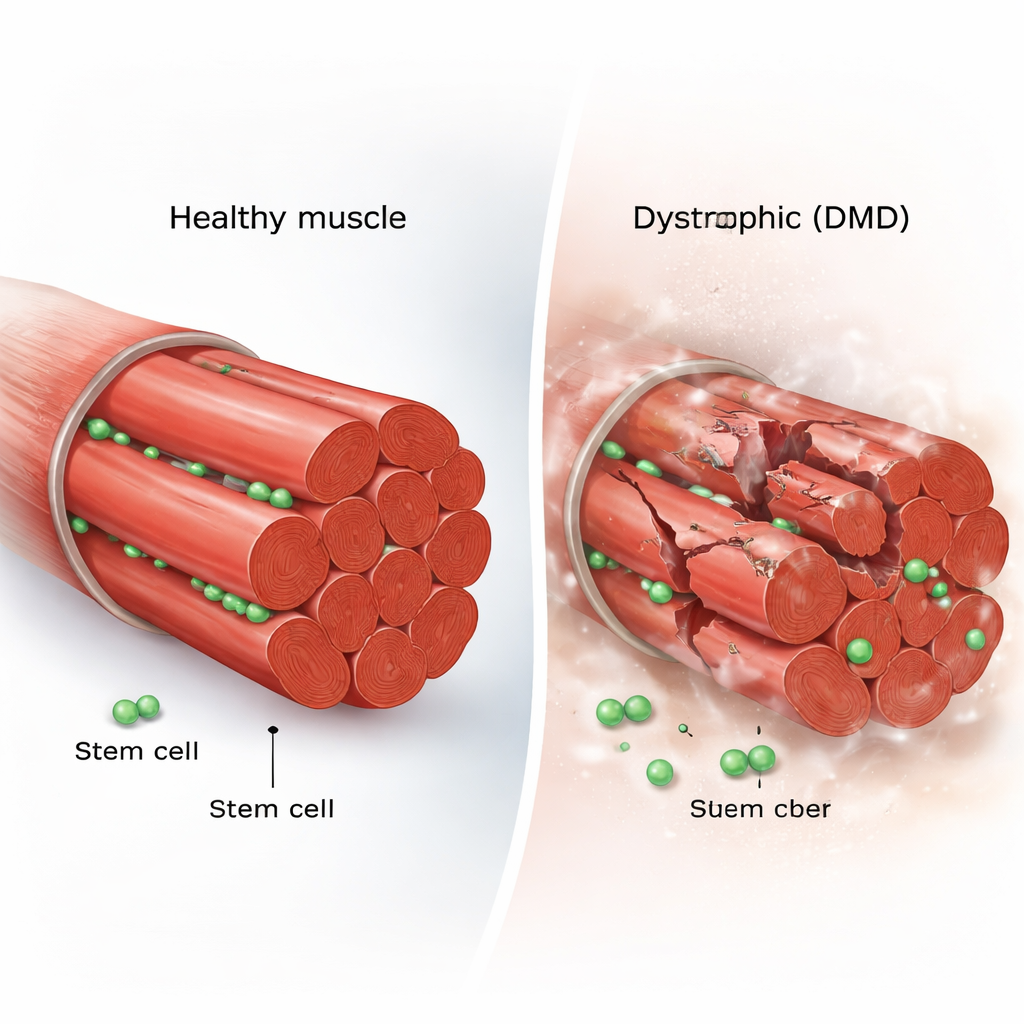
Filmowanie komórek macierzystych w akcji
Aby odpowiedzieć na to pytanie, badacze użyli myszy mdx, standardowego modelu DMD, i genetycznie oznaczyli ich komórki macierzyste mięśni tak, by świeciły pod mikroskopem. Następnie przeprowadzili obrazowanie in vivo (intravital imaging), technikę pozwalającą filmować żywe komórki w anestetyzowanym zwierzęciu przez wiele godzin. Opracowali też niestandardowy system „mikro studzienek” do utrzymywania pojedynczych włókien mięśniowych w hodowli, śledząc każdy podział i ruch komórki. To podwójne podejście umożliwiło śledzenie pojedynczych komórek od spokojnego spoczynku, przez kolejne podziały, migracje, aż po fuzję z nowym mięśniem, rejestrując zachowania, które statyczne migawki łatwo mogłyby przeoczyć.
Gdy komórki naprawcze spieszą się i potykają
W obrębie kontuzjowanych, zdrowych mięśni komórki mięśniogenezy pochodzące z komórek macierzystych wydłużały się i pełzały wzdłuż włókien po stosunkowo prostych, ukierunkowanych torach, dzieląc się i rozprzestrzeniając wydajnie. W przeciwieństwie do tego komórki dystroficzne (mdx) często stawały się okrągłe i ociężałe. Poruszały się wolniej i z mniejszą kierunkowością, a znaczna ich część pozostawała prawie nieruchoma. Zespół stwierdził też, że komórki mdx fuzjowały z nowymi włóknami wcześniej niż normalnie, a wiele komórek potomnych migrowało razem zamiast się rozdzielać po podziale. Ogólnie mięśnie mdx wykazywały oznaki „przedwczesnego różnicowania”: komórki macierzyste zbyt szybko przechodziły w komórki mięśniowe i tworzyły włókna zamiast utrzymywać solidną pulę rezerwową do dalszej naprawy.
Niezrównoważone podziały komórek i zdezorientowane otoczenie
Na izolowanych włóknach badacze mogli sklasyfikować sposoby podziału każdej komórki macierzystej. W zdrowych mięśniach większość podziałów była symetryczna, ale zrównoważona — wiele dawało dwie proliferujące komórki potomne, które mogły dalej powiększać pulę naprawczą, a mniej produkowało dwie komórki terminalnie różnicujące się. Podziały asymetryczne, gdzie jedna komórka potomna pozostawała komórką macierzystą, a druga przejmowała rolę naprawczą, były stosunkowo rzadkie, ale występowały. W mięśniach mdx wzorzec przesunął się drastycznie: podziały symetryczne były skierowane w stronę produkcji dwóch komórek różnicujących się, a znacznie rzadziej powstawały podziały generujące dwie odnawiające się komórki. Eksperymenty z przeszczepianiem krzyżowym, gdzie zdrowe komórki macierzyste umieszczano na dystroficznych włóknach i odwrotnie, wykazały, że defekty migracji są w dużej mierze dyktowane przez uszkodzone środowisko włókna, podczas gdy nadmierne różnicowanie komórek mdx wynika z cech samych tych komórek, ukształtowanych częściowo przez ich historię zapalną.
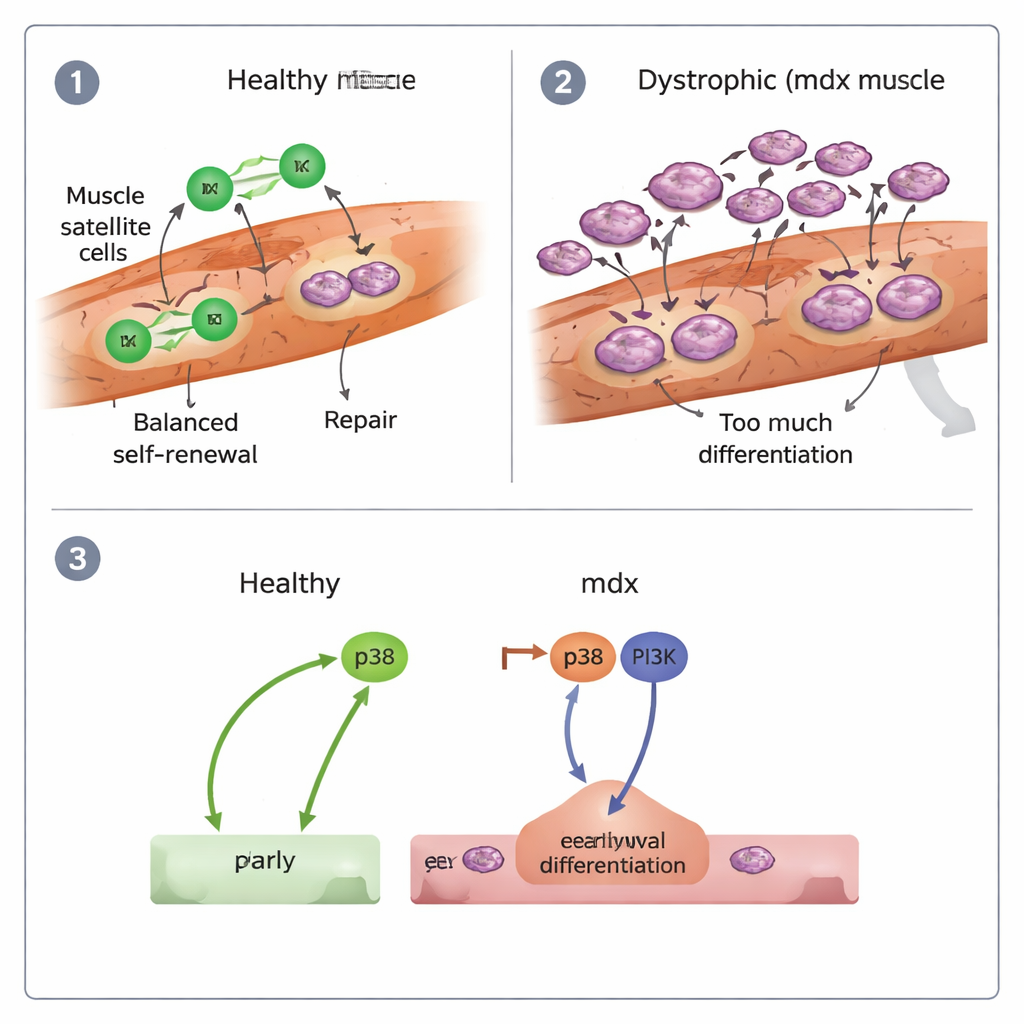
Źle ustawione sygnały i co to oznacza dla terapii
Autorzy zbadali także molekularne przełączniki popychające komórki macierzyste do różnicowania. Skupili się na dwóch szlakach sygnałowych, znanych jako p38 i PI3K. W zdrowych komórkach blokada p38 silnie ograniczała różnicowanie, podczas gdy hamowanie PI3K miało niewielki efekt. W komórkach mdx jednak oba szlaki trzeba było zablokować jednocześnie, aby powstrzymać nadmierny pośpiech w kierunku specjalizacji, a nawet wtedy ich zdolność do utrzymania proliferacji pozostawała słaba. Sugeruje to, że komórki macierzyste w DMD są popychane do „wczesnego wypalenia” przez skumulowaną aktywność p38 i PI3K, co przyczynia się do regeneracji, która zaczyna się szybko, ale nie może być utrzymana.
Nowe spojrzenie na Duchenne’a: także choroba komórek macierzystych
Dla czytelnika niebędącego specjalistą kluczowy przekaz jest taki, że DMD to nie tylko problem kruchych włókien mięśniowych; to także problem systemu naprawczego przeznaczonego do ich naprawy. W mięśniach dystroficznych komórki macierzyste poruszają się mniej efektywnie, dzielą się w sposób wyczerpujący rezerwę i nieprawidłowo reagują na kluczowe sygnały wzrostowe. Dzięki rozróżnieniu, które aspekty wynikają z uszkodzonego środowiska mięśnia, a które są wpisane w zmieniony stan samych komórek macierzystych, ta praca sugeruje nowe strategie: terapie łagodzące sygnalizację p38 i PI3K, przywracające zrównoważone podziały komórek lub poprawiające lokalną niszę mogłyby skuteczniej odbudować mięsień i wydłużyć korzyści płynące z terapii genowych lub komórkowych dla osób żyjących z dystrofią mięśniową Duchenne’a.
Cytowanie: Sarde, L., Letort, G., Varet, H. et al. Impaired stem cell migration and divisions in Duchenne muscular dystrophy revealed by live imaging. Nat Commun 17, 1769 (2026). https://doi.org/10.1038/s41467-026-68474-5
Słowa kluczowe: dystrofia mięśniowa Duchenne’a, komórki macierzyste mięśni, migracja komórek, podział komórek macierzystych, medycyna regeneracyjna