Clear Sky Science · pl
Systemy do dzielenia edytorów zasad oparte na heterodimerach koiled‑coil umożliwiają elastyczne i odporne substytucje nukleotydów
Naprawianie DNA z mniejszą liczbą efektów ubocznych
Wiele chorób wynika z drobnych literówek w naszym DNA — pojedynczych błędów, które mogą mieć ciężkie, zagrażające życiu konsekwencje. Naukowcy dysponują potężnymi narzędziami, zwanymi edytorami zasad, które potrafią poprawiać takie literówki bez cięcia DNA, lecz są one duże i trudne do bezpiecznego dostarczenia do organizmu. W artykule przedstawiono nowy sposób rozdzielania edytorów zasad na mniejsze, inteligentniejsze części, które nadal działają tak samo dobrze — a czasem lepiej — niż pełnowymiarowe wersje, otwierając nowe drogi do leczenia chorób genetycznych w wątrobie, mięśniach i poza nimi.
Dlaczego rozmiar stanowi problem dla narzędzi naprawy genów
Edytory zasad łączą elementy systemu CRISPR z enzymami zdolnymi do podmiany jednej litery DNA na inną, na przykład zmieniając A na G lub C na T. Te precyzyjne podmiany są obiecujące w leczeniu schorzeń takich jak wysoki poziom cholesterolu czy dystrofia mięśniowa. Jednak wiodący nośnik terapii genowej, wirus adeno‑zależny (AAV), może przenosić tylko około 4,7 tysiąca nukleotydów, podczas gdy standardowe edytory zasad są większe. Wcześniejsze prace próbowały dzielić te edytory z użyciem specjalnych białkowych „nożyczek” zwanych inteinami lub poprzez zmniejszanie ich za pomocą zminiaturyzowanych enzymów, ale podejścia te często obniżały wydajność, zwiększały złożoność projektu lub ograniczały miejsca w genomie, w których narzędzia mogły działać.
Użycie molekularnego rzepu do odbudowy edytora
Aby rozwiązać ten problem, badacze zaprojektowali „podzielony” edytor zasad połączony za pomocą małych białkowych suwaków znanych jako heterodimery coiled‑coil — coś jak molekularny rzep. Rozdzielili edytor na dwie części: jedną z nikkazą Cas9 kierującą do DNA, a drugą z enzymem edytującym. Krótkie peptydy coiled‑coil na każdej połowie rozpoznają się wzajemnie i łączą, gdy obie części dotrą do tego samego odcinka DNA. Powstały w ten sposób coiled‑coil edytory zasad (CC‑BE), w tym wersje edytujące C (CC‑CBE), A (CC‑ABE) oraz bardziej złożone warianty umożliwiające różne typy podmian. 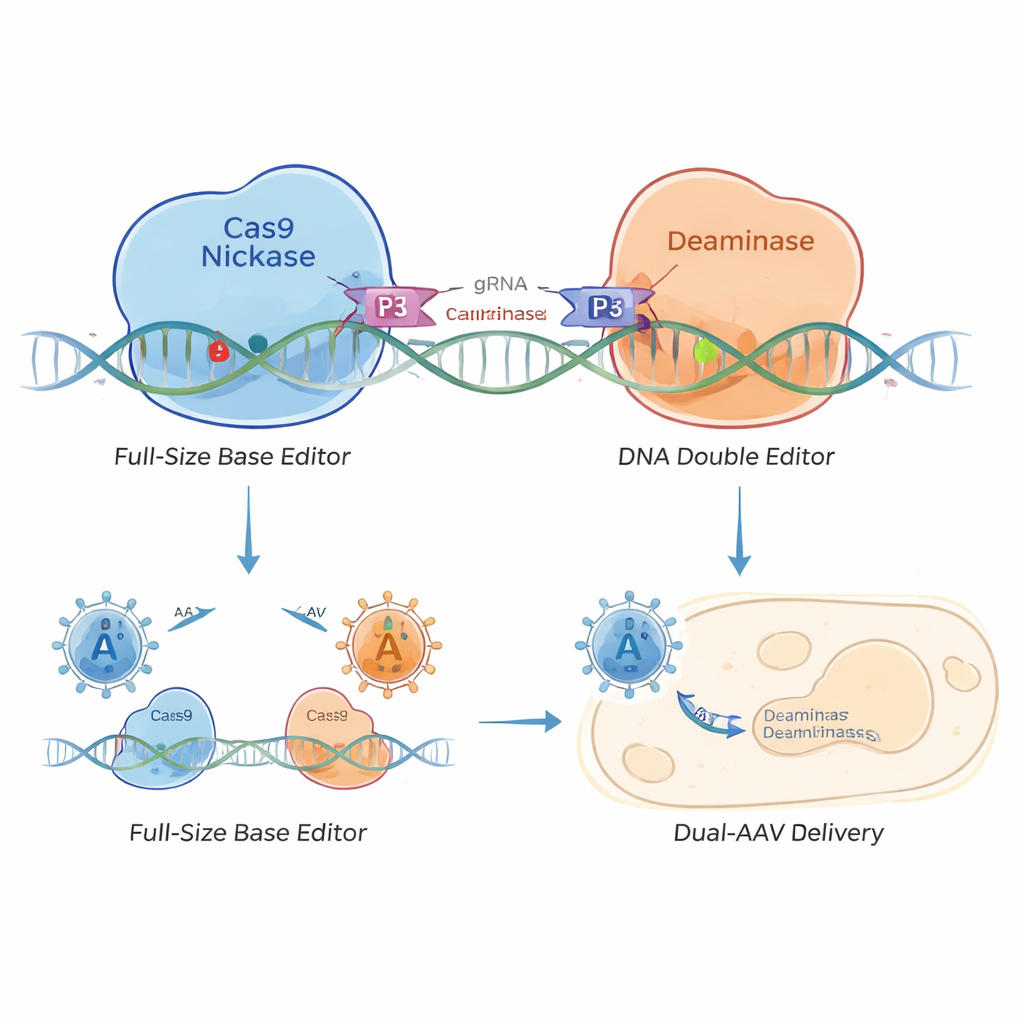
Elastyczna, silna i precyzyjna edycja
Zespół przetestował CC‑BE w różnych typach komórek, w tym ludzkich komórkach oraz pierwotnych komórkach świni, oraz z różnymi wariantami Cas9 rozpoznającymi szerszy zakres sekwencji DNA. Wersje CC‑CBE działały niezawodnie w wielu miejscach i wykazywały szersze „okno edycji”, co oznacza, że mogły zmieniać docelowe litery na dłuższym odcinku DNA, dając naukowcom większą swobodę przy wyborze prowadnic RNA. Wersje CC‑ABE osiągały podobną wydajność do najlepszych istniejących edytorów adeniny, często generując przy tym mniej produktów ubocznych poza celem. Badacze dostosowali także strategię coiled‑coil do nowszych projektów edytorów — takich jak kompaktowy TadCBE i precyzyjny ABE9 — i ponownie stwierdzili, że podział z użyciem par coiled‑coil zachowuje lub poprawia wydajność.
Od hodowli komórek do żywych myszy
Co istotne, autorzy wykazali, że te podzielone edytory działają w żywych organizmach przy zastosowaniu podwójnej dostawy AAV, gdzie każdy wirus przenosi jedną połowę edytora. U myszy, CC‑ABE skierowany przeciwko genowi Pcsk9 w wątrobie osiągnął edycje A→G sięgające około 70%, znacząco obniżając poziom białka Pcsk9 i frakcję LDL we krwi bez oznak uszkodzenia wątroby. 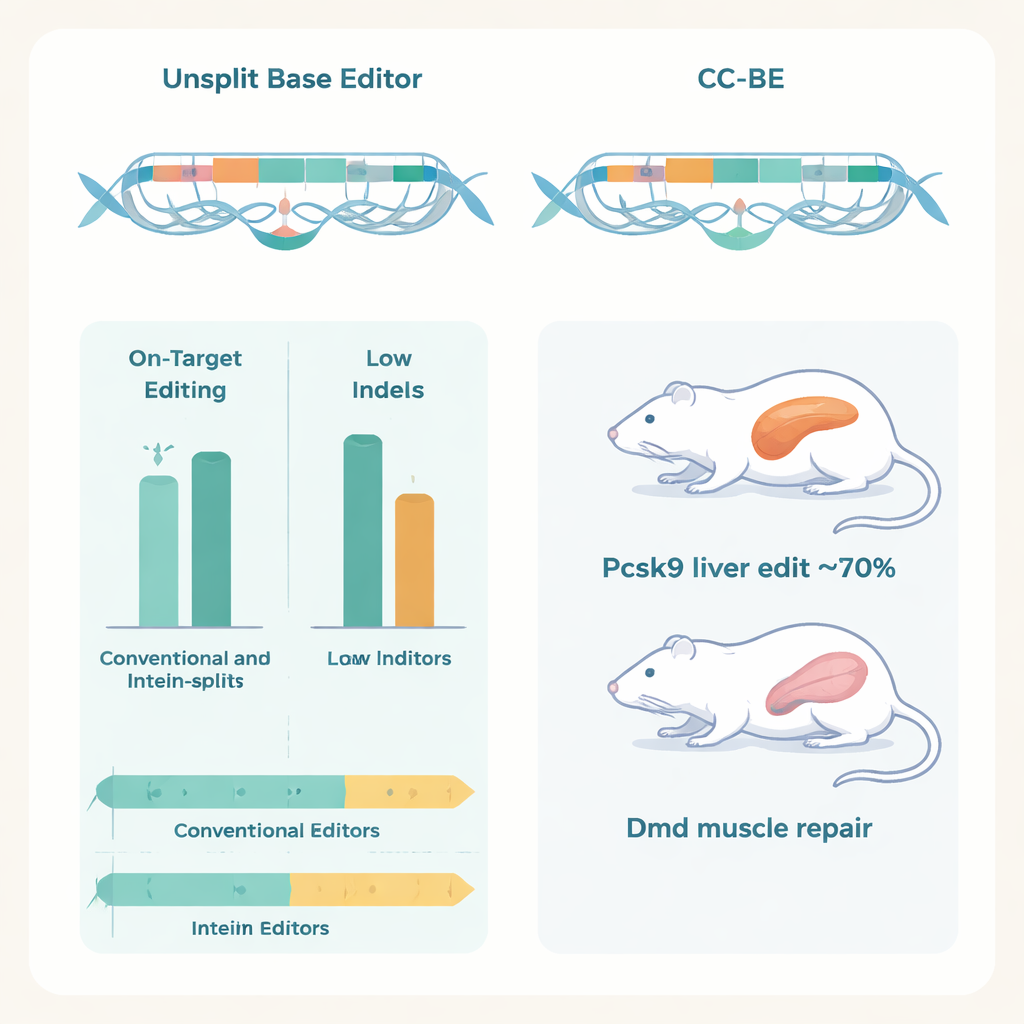
Nowa ścieżka w kierunku praktycznej naprawy DNA
W istocie, badanie przedstawia prosty, lecz potężny inżynieryjny trik: użyć małych „haczyków” coiled‑coil, aby podzielić duże edytory zasad na moduły mieszczące się w AAV, które łączą się ponownie tylko tam, gdzie są potrzebne. Dla osób niebędących ekspertami kluczowa informacja jest taka, że naukowcy mogą teraz zapakować wysoce zdolne narzędzia do naprawy DNA w klinicznie sprawdzone wirusowe nośniki bez poświęcania dokładności czy siły działania. Podejście coiled‑coil może ułatwić projektowanie terapii dla szerokiego spektrum chorób wywołanych pojedynczymi literówkami w genach w takich narządach jak wątroba, serce i mięśnie, przybliżając precyzyjną korekcję genów do zastosowań klinicznych.
Cytowanie: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
Słowa kluczowe: edycja zasad, terapia genowa, CRISPR, dostawa AAV, choroba genetyczna