Clear Sky Science · pl
Imprinting zależny od H3K27me3 i regulacja transkrypcji we wczesnych zarodkach myszy wymaga ograniczenia aktywności PRC2 przez EZHIP
Dlaczego malutkie zarodki potrzebują precyzyjnego czasu genetycznego
Każde ssak zaczyna życie jako jedna komórka, która niesie zestaw chromosomów od matki i jeden od ojca. Chociaż te dwa pakiety genetyczne zawierają prawie te same litery DNA, przychodzą opakowane w różne chemiczne znaczniki, które pomagają decydować, które geny są włączone lub wyłączone. W tym badaniu analizowano, jak taki system znakowania jest utrzymywany w równowadze podczas pierwszych dni po zapłodnieniu u myszy i dlaczego zaburzenie tej równowagi może wykoleić prawidłowy rozwój.
Dwoje rodziców, dwie inaczej zapakowane genomy
U ssaków niektóre geny zachowują się inaczej w zależności od tego, czy pochodzą od matki, czy od ojca — zjawisko zwane imprintingiem genomowym. Klasyczny imprinting opiera się na chemicznych znakach na samym DNA, ale w ostatnich latach odkryto drugi, krótkotrwały typ zależny od modyfikacji białek histonowych zwanej H3K27me3. Histony działają jak szpulki, wokół których owija się DNA, a H3K27me3 zwykle wycisza pobliskie geny. W normalnych zarodkach myszy genom matczyny nosi więcej tej modyfikacji niż genom ojcowski tuż po zapłodnieniu, co pomaga uciszać konkretne kopie genów matczynych przy jednoczesnym dopuszczeniu aktywności kopii ojcowskich.
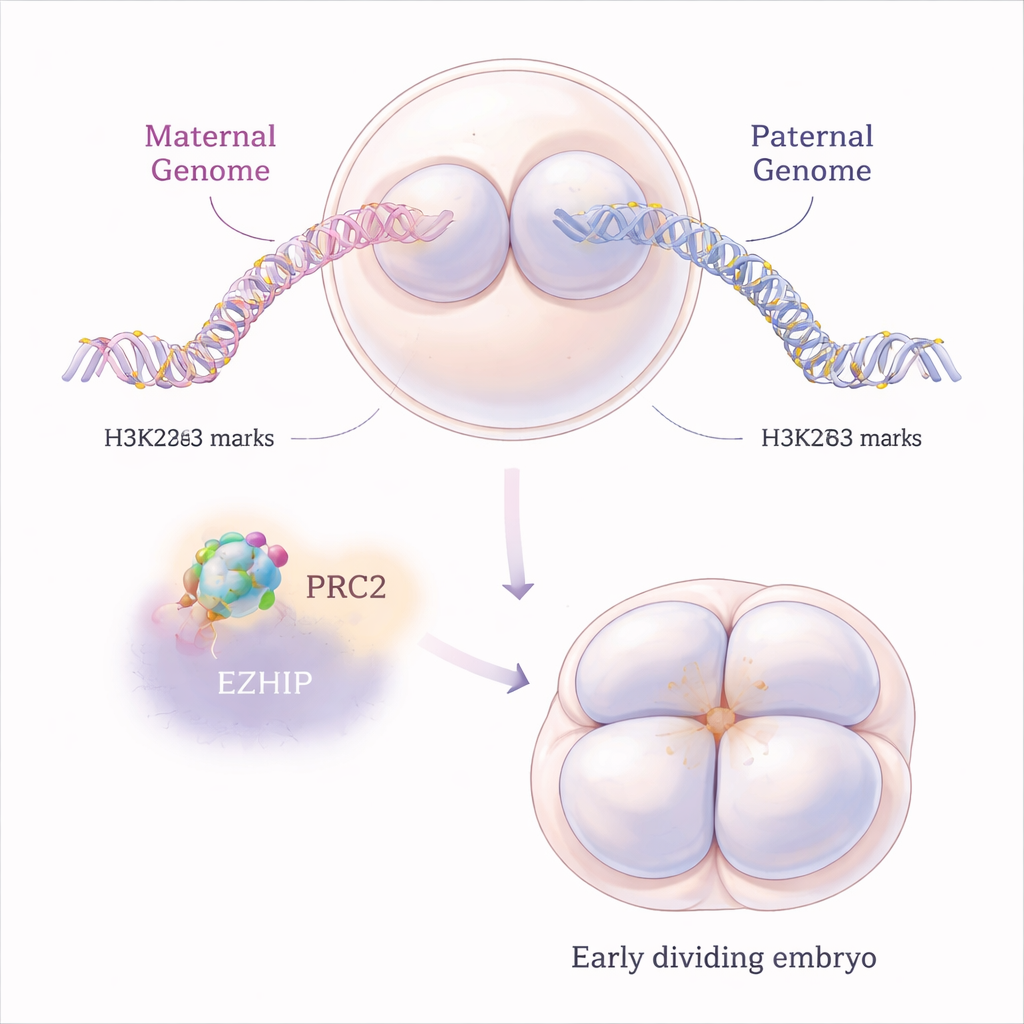
Molekularny hamulec na potężnego represora
H3K27me3 jest nanoszony na chromatynę przez duży kompleks białkowy zwany PRC2. Autorzy skupili się na EZHIP, mniej znanym białku, które wiąże się z PRC2 i spowalnia jego działanie. Komórki jajowe myszy produkują dużo RNA Ezhip, a wynikające z tego białko EZHIP utrzymuje się w zarodkach przez pierwsze podziały komórkowe. Badając myszy, których matki nie posiadały Ezhip, naukowcy zapytali, co się dzieje, gdy naturalny hamulec zostaje usunięty. Stwierdzili, że bez EZHIP komórki jajowe i wczesne zarodki zyskały dodatkowe znaczniki H3K27me3, ale w zaskakująco „spłaszczony” sposób: zamiast ostrych, dobrze zdefiniowanych domen, znak represyjny rozprzestrzeniał się szerzej i zacierał normalne wzorce, wpływając na chromosomy zarówno matczyne, jak i ojcowskie.
Gdy nadmierna represja łamie imprinting
Przy użyciu wrażliwych metod mapowania genomu zespół pokazał, że zwykła asymetria krajobrazów H3K27me3 między genomem matczynym a ojcowskim jest w dużej mierze utracona w zarodkach rozwijających się z komórek jajowych pozbawionych Ezhip. Wiele regionów, które normalnie utrzymują H3K27me3 tylko na jednej kopii rodzicielskiej, zyskało je na obu albo ich wzory zostały rozmyte. Ta zmiana miała istotne konsekwencje dla genów imprintowanych, które są zwykle kontrolowane przez H3K27me3 zamiast metylacji DNA. W zarodkach kontrolnych te geny są zazwyczaj wyrażane głównie z allelu ojcowskiego. W zarodkach pozbawionych matczynego EZHIP te same geny często były aktywne z obu kopii rodzicielskich, a ogólne poziomy RNA dla wielu z nich zwiększały się zamiast być podwójnie uciszone.
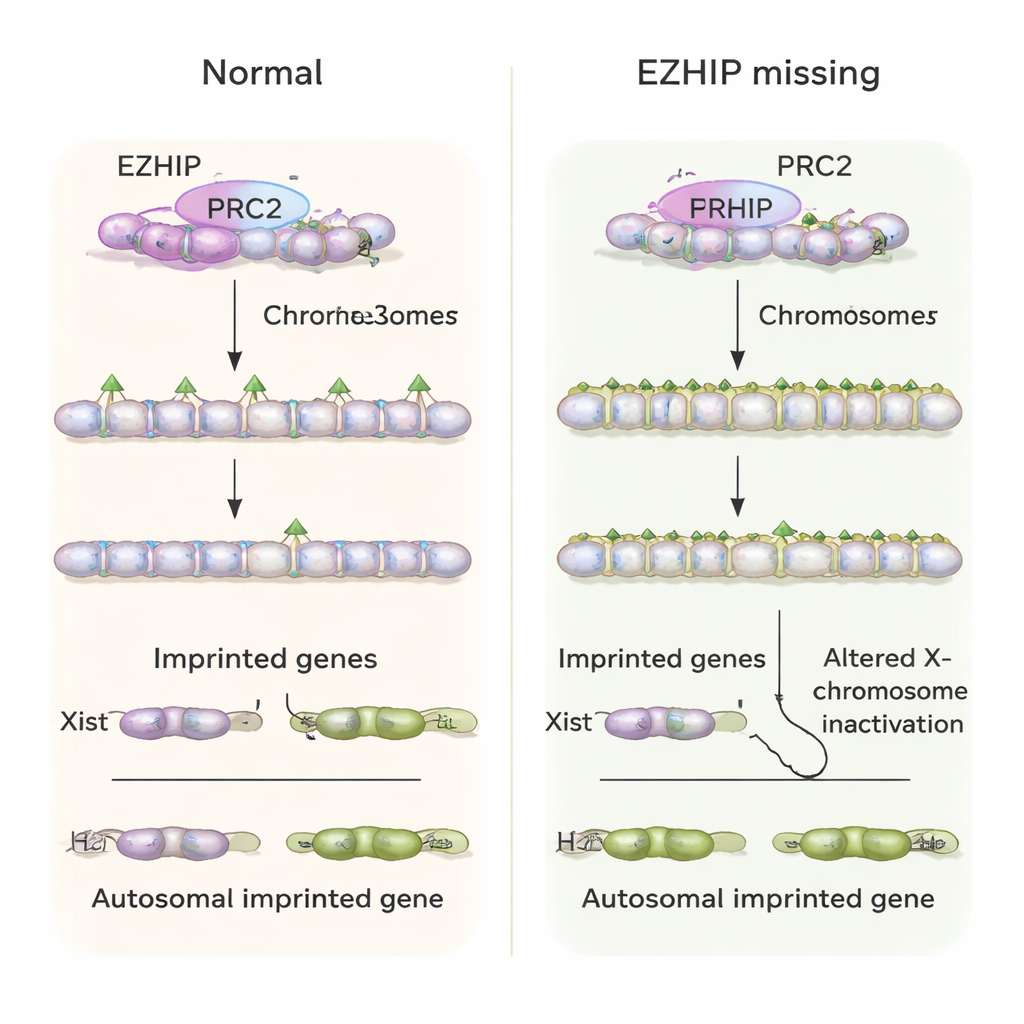
Zakłócona kontrola chromosomu X i kondycja zarodka
Jednym z kluczowych genów imprintowanych zależnych od H3K27me3 jest Xist, długa cząsteczka RNA, która pokrywa i inaktywuje jeden chromosom X w komórkach żeńskich, aby zrównoważyć dawkę genów z samcami. Zwykle we wczesnych zarodkach myszy Xist jest wyrażany tylko z chromosomu X pochodzącego od ojca u samic i wcale u samców. W braku matczynego EZHIP autorzy zaobserwowali, że zarodki żeńskie często wyrażały Xist z obu chromosomów X, podczas gdy zarodki męskie „niewłaściwie” włączały Xist ze swojego pojedynczego X. Prowadziło to do nieprawidłowych wzorców inaktywacji genów sprzężonych z X. Na poziomie całego organizmu myszy urodzone od matek pozbawionych Ezhip były liczniejsze — nośne mniej liczne — oraz zarodki wykazywały zmieniony wzrost i problemy w tkankach pozazarodkowych wspierających łożysko, co odpowiada długotrwałemu stresowi rozwojowemu spowodowanemu wczesnym niepowodzeniem imprintingu.
Za dużo dobrego może być szkodliwe
Dla osoby niezwiązanej ze specjalnością może wydawać się intuicyjne, że więcej znaku wyciszającego jak H3K27me3 po prostu uciszy więcej genów. Zamiast tego praca ta pokazuje, że przeciążenie genomu takimi znacznikami w niewłaściwym układzie może w rzeczywistości podkopać ich zdolność do działania jak precyzyjne przełączniki. Usuwając EZHIP, badacze uwolnili PRC2, powodując, że H3K27me3 rozlał się tak szeroko, iż sygnały imprintingowe zostały rozmyte, a krytyczne regulatory, takie jak Xist, zostały źle kontrolowane. Badanie podkreśla, że we wczesnych zarodkach ważne jest nie tylko posiadanie właściwych cząsteczek, lecz także utrzymanie ich aktywności w ścisłej równowadze, aby genomy matczyny i ojcowski były odczytywane we właściwym balance.»
Cytowanie: Diop, S., Richart, L., Petitalot, A. et al. H3K27me3-dependent imprinting and transcriptional regulation in early mouse embryos requires EZHIP-mediated restriction of PRC2 activity. Nat Commun 17, 1758 (2026). https://doi.org/10.1038/s41467-026-68467-4
Słowa kluczowe: epigenetyka, imprinting genetyczny, wczesny rozwój embrionalny, inaktywacja chromosomu X, kompleks Polycob PRC2