Clear Sky Science · pl
Wykorzystanie glukanem indukowanej odporności wyuczonej do epigenetycznego i metabolicznego przeprogramowania makrofagów w celu wzmocnienia odpowiedzi na szczepionkę przeciw rakowi jelita grubego
Przebudzenie pierwszych obrońców organizmu
Rak jelita grubego jest jednym z najgroźniejszych nowotworów na świecie, a większość pacjentów nie odnosi korzyści z obecnych terapii immunologicznych. W tym badaniu rozważono intrygującą hipotezę: co jeśli moglibyśmy „wyszkolić” wrodzony układ odpornościowy — pierwszych obrońców organizmu — aby zapamiętywał zagrożenie i wspierał działanie szczepionek przeciw guzom jelita grubego? Używając naturalnego cukru pochodzącego z drożdży, zwanego beta‑glukanem, autorzy pokazują, jak komórki wczesnej odpowiedzi immunologicznej można przeprogramować, tak że szczepionki przeciwnowotworowe wywołują silniejsze i trwalsze ataki na guzy.
Dlaczego rak jelita grubego potrzebuje nowych strategii
Rak jelita grubego powoduje niemal milion zgonów rocznie na świecie, a liczba zachorowań wśród młodszych dorosłych rośnie. Standardowe leczenia, takie jak operacja, chemioterapia i radioterapia, mogą być skuteczne, lecz wielu pacjentów doświadcza nawrotów i poważnych skutków ubocznych. Nowsze leki immunologiczne, np. inhibitory punktów kontrolnych, działają bardzo dobrze tylko w niewielkiej podgrupie nowotworów jelita grubego z określonymi defektami naprawy DNA. U większości pacjentów te leki, a nawet eksperymentalne szczepionki przeciwnowotworowe, zawodzą, ponieważ środowisko guza jest zdominowane przez komórki i sygnały tłumiące odpowiedź immunologiczną.
Nauka nowych sztuczek wrodzonej odporności
Wrodzone komórki odpornościowe — zwłaszcza makrofagi — zwykle reagują szybko, lecz krótko, i uważano, że nie mają pamięci. Jednak prace ostatniej dekady ujawniły zjawisko „odporności wyuczonej”, w którym silny początkowy bodziec pozostawia trwałe ślady w tych komórkach, pozwalając im reagować intensywniej w przyszłości. Autorzy zastosowali beta‑glukan, składnik ścian komórkowych drożdży, aby wywołać taki wyuczony stan. U myszy krótkie leczenie całymi cząstkami beta‑glukanu przeprogramowało makrofagi zarówno na poziomie aktywności genów, jak i metabolizmu komórkowego. Gdy te „wyszkolone” zwierzęta później otrzymały szczepionkę przeciw rakowi jelita grubego opartą na zmodyfikowanym adenowirusie (nazywaną PeptiCrad), ich układ odpornościowy wytworzył silniejsze komórki zabójcze T, które lepiej rozpoznawały i atakowały cele specyficzne dla nowotworu. 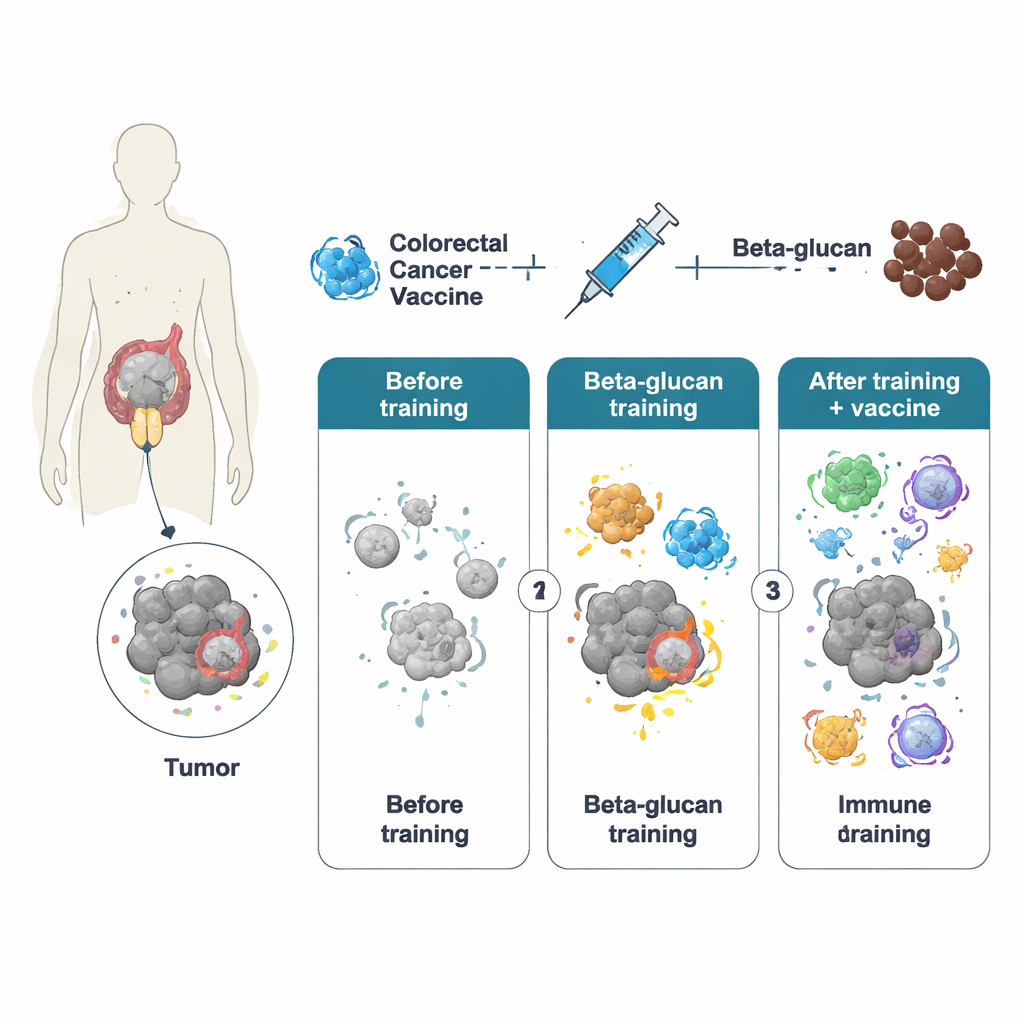
Przeprogramowanie energetyki i komunikacji wewnątrz guzów
Idąc dalej, badacze izolowali komórki odpornościowe z guzów i profilowali ich metabolizm oraz aktywność genów pojedynczo. Odkryli, że wyszkolone makrofagi przestawiły się na intensywny tryb metaboliczny przypominający „efekt Warburga”, w którym komórki szybko spalają cukier i przekierowują zasoby na budowę składników niezbędnych do funkcji i wzrostu. Komórki te także zwiększyły metabolizm kreatyny — znany szerzej z suplementów sportowych — co pomagało dostarczać dodatkową energię konieczną do produkcji prozapalnych cząsteczek. Równocześnie specyficzne chemiczne znaczniki na białkach związanych z DNA (zwłaszcza wzrost H3K4me3) oznaczały geny zaangażowane w produkcję chemokin, skutecznie utrwalając zapalny, przeciwnowotworowy program genowy, który utrzymywał się przez dłuższy czas.
Budowanie zespołu przekaźników odpornościowych
Sekwencjonowanie pojedynczych komórek ujawniło stopniowy przekaz sygnałów między różnymi komórkami odpornościowymi w obrębie guza. Najpierw wyszkolone makrofagi uwalniały duże ilości dwóch kluczowych sygnałów, CXCL9 i CXCL10, które przyciągały komórki NK poprzez receptor CXCR3. Gdy te komórki NK zostały zrekrutowane, nie ograniczały się jedynie do zabijania komórek nowotworowych; wydzielały także kolejny komunikator, CCL5, który przyciągał wyspecjalizowaną podpopulację komórek dendrytycznych znaną jako cDC1. Te komórki dendrytyczne świetnie prezentują fragmenty guza komórkom T. W rezultacie więcej komórek CD8 T zostało aktywowanych i przekształciło się w komórki pamięci efektorowej — komórki, które reagują szybko i silnie przy ponownym zetknięciu z guzem. Blokowanie wykorzystania kreatyny, usuwanie makrofagów lub komórek NK albo przerywanie tych szlaków chemokin osłabiało kontrolę guza, podkreślając, jak bardzo powodzenie szczepionki zależało od tego obwodu makrofag–NK–dendrytyczna komórka–komórka T. 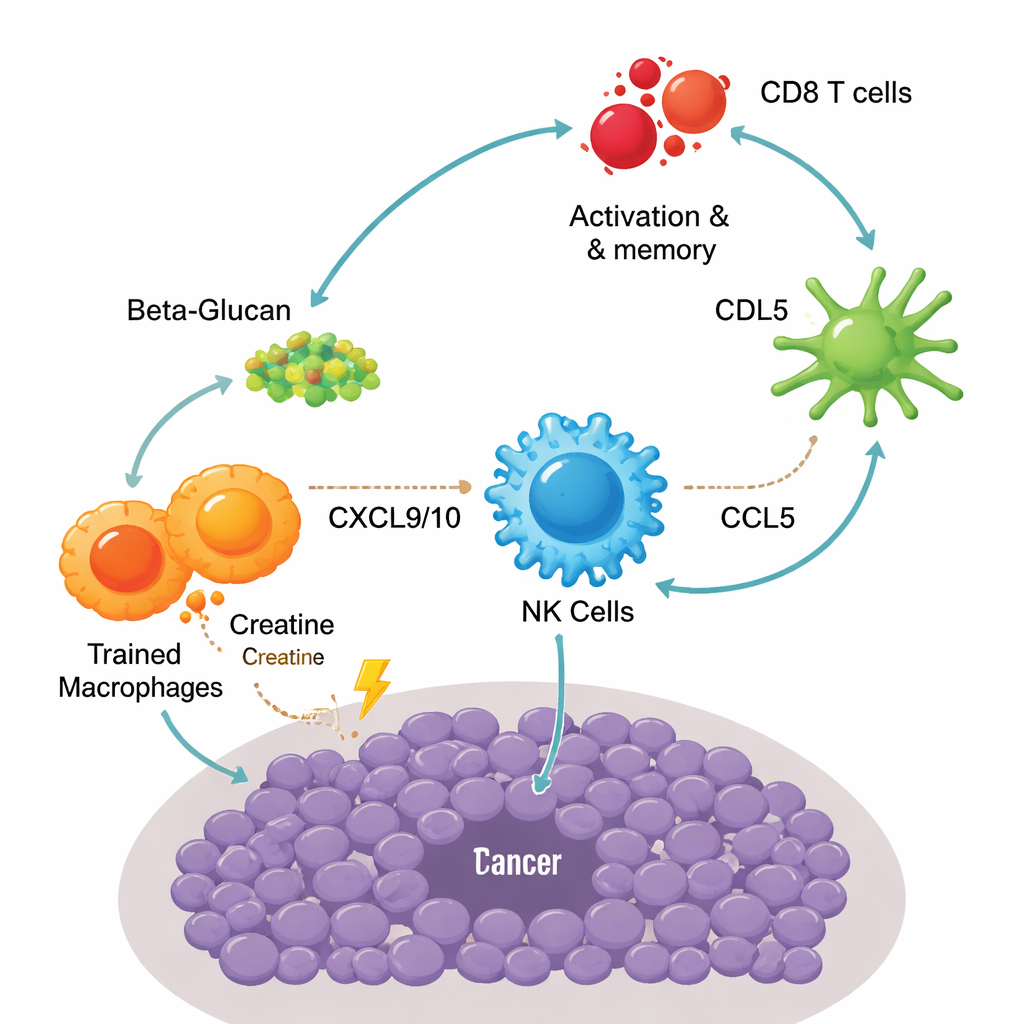
Od modeli mysich do ludzkich organoidów nowotworowych
Zespół przetestował podejście w kilku modelach mysich raka jelita grubego, w tym w szczególnie opornym typie, odpornym na powszechne immunoterapie. W każdym przypadku połączenie treningu beta‑glukanem ze szczepionką spowalniało wzrost guza skuteczniej niż każde z tych działań osobno. Co ważne, badacze wyszli poza modele mysie. Ludzkie komórki krwi eksponowane na beta‑glukan lepiej reagowały na peptyd szczepionkowy przeciw rakowi jelita grubego, wytwarzając więcej cytokin stymulujących odpowiedź immunologiczną. Gdy te wyszkolone komórki odpornościowe zostały powiększone i współhodowane z miniaturowymi guzami pochodzącymi od pacjentów (organoidami), zabijały więcej komórek nowotworowych niż komórki niewyszkolone. Usunięcie ludzkich monocytów i makrofagów z tego układu likwidowało tę korzyść, potwierdzając, że wyszkolone komórki są kluczowymi organizatorami reakcji, a nie bezpośrednimi zabójcami guza.
Co to może znaczyć dla przyszłych szczepionek przeciwnowotworowych
Mówiąc prosto, praca ta pokazuje, że bezpieczny, pochodzący z drożdży cukier może „wyszkolić” komórki wrodzonego układu odpornościowego, by wspierały skuteczniejsze szczepienia przeciw rakowi jelita grubego. Przeprogramowując sposób, w jaki makrofagi wykorzystują energię oraz które geny utrzymują w gotowości, trening beta‑glukanem uruchamia efekt domina: makrofagi przyciągają komórki NK, komórki NK rekrutują wyspecjalizowane komórki dendrytyczne, a razem budują silniejszą armię pamięciowych komórek CD8 T. Choć wiele pozostaje do sprawdzenia w badaniach klinicznych — w tym bezpieczeństwo, timing i najlepsze kombinacje szczepionek — odporność wyuczona jawi się tutaj jako obiecująca strategia adiuwantowa, która może zamienić „zimne”, tłumiące guzy jelita grubego w takie, które układ odpornościowy potrafi rozpoznać i kontrolować.
Cytowanie: Hamdan, F., Gandolfi, S., D’Alessio, F. et al. Leveraging glucan-induced trained immunity for the epigenetic and metabolic rewiring of macrophages to enhance colorectal cancer vaccine response. Nat Commun 17, 1757 (2026). https://doi.org/10.1038/s41467-026-68466-5
Słowa kluczowe: immunoterapia raka jelita grubego, odporność wyuczona, beta-glukan, makrofagi i komórki NK, szczepionki przeciw nowotworom