Clear Sky Science · pl
Badanie przesiewowe CRISPR in vivo identyfikuje członków kompleksu SAGA jako kluczowych regulatorów hematopoezy
Dlaczego utrzymanie równowagi produkcji krwi ma znaczenie
Każdego dnia organizm wytwarza po cichu setki miliardów nowych komórek krwi, które przenoszą tlen, zwalczają infekcje i zatrzymują krwawienie. Ta nieustanna produkcja zależy od rzadkich „matczynych” komórek w szpiku kostnym, zwanych komórkami macierzystymi tworzącymi krew. Gdy mechanizmy kontrolujące te komórki zawodzą, u ludzi mogą pojawić się anemia, osłabiona odporność lub nowotwory, takie jak białaczka. W tym badaniu postawiono proste, lecz istotne pytanie: spośród tysięcy genów w naszym genomie, które rzeczywiście są niezbędne do utrzymania zdrowej i zrównoważonej produkcji komórek krwi?
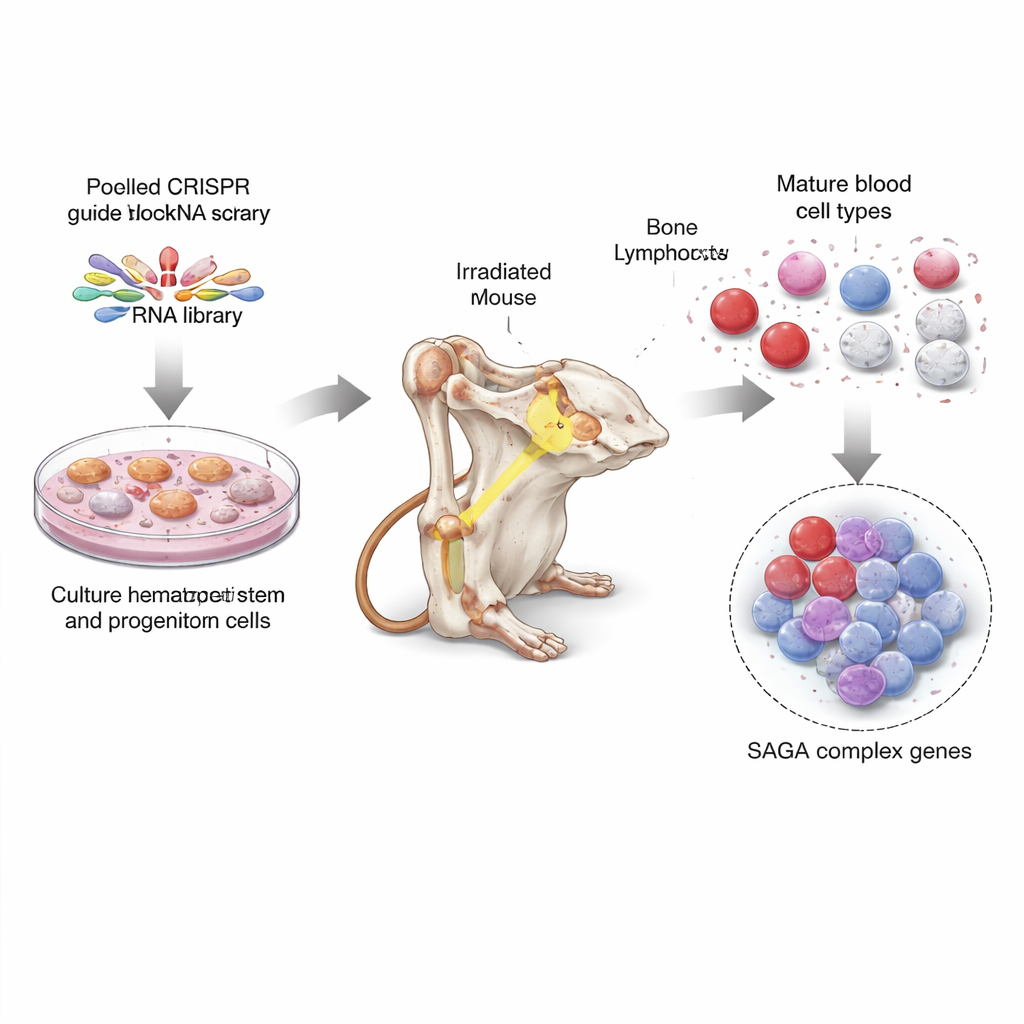
Poszukiwanie skarbów w całym genomie w komórkach macierzystych myszy
Aby to zbadać, naukowcy użyli CRISPR — narzędzia do edycji genów często porównywanego do molekularnych nożyc — aby wyłączyć niemal każdy gen w genomie myszy, stosując dziesięć sond na gen. Najpierw rozmnożyli duże liczby komórek macierzystych i prekursorowych ze szpiku w specjalnych warunkach hodowlanych, a następnie zakażali te komórki złożoną pulą sond CRISPR, tak że każda komórka miała zablokowany inny gen. Potem przeszczepili te zmieszane, edytowane komórki do kilkudziesięciu naświetlanych promieniami rentgenowskimi myszy, pozwalając edytowanym komórkom odbudować układy krwiotwórcze zwierząt. Miesiące później oczyszczono różne dojrzałe typy komórek krwi i komórkopodobne komórki macierzyste ze szpiku i odczytano, które sondy CRISPR były nad- lub niedoreprezentowane. To ujawniło, jakie utraty genów sprzyjały utrzymaniu się komórek niedojrzałych, a które wspierały produkcję w pełni uformowanych komórek krwi.
Wyłania się ukryte centrum kontroli zwane SAGA
Wśród wielu znanych regulatorów tworzenia krwi pojawił się zaskakujący zestaw trafień: kilka elementów strukturalnych dużego zespołu białkowego zwanego kompleksem SAGA, w tym geny o nazwach Tada2b, Taf5l i Tada1. SAGA nie wytwarza komórek krwi bezpośrednio; zamiast tego pomaga włączaniu lub wyłączaniu innych genów poprzez chemiczne znakowanie białek opakowujących DNA, zwanych histonami. Kiedy zespół indywidualnie wyłączał te składniki SAGA i przeszczepiał zedytowane komórki do myszy, obserwowano spójny wzorzec. Komórki niedojrzałe w szpiku się kumulowały, ale ich zdolność do dojrzewania w krążące granulocyty, erytrocyty i niektóre komórki odpornościowe była wyraźnie zmniejszona. W istocie komórki macierzyste i prekursorowe ugrzęzły w wąskim gardle, niezdolne do zakończenia drogi prowadzącej do w pełni funkcjonalnych komórek krwi.
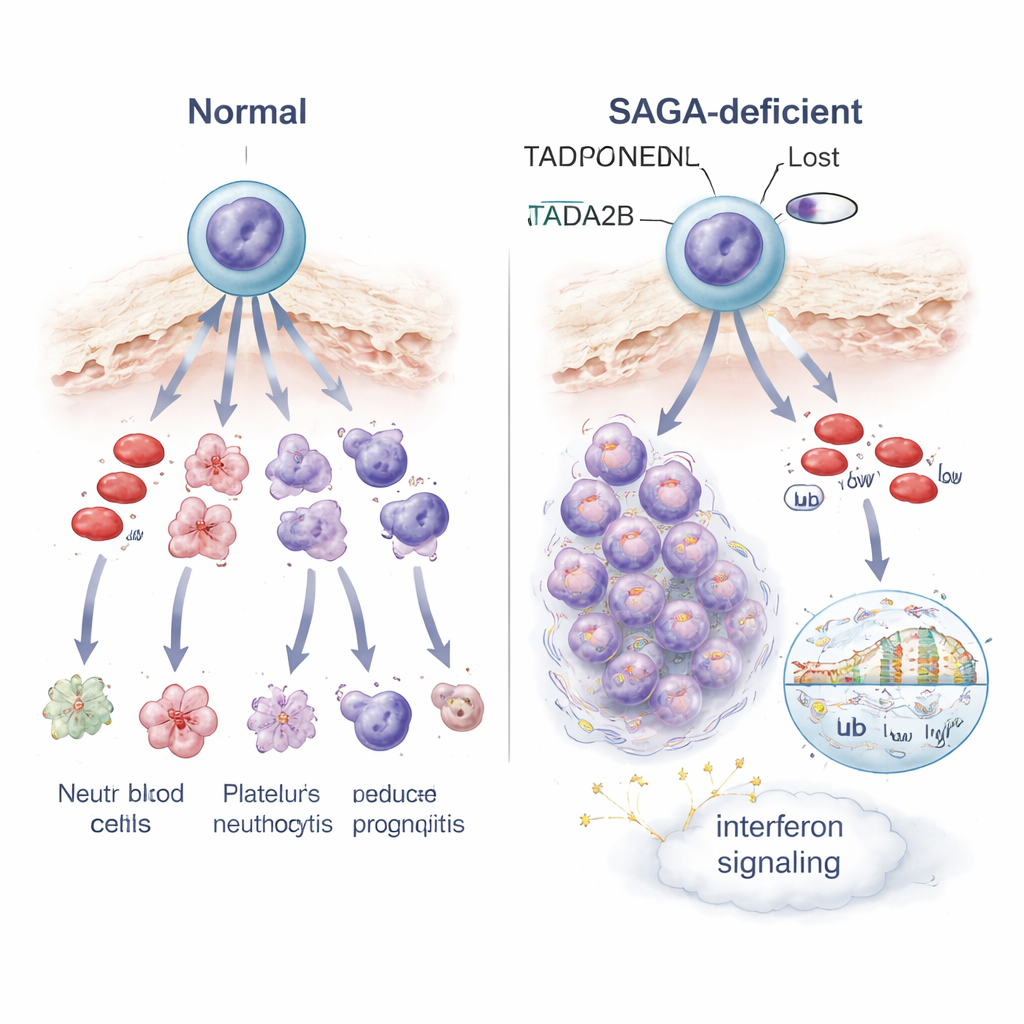
Jak zaburzona kontrola genów zmienia losy komórek i sygnały stresu
Aby zrozumieć, co idzie nie tak w tych zablokowanych komórkach, naukowcy profilowali aktywność genów pojedynczo na poziomie pojedynczych komórek i w populacji. Utrata Tada2b lub Taf5l przeprogramowała aktywność wielu genów w komórkach macierzystych, z dwoma wyraźnymi motywami. Po pierwsze, geny zaangażowane w sygnalizację interferonową — normalnie część antywirusowej obrony organizmu — zostały włączone, co wskazuje na wewnętrzny alarm lub stan stresu. Po drugie, mitochondria komórek, maleńkie elektrownie napędzające pracę komórkową, stały się mniej aktywne, a zmienione komórki wykazywały większą wrażliwość na lek celujący w produkcję energii mitochondrialnej. Na poziomie pakowania DNA komórki pozbawione Tada2b wykazywały obniżone poziomy jednego znaku histonowego związanego z otwartą, aktywną chromatyną oraz zmiany innego znaku powiązanego z tym, jak geny są odczytywane. Te przesunięcia w chemii chromatyny prawdopodobnie pomagają wyjaśnić, dlaczego wiele genów, w tym te kierujące prawidłowym dojrzewaniem krwi, ulega niewłaściwej regulacji.
Od podstawowych mechanizmów do modeli chorób
Zespół następnie zbadał, czy zmiana aktywności SAGA w górę lub w dół może odwrócić te efekty. Wymuszone nadprodukcja Tada2b obniżyła aktywność genów związanych z interferonem i zmniejszyła odsetek komórek o cechach macierzystych — efekt odwrotny do utraty genu. Leczenie normalnych komórek macierzystych lekiem hamującym kluczowe podjednostki enzymatyczne SAGA odtworzyło dużą część sygnatury związanej z utratą Tada2b, co wzmacnia przekonanie, że modyfikująca chromatynę aktywność SAGA jest centralna dla jej roli. Wreszcie badacze sięgnęli po model komórek ludzkich zespołu mielodysplastycznego, stanu przedbiałaczkowego, w którym produkcja krwi słabnie, a szlaki interferonowe często są podwyższone. Gdy wyłączyli składniki SAGA w tych ludzkich komórkach i przeszczepili je do myszy z defektem układu odpornościowego, zedytowane komórki zyskały przewagę wzrostową i ponownie aktywowały programy genów interferonowych i mieloidalnych, sugerując, że to centrum regulacyjne także kształtuje zachowanie choroby.
Co to oznacza dla zdrowia krwi i przyszłych terapii
Dla czytelnika niebędącego specjalistą główne przesłanie jest takie: badanie ujawnia potężne centrum kontrolne — kompleks SAGA — które pomaga komórkom macierzystym tworzącym krew decydować, kiedy pozostawać niedojrzałymi, kiedy dojrzewać i jak unikać szkodliwych reakcji stresowych. Gdy brak kluczowych części SAGA, komórki macierzyste się kumulują, ale nie produkują wystarczającej liczby funkcjonalnych komórek krwi, podczas gdy sygnały stresowe i przypominające odpowiedź przeciwwirusową rosną, a mitochondria zawodzą. Odkrycia te pogłębiają nasze rozumienie, jak utrzymuje się zdrowa produkcja krwi przez całe życie, a także sugerują, że subtelne zmiany aktywności SAGA mogą przyczyniać się do problemów krwi związanych z wiekiem i zaburzeń takich jak zespół mielodysplastyczny. W dłuższej perspektywie mapowanie tego układu kontrolnego może pomóc naukowcom zaprojektować terapie, które skierują wadliwe komórki macierzyste z powrotem w stronę zrównoważonej, odpornej produkcji krwi.
Cytowanie: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
Słowa kluczowe: komórki macierzyste hematopoetyczne, przesiewanie CRISPR, kompleks SAGA, sygnalizacja interferonowa, zespół mielodysplastyczny