Clear Sky Science · pl
Wnioskowanie architektury chromatyny w pojedynczym loci dzięki probabilistycznej lokalizacji DNA in situ
Jak trójwymiarowy kształt DNA kontroluje, kiedy geny się włączają
Nasze DNA często przedstawia się jako prostą drabinę, ale w komórkach składa się ono w złożone pętle i spirale. Te kształty mają znaczenie: pomagają decydować, które geny się włączą, kiedy i gdzie. Badanie to wprowadza nowy sposób obserwacji drobnych trójwymiarowych układów DNA wokół pojedynczego genu w rozwijających się zarodkach muchy owocowej, ujawniając, jak subtelne zmiany w układzie fałdowania DNA mogą modyfikować wzorce aktywności genów kształtujące plan ciała.
Obserwowanie kontroli genów w rozwijającym się zarodku
W miarę rozwoju zarodka tysiące genów muszą się włączać i wyłączać w odpowiednich momentach. Wiele z tych decyzji podejmują krótkie fragmenty DNA zwane enhancerami, które mogą leżeć dziesiątki tysięcy nukleotydów od genów, które regulują. Aby działać, enhancery muszą fizycznie zbliżyć się do docelowego genu w przestrzeni 3D, pętlując DNA tak, by odległe miejsca stykały się ze sobą. Jednak te pętle są bardzo małe, dynamiczne i trudne do zobaczenia. Autorzy badania skupili się na pojedynczym genie, brinker (brk), u muchy Drosophila. Gen ten pomaga formować wczesny zarodek, włączając się w pasku wzdłuż boku jaja. Trzy pobliskie elementy kontrolne — dwa enhancery (E1 i E2) oraz element promotor-proksymalny (PPE) tuż przy genie — współpracują, by wygenerować ten precyzyjny wzorzec.
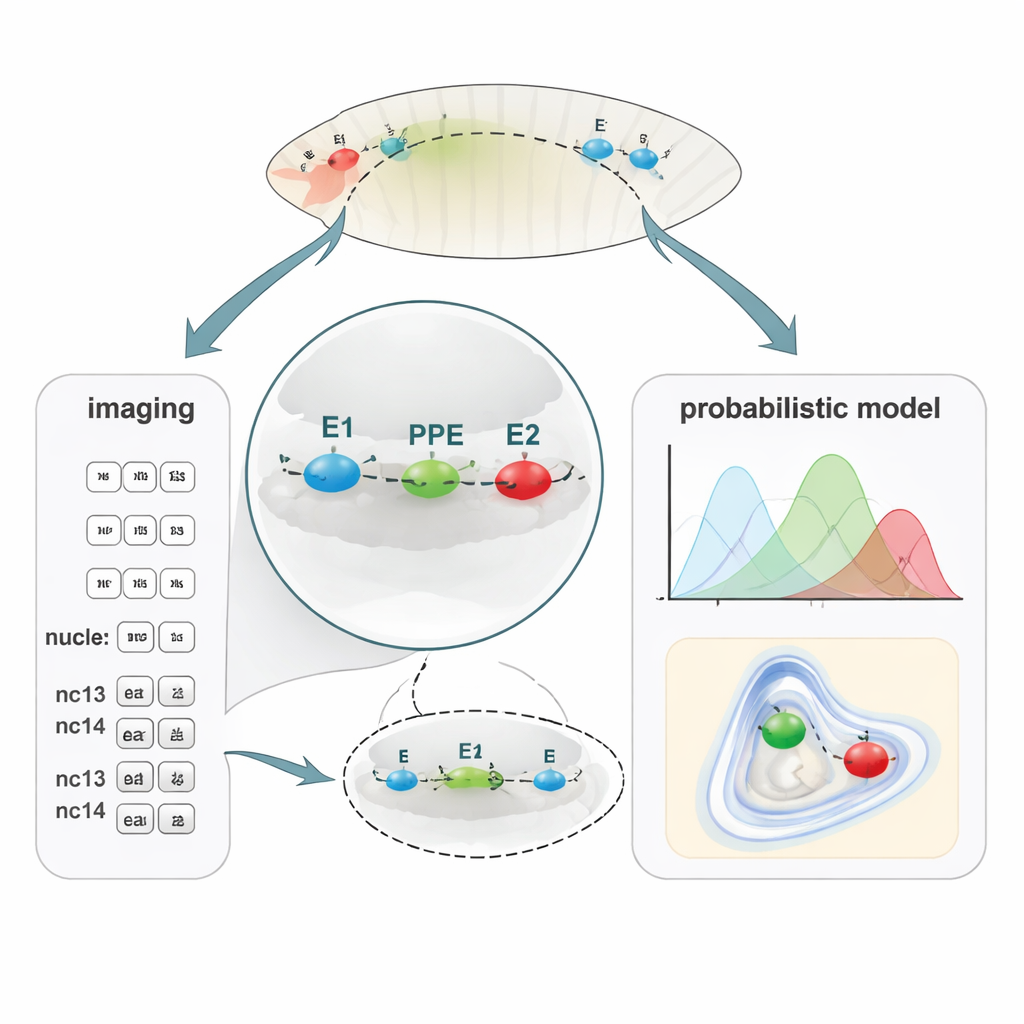
Nowy sposób mapowania mikroskopijnych odległości DNA
Aby powiązać składanie się DNA z aktywnością genu, zespół opracował metodę PLOTTED (Probabilistic Localization of Oligopaint Tagged Target Element Distances). Najpierw zastosowali znakowanie DNA metodą Oligopaint FISH, przyłączając trzy różne barwniki fluorescencyjne do regionów E1, PPE i E2 w utrwalonych zarodkach much. Za pomocą konfokalnego mikroskopu nadrozdzielczego zmierzyli odległości 3D między tymi trzema kolorowymi punktami w dziesiątkach tysięcy jąder komórkowych w zarodkach na kolejnych cyklach jądrowych, od tuż przed rozpoczęciem aktywności genu (pre-nc13) poprzez późniejsze stadia (nc13 i nc14). Następnie wprowadzili wszystkie te odległości do niestandardowego potoku obliczeniowego, który filtruje pomiary zaszumione i buduje mapy prawdopodobieństwa pokazujące, gdzie każdy element najprawdopodobniej się znajduje względem pozostałych. Zamiast pojedynczej statycznej „pętli”, PLOTTED tworzy krajobraz prawdopodobnych kształtów chromatyny na każdym etapie rozwoju.
Gdy DNA się zagęszcza, gen się budzi
W zarodkach dzikiego typu badacze zaobserwowali, że w miarę jak zarodek osiąga cykl jądrowy 13, oba enhancery zbliżają się do PPE: lokalne sąsiedztwo DNA wokół genu brk staje się bardziej zwarte. Po tym punkcie odległości między trzema elementami pozostają stosunkowo stabilne. Co istotne, ten moment czasowy pokrywa się z początkiem ekspresji brk, co sugeruje, że „zaciskanie” konfiguracji DNA pomaga umożliwić włączenie genu. PLOTTED wykazał też, że ta zwarta aranżacja pojawia się częściej w obszarach zarodka, w których brk jest aktywny, natomiast luźniejsze konfiguracje dominują tam, gdzie gen jest represjonowany, wzmacniając związek między architekturą 3D a transkrypcją.
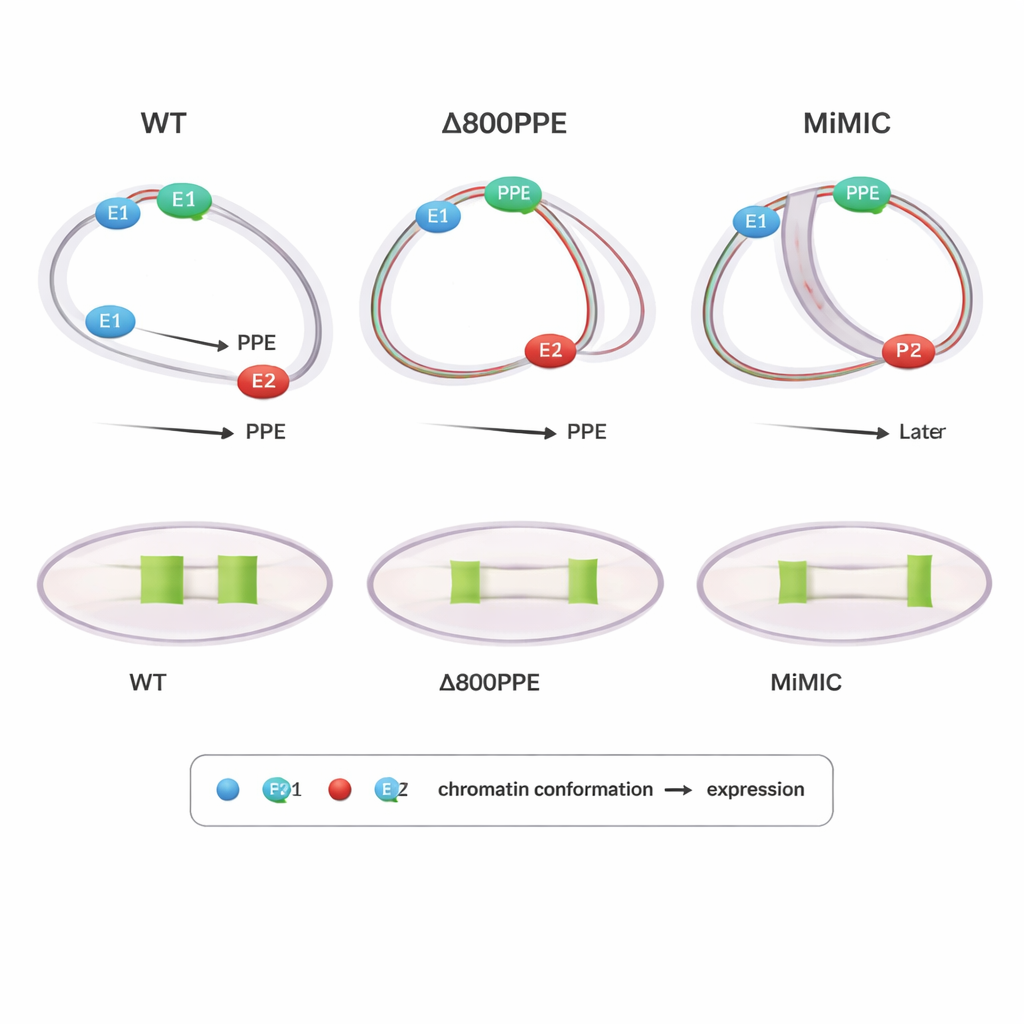
Mutacje ujawniają, jak ważne są czas i pozycja
Aby zbadać przyczynowość, autorzy przeanalizowali muszki z zaprojektowanymi zmianami w locus brk. W jednym mutantzie usunięto 800 par zasad PPE, osłabiając ten centralny element; w innym wstawiono kasetę DNA o długości 7,3 kb (MiMIC) między E1 a PPE, efektywnie oddalając je od siebie i dodając dodatkowy promotor. Oba mutanty wykazywały opóźnioną lub zmniejszoną ekspresję brk. PLOTTED wyjaśnił przyczynę: w linii z delecją PPE zagęszczenie odległości między PPE i oboma enhancerami następowało później niż normalnie, a w późnych stadiach PPE pozostawało zbyt blisko E1, uniemożliwiając E2 wywołanie szerokiego wzorca ekspresji widocznego w typie dzikim. W linii MiMIC PPE wiązało się zbyt wcześnie i silnie z E2, a dopiero później zbliżało się do E1, ponownie zaburzając normalne przekazanie roli między enhancerami. Wyniki sugerują, że nie tylko fakt zbliżenia elementów ma znaczenie, ale także kiedy i z którym partnerem są najbliżej — to kluczowe dla prawidłowego wyniku genowego.
Składanie DNA różni się w obrębie zarodka
Ponieważ PLOTTED zachowuje informację przestrzenną w nienaruszonych zarodkach, zespół mógł także sprawdzić, czy architektura DNA różni się w różnych regionach ciała. Porównując strefy boczne, gdzie brk jest aktywny, z obszarami brzusznymi, gdzie jest represjonowany, stwierdzili, że trzy elementy leżą bliżej siebie w regionach aktywnych i rozciągają się dalej w domenach represjonowanych. Wzdłuż osi głowa–ogon zaobserwowano, że odległości E1–PPE zmieniają się inaczej z przodu niż z tyłu zarodka, co sugeruje, że sygnały regionalne dostrajają architekturę chromatyny, by precyzować wzorce ekspresji genów. Te ustalenia wspierają pogląd, że trójwymiarowe ułożenie DNA regulatoryjnego zależy od kontekstu, odzwierciedlając zarówno czas, jak i pozycję w rozwijającym się organizmie.
Dlaczego to ma znaczenie poza muchami owocowymi
Mówiąc prosto, badanie pokazuje, że sposób, w jaki DNA fałduje się wokół pojedynczego genu, jest ściśle powiązany z tym, kiedy i gdzie gen się włącza. Nowa metoda PLOTTED dostarcza praktycznego sposobu mapowania tych mikroskopijnych „sąsiedztw” DNA w nienaruszonych tkankach, używając szeroko dostępnych mikroskopów i prostej chemii, połączonych z wydajnym modelowaniem probabilistycznym. Chociaż metoda została zademonstrowana w zarodkach muchy, można ją zastosować w wielu organizmach i modelach chorobowych. W miarę jak naukowcy coraz częściej odkrywają, że nieprawidłowe fałdowanie chromatyny leży u podstaw zaburzeń rozwojowych i nowotworów, narzędzia takie jak PLOTTED pomogą ujawnić, jak niewielkie przesunięcia w trójwymiarowym układzie enhancerów i genów mogą rozlać się na duże zmiany losu komórek i zdrowia.
Cytowanie: Le, M.T., McGehee, J., Dunipace, L. et al. Inferring chromatin architecture at a single locus through probabilistic in situ DNA localization. Nat Commun 17, 1752 (2026). https://doi.org/10.1038/s41467-026-68460-x
Słowa kluczowe: architektura chromatyny, interakcje enhancer-promotor, embriogeneza Drosophila, regulacja genów, mikroskopia nadrozdzielcza