Clear Sky Science · pl
Komórkowo pochodzące z grzebienia nerwowego DKK1 i NEDD4 modulują sygnalizację Wnt w drugie polu serca, by zorganizować rozwój przewodu odpływowego
Dlaczego mali budowniczowie serca mają znaczenie
Wczesne serce zarodka zaczyna jako prosta rurka, ale musi szybko przekształcić się w złożony organ tłoczący krew do ciała i do płuc. Subtelne potknięcia w tym procesie budowy mogą powodować poważne wady wrodzone, w tym takie, które wymagają operacji krótko po narodzinach. W badaniu tym odkryto, jak dwie grupy komórek komunikują się ze sobą podczas kształtowania głównej drogi odpływu serca i ujawniono błąd molekularny, który może przyczyniać się do wrodzonych wad serca u myszy i u ludzi.
Dwie ekipy budujące rampę odpływu serca
Część serca odprowadzająca krew z komór—przewód odpływowy—powstaje z obszaru zwanego drugim polem sercowym. Komórki w tym rejonie muszą pozostawać plastycznymi „przodkami” wystarczająco długo, aby zostać dodane do rosnącego przewodu odpływowego, a następnie przełączyć się w dojrzałą tkankę mięśniową we właściwym czasie. Tuż obok przemieszczają się komórki grzebienia nerwowego, wędrująca populacja, która pomaga budować wielkie tętnice i zastawki. Wcześniejsze prace sugerowały, że te komórki grzebienia nerwowego w jakiś sposób wpływają na drugie pole sercowe, ale mechanizm tej komunikacji był nieznany. 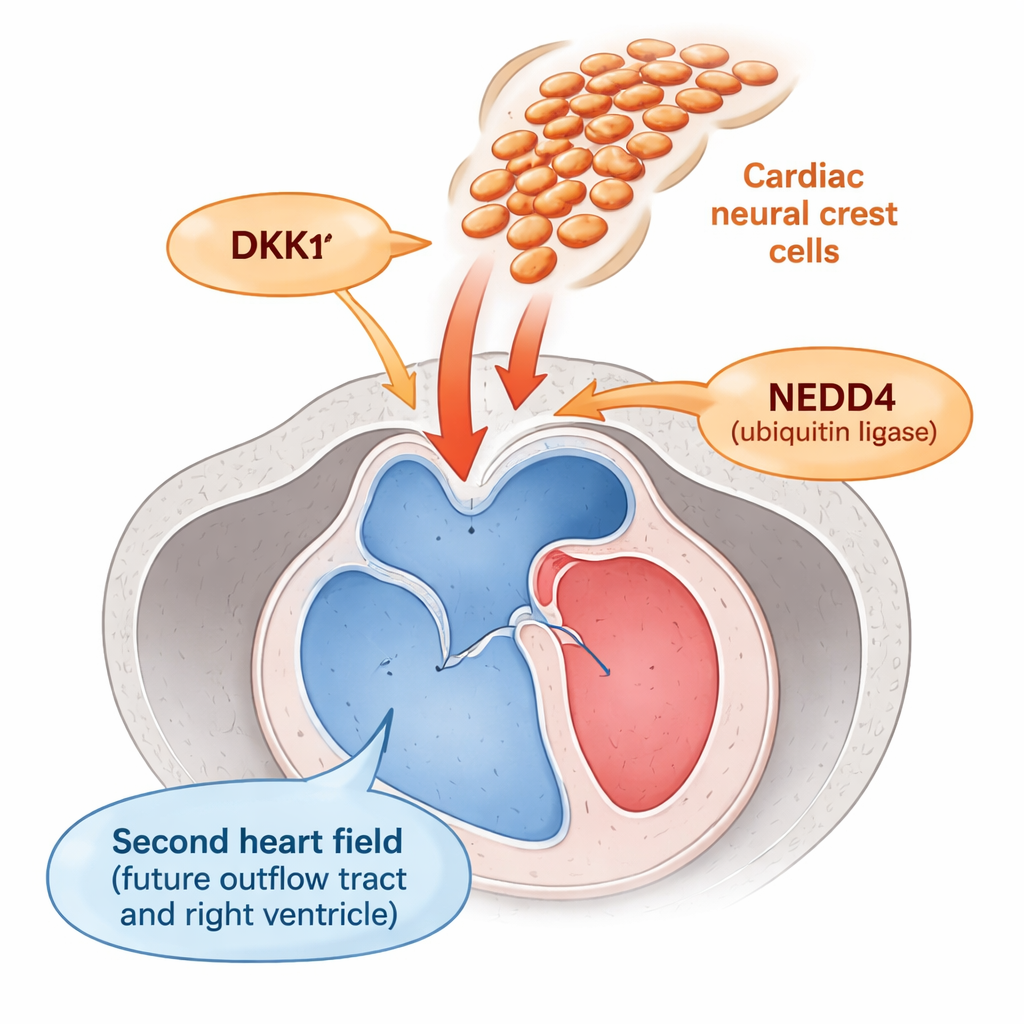
Molekularny ściemniacz sygnałów wzrostu
Autorzy odkryli, że komórki grzebienia nerwowego działają jak ściemniacz dla kluczowego sygnału wzrostu nazwanego Wnt, który utrzymuje komórki progenitorowe w podziale i opóźnia ich dojrzewanie. Stwierdzili, że komórki grzebienia nerwowego są głównym źródłem DKK1, małego białka wydzielanego, które wyłącza sygnalizację Wnt w pobliskich komórkach. Sam DKK1 jest normalnie kontrolowany przez NEDD4, białko znakujące DKK1 do usunięcia. U zarodków myszy pozbawionych Nedd4 specyficznie w komórkach grzebienia nerwowego stężenie DKK1 narastało do nieprawidłowo wysokich poziomów. Nadmiar DKK1 osłabił aktywność Wnt w sąsiednim drugim polu sercowym, o czym świadczyło zmniejszenie ilości beta‑kateiny w jądrze — standardowy wskaźnik sygnalizacji Wnt — oraz obniżenie poziomów wielu genów reagujących na Wnt.
Gdy timing zawodzi, geometria serca się nie powodzi
Zbyt dużo DKK1 i zbyt mało sygnalizacji Wnt miało oczywisty skutek: komórki drugiego pola sercowego zaczęły różnicować się w mięsień sercowy za wcześnie. Markery dojrzałej tkanki mięśniowej pojawiły się wcześnie w tej strefie prekursorowej, a pozostało mniej komórek niedojrzałych, które mogłyby wydłużyć przewód odpływowy. Śledząc dzielące się komórki w czasie, zespół wykazał, że do przewodu odpływowego u mutantów włączano mniej komórek drugiego pola sercowego. W rezultacie przewód odpływowy był krótszy i obrócony niewłaściwie, prowadząc do niewłaściwego ustawienia między wielkimi tętnicami a komorami. Te błędy strukturalne przypominały ludzkie wady konotrunkalne, takie jak dwuujściowa prawa komora i pokrewne malformacje obserwowane u myszy z całkowitym wyłączeniem Nedd4.
Udowodnienie roli sygnału i związek z chorobą u ludzi
Aby potwierdzić, że zmieniona sygnalizacja Wnt rzeczywiście powodowała te problemy, badacze manipulowali ścieżką za pomocą leków u ciężarnych myszy. Blokowanie Wnt u w przeciwnym razie zdrowych zarodków wywołało te same przedwczesne różnicowanie i defekty rotacji, jakie obserwowano po utracie Nedd4, podczas gdy zmniejszenie dawki genu Dkk1 na tle deficytu Nedd4 częściowo przywróciło wielkość i orientację przewodu odpływowego. Wreszcie zespół zidentyfikował dziecko z tetralogią Fallota, które nosiło rzadką dziedziczną zmianę w NEDD4 osłabiającą jego zdolność do znakowania DKK1 do degradacji. Myszy zaprojektowane tak, by niesły mieć tę samą wariantę Nedd4, rozwijały prawostronne wady ściany serca i przegrody, co wspiera ideę, że błędna kontrola NEDD4–DKK1 może przyczyniać się do ludzkich wad wrodzonych serca. 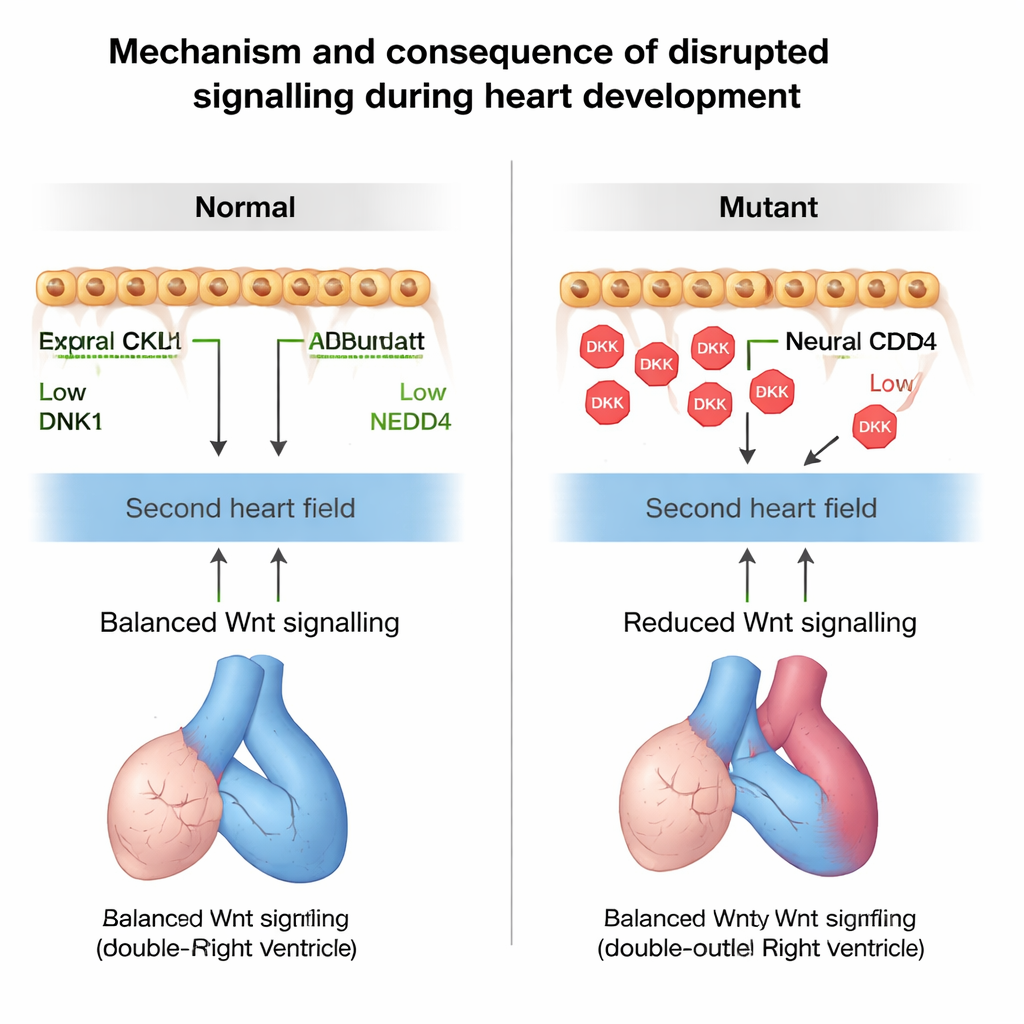
Co to znaczy dla zrozumienia wad serca
Dla osób niebędących specjalistami kluczowa wiadomość jest taka, że „rampa odpływu” serca zależy od precyzyjnego timing’u, kiedy jej elementy przestają się mnożyć i zaczynają przekształcać w mięsień. Ten timing jest kontrolowany nie tylko wewnątrz samej tkanki sercowej, lecz także przez sąsiednie komórki grzebienia nerwowego, które wyciszają sygnał wzrostu za pośrednictwem pary NEDD4–DKK1. Gdy ten molekularny ściemniacz jest ustawiony zbyt nisko, przewód odpływowy jest niedorozwinięty i źle ustawiony, co prowadzi do poważnych wad wrodzonych. Mapując tę ścieżkę i wiążąc ją z wariantem genu u człowieka, badanie dostarcza nowych wskazówek, jak powstają niektóre wrodzone wady serca, i wskazuje potencjalne cele molekularne dla przyszłej diagnostyki lub interwencji.
Cytowanie: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
Słowa kluczowe: wrodzone wady serca, rozwój serca, komórki grzebienia nerwowego, sygnalizacja Wnt, przewód odpływowy serca