Clear Sky Science · pl
Pospolite usunięcie fragmentu DNA zmieniające 3’UTR genu mdr1 wiąże się ze zmniejszoną wrażliwością na meflochinę u pasożytów P. vivax od kambodżańskich pacjentów
Dlaczego to badanie nad malarią ma znaczenie
Dla osób mieszkających lub podróżujących do rejonów endemiczych malarii skuteczne leki to kwestia życia i śmierci. Pasożyty malarii nieustannie ewoluują, by przetrwać leczenie. Badanie koncentruje się na Plasmodium vivax, głównej przyczynie malarii poza Afryką, i ujawnia subtelną zmianę genetyczną, która może już pomagać pasożytowi tolerować jeden z ważnych leków — meflochinę. Zrozumienie tej zmiany teraz może pomóc władzom zdrowia publicznego wyprzedzić pojawiającą się oporność na leki.
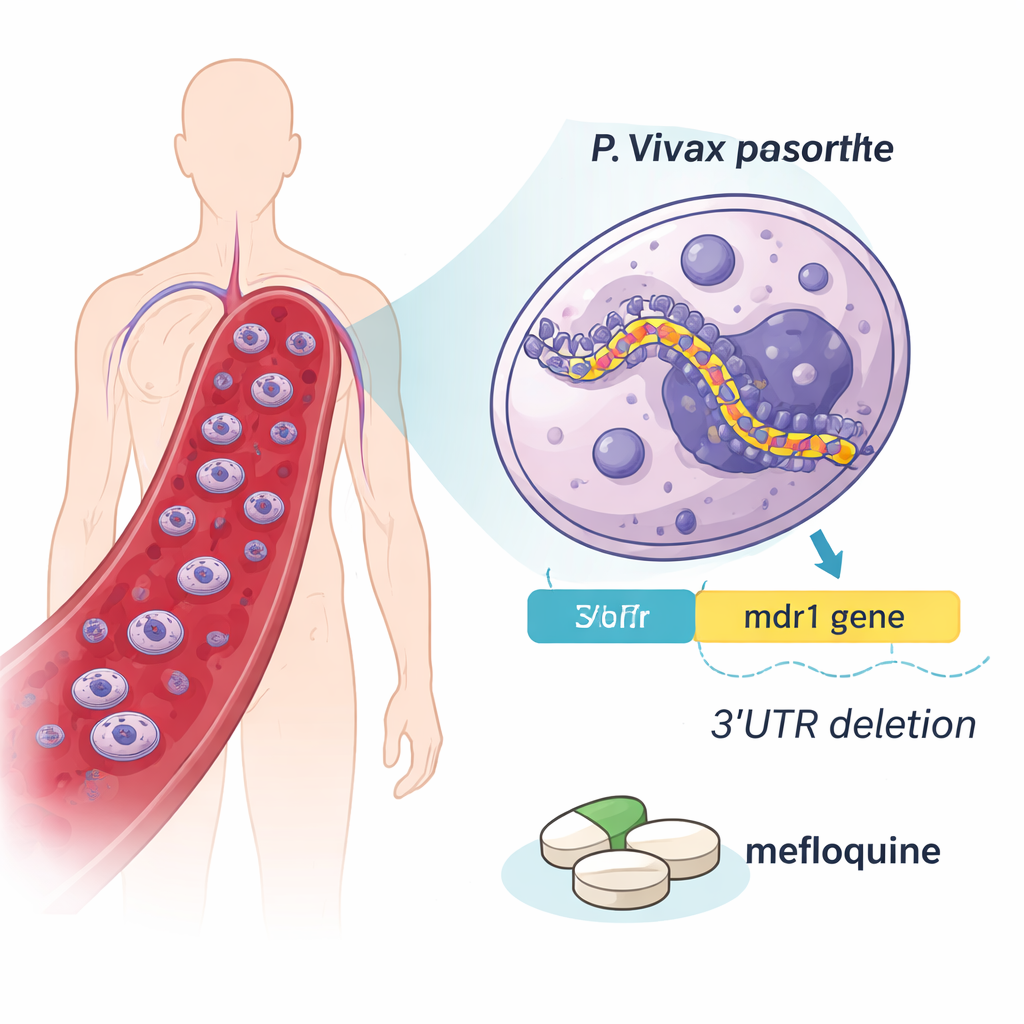
Uparcie utrzymujący się pasożyt i kurczący się wybór terapii
Malarię u ludzi wywołuje kilka spokrewnionych pasożytów, ale P. vivax jest szczególnie trudny do wykorzenienia. Może ukrywać się w wątrobie przez miesiące, zanim ponownie pojawi się we krwi, i często krąży na poziomach zbyt niskich, by wykryć je standardowymi testami. Przez dekady lek pierwszego rzutu — chlorochina — był skuteczny przeciwko P. vivax, ale pojawiły się sygnały oporności. W efekcie Światowa Organizacja Zdrowia zaleca teraz stosowanie terapii opartych na artemizyninie w połączeniu z partnerem o dłuższym działaniu (ACT), na przykład meflochiną. Ponieważ hodowla P. vivax w warunkach laboratoryjnych jest trudna, naukowcy w dużym stopniu polegają na próbkach od pacjentów i wskazówkach genetycznych, by śledzić, jak pasożyt reaguje na te leki.
Maleńki brakujący fragment DNA w kluczowym genie związanym z opornością
Naukowcy zsekwencjonowali genomy 206 próbek P. vivax pobranych od pacjentów z malarią w Kambodży w latach 2021–2023. Szukali odcinków DNA, które zostały usunięte lub zduplikowane. Spośród wielu przestawień wyróżniał się jeden: ponad 80% pasożytów nosiło małe usunięcie DNA położone tuż za końcem regionu kodującego genu o nazwie mdr1 (multidrug resistance 1). Gen ten koduje białko transportujące, które może wypompowywać różne związki, w tym leki, przez błonę wewnątrz pasożyta. W przeciwieństwie do wcześniej opisywanych mutacji, to usunięcie o długości 837 par zasad nie zmieniało samej sekwencji białka. Leżało natomiast w tzw. 3' nieprzetłumaczalnym regionie (3'UTR) — fragmencie genu, który nie jest tłumaczony na białko, lecz silnie wpływa na to, ile białka ostatecznie zostanie wytworzone.
Niezależne usunięcia i zmienione komunikaty z tego samego genu
Aby sprawdzić, czy podobne zmiany występują także gdzie indziej, zespół ponownie przeanalizował niemal 830 genomów P. vivax z 25 krajów. Odkryli kolejne, krótsze usunięcie pokrywające ten sam okolony region mdr1 u pasożytów z Ameryki Południowej. Szczegółowe porównania i potwierdzające testy PCR wykazały, że usunięcia z Azji Południowo-Wschodniej i z Ameryki Południowej są różne, co sugeruje, że powstały niezależnie — wskazówka, że selekcja naturalna może faworyzować zmiany w tym regionie regulacyjnym. Wykorzystując sekwencjonowanie RNA z 95 kambodżańskich infekcji, badacze pokazali, że pasożyty z usunięciem wytwarzały alternatywną wersję mRNA mdr1 z innym 3'UTR. Po uwzględnieniu długości transkryptu pasożyty z usunięciem miały prawie dwa razy więcej mRNA mdr1 niż te bez niego, co sugeruje, że brakujący fragment DNA lub nowa sekwencja 3'UTR pomaga stabilizować lub zwiększać ekspresję genu.
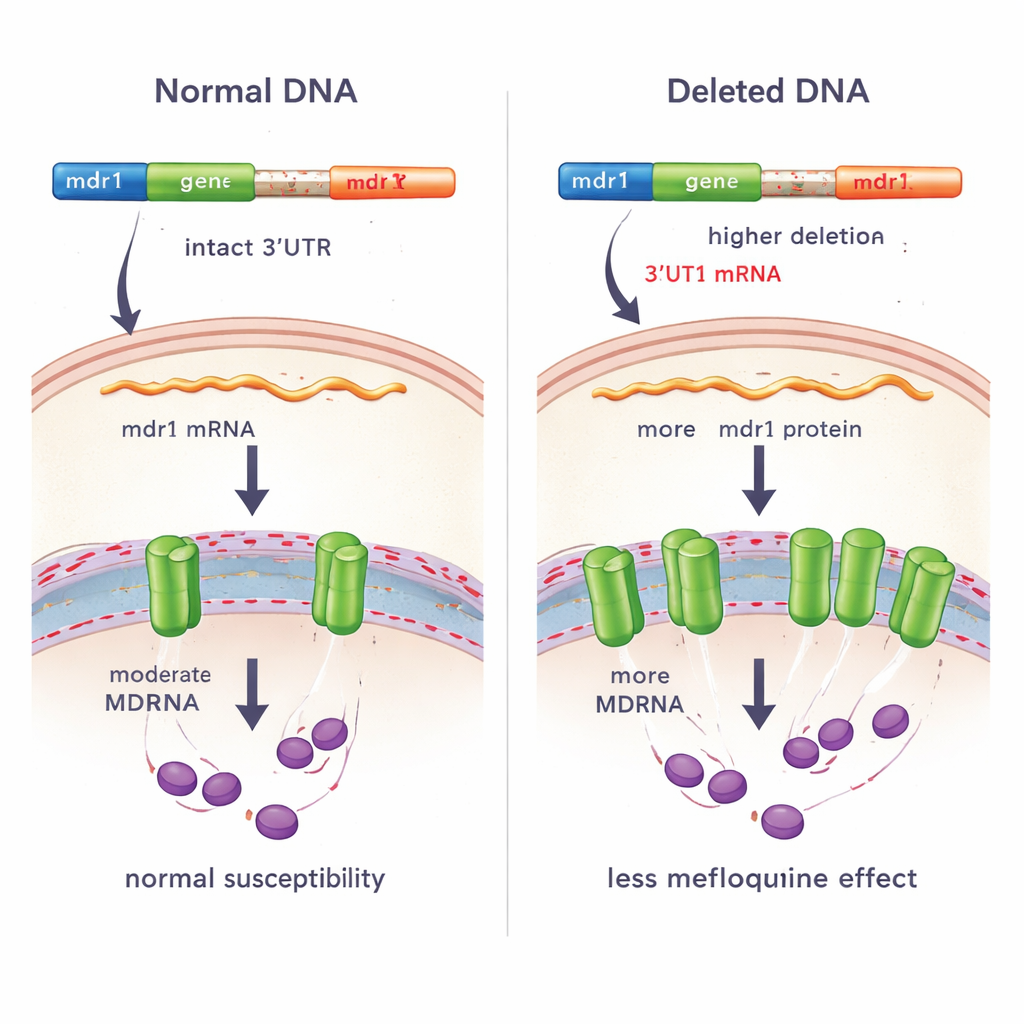
Powiązanie usunięcia z odpowiedzią na lek u pacjentów i w testach laboratoryjnych
Ponieważ mdr1 był wcześniej powiązany z opornością na kilka leków przeciwmalarycznych, zespół zbadał, czy usunięcie ma związek z odpowiedzią pasożytów na leczenie. Najpierw porównali tempo oczyszczania pasożytów z krwi pacjentów po leczeniu artesunatem. Wśród 167 infekcji nie stwierdzono istotnej różnicy w tempie oczyszczania między pasożytami z usunięciem a bez niego, co sugeruje, że ta zmiana genetyczna nie wpływa bezpośrednio na wrażliwość na sam artesunat. Jednak w mniejszej grupie 14 infekcji, gdzie badacze mierzyli wzrost pasożytów w obecności meflochiny poza organizmem, pasożyty z usunięciem miały skłonność do wyższych wartości IC50 — co oznacza, że potrzebowały więcej leku, by zahamować wzrost — niż pasożyty bez usunięcia. Ten wzorzec jest zgodny ze zmniejszoną podatnością na meflochinę, choć wielkość próbki była ograniczona.
Niepokojący wzrost w czasie i jego możliwe konsekwencje
Aby zrozumieć, jak rozpowszechnione stało się to usunięcie, autorzy przebadali 592 zarchiwizowane próbki P. vivax zebrane w całej Kambodży w latach 2014–2024. Przed wprowadzeniem meflochiny jako części ACT wobec malarii vivax około 2016–2017 r. około 30% pasożytów nosiło to usunięcie. Po zmianie częstość wzrosła powyżej 60%, a następnie ustabilizowała się — trend ten był statystycznie istotny i utrzymywał się także przy ograniczeniu analizy do wschodniej Kambodży. Usunięcie było obecne w niskich poziomach już przed szerokim stosowaniem meflochiny przeciwko P. vivax, prawdopodobnie w wyniku pośredniej ekspozycji, gdy lek stosowano do leczenia P. falciparum, lub dlatego, że zmiana wpływa także na odpowiedź na inne leki. Wraz z niedawnymi doniesieniami o nieco wolniejszym oczyszczaniu pasożytów po leczeniu artemizyniną wyniki budzą obawę, że P. vivax w Kambodży może zmierzać w kierunku zmniejszonej skuteczności obecnej kombinacji artesunat–meflochina.
Co to oznacza dla kontroli malarii
Dla osób niebędących specjalistami najważniejszy przekaz jest taki, że nawet jeśli główny gen odpowiedzialny za oporność pasożyta wydaje się nienaruszony, małe zmiany w pobliskich „mechanizmach sterujących” DNA mogą zmienić, jak mocno gen jest włączany. W tym przypadku powszechne usunięcie w niekodującym regionie mdr1 wydaje się zwiększać aktywność genu i wiąże się z nieco słabszym działaniem meflochiny na P. vivax. Chociaż nie ma jeszcze wyraźnych dowodów na porażki leczenia w Kambodży, rosnąca częstość tego usunięcia sugeruje, że nacisk selekcyjny może potajemnie faworyzować pasożyty z tą cechą. Wczesne rozpoznanie i monitorowanie takich subtelnych genetycznych sygnałów ostrzegawczych może pomóc władzom zdrowotnym dostosować politykę lekową, opracować lepsze narzędzia nadzoru i chronić kurczący się zestaw skutecznych terapii przeciwmalarycznych.
Cytowanie: Ko, K., Tebben, K., Andrianinarivomanana, T. et al. A common DNA deletion altering the 3’UTR of mdr1 is associated with reduced mefloquine susceptibility in P. vivax parasites from Cambodian patients. Nat Commun 17, 1748 (2026). https://doi.org/10.1038/s41467-026-68456-7
Słowa kluczowe: Plasmodium vivax, oporność na leki przeciwmalaryczne, meflochina, gen mdr1, Kambodża