Clear Sky Science · pl
Af-CUT&Tag: czuła i pozbawiona przeciwciał metoda profilowania chromatyny wykorzystująca genetycznie kodowane znaczniki i wysokoczułe wiążące białka sprzężone z Tn5
Zajrzeć do naszej komórkowej centrali sterowania DNA
Każda komórka w twoim ciele nieustannie decyduje, które geny włączyć, a które wyłączyć, co kształtuje wszystko — od naprawy wątroby po ryzyko nowotworu. Naukowcy badają te decyzje, mapując miejsca, w których kluczowe białka siedzą na naszym DNA, ale najlepsze narzędzia do tego przez długi czas polegały na kruchej, kosztownej technologii przeciwciał, która nie zawsze działa dobrze. W artykule przedstawiono nowy, pozbawiony przeciwciał sposób na odwzorowywanie interakcji DNA–białko, nazwany Af-CUT&Tag, który jest bardziej czuły, bardziej niezawodny i wystarczająco wydajny, by działać nawet na małych próbkach i pojedynczych komórkach.
Dlaczego przeciwciała nas ograniczają
Klasyczne metody mapowania chromatyny wymagają przeciwciał — dużych białek w kształcie litery Y, które rozpoznają konkretny białkowy cel — aby poprowadzić enzym do właściwych miejsc na DNA. Gdy przeciwciała działają perfekcyjnie, pozwalają badaczom zobaczyć, gdzie czynniki transkrypcyjne i inni regulatorzy wiążą się w całym genomie. W praktyce jednak przeciwciała bywają trudne do uzyskania, niestabilne jakościowo i mogą być blokowane przez powszechne modyfikacje chemiczne białek, takie jak fosforylacja czy acetylacja. Te problemy mogą zamazywać powstałe mapy, ograniczać zakres badanych białek i utrudniać porównywanie wyników między laboratoriami czy eksperymentami.
Maleńkie znaczniki i sprytne wiążące zastępują przeciwciała
Af-CUT&Tag całkowicie omija przeciwciała, nadając białku zainteresowania mały genetyczny identyfikator. Z wykorzystaniem edycji genomu CRISPR badacze fuzjonują krótkie peptydowe znaczniki, takie jak HiBiT lub ALFA, z naturalnym białkiem w komórkach lub tkankach. Następnie używają zmodyfikowanych białek partnerskich — wysokowydajnych wiążących, które rozpoznają te znaczniki — bezpośrednio sprzężonych z enzymem Tn5, który tnie DNA i przyłącza startery do sekwencjonowania. Gdy fuzja wiążący–Tn5 przyczepi się do znacznika na białku docelowym, nacinana jest sąsiednia cząstka DNA i oznaczane są te miejsca do sekwencjonowania. Ponieważ znaczniki są bardzo małe, a fuzja wiążący–Tn5 znacznie mniejsza niż przeciwciało, system ten łatwo przenika do komórek i jąder, wiąże się z wyjątkową precyzją i nie jest zakłócany przez modyfikacje chemiczne białka docelowego. 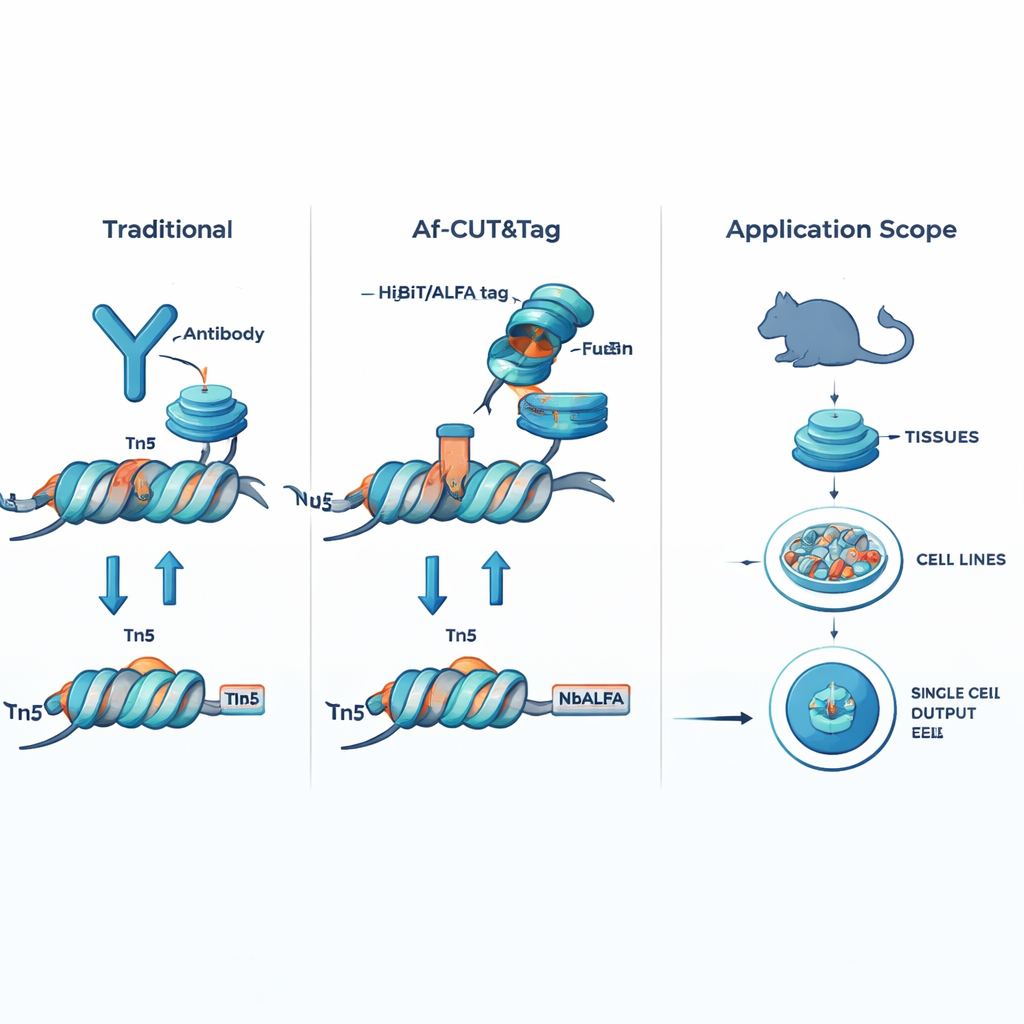
Bardziej wyraźne mapy z mniejszej liczby komórek
Zespół najpierw wykazał, że ich fuzy wiążący–Tn5 nadal bardzo mocno chwytają znaczniki i efektywnie tną DNA. Następnie porównali Af-CUT&Tag ze współczesnymi metodami opartymi na przeciwciałach do mapowania polimerazy RNA II, enzymu czytającego geny kodujące białka, oraz białka CTCF, kluczowego organizatora struktury genomu. W liniach komórkowych pochodzenia ludzkiego Af-CUT&Tag wykazywał czystszy sygnał przy punktach startu genów, mniej niecelowych cięć w otwartych, lecz nieistotnych regionach DNA oraz biblioteki sekwencyjne wyższej jakości. Co godne uwagi, generował solidne mapy z zaledwie około 500 komórek, a ta sama strategia mogła być dostosowana do wielu różnych wiążących celujących w odrębne cechy DNA. Metodę rozszerzono też na pojedyncze komórki przez znakowanie (barcoding) fragmentów pochodzących z każdej komórki, co pozwoliło zbudować szczegółowe, komórka po komórce mapy chromatyny.
Śledzenie naprawy wątroby na żywo
Aby pokazać, co ta technologia może ujawnić w żywych organizmach, autorzy zastosowali Af-CUT&Tag do regeneracji wątroby myszy. Użyli wirusów i CRISPR, aby dodać znaczniki HiBiT do dwóch kluczowych regulatorów szlaku Hippo, YAP1 i TAZ, które pomagają kontrolować rozmiar narządu i naprawę. Po chirurgicznym usunięciu części wątroby izolowali jądra komórek wątrobowych przed operacją i 24 godziny po niej, a następnie użyli Af-CUT&Tag, by zobaczyć, gdzie YAP1 i TAZ wiązały się w genomie. Mapy pokazały, że wczesnie po urazie te białka zmniejszają obecność przy genach napędzających przetwarzanie i syntezę tłuszczów, podczas gdy komórki wątroby tymczasowo gromadzą krople tłuszczu. Jednocześnie YAP1/TAZ zwiększają wiązanie przy genach zaangażowanych w usuwanie hemu, potencjalnie toksycznego składnika krwi, oraz przy Mir122, genie produkującym mikroRNA silnie wzbogacone w wątrobie.
miR-122 jako strażnik regeneracji
miR-122 to drobna cząsteczka RNA, która pomaga precyzyjnie regulować aktywność wielu innych genów. Dzięki Af-CUT&Tag badacze zaobserwowali silniejsze wiązanie YAP1/TAZ w pobliżu regionu Mir122, wraz z bardziej otwartą chromatyną i nasilonymi chemicznymi znakami związanymi z aktywacją genów. Eksperymenty potwierdziły, że poziomy miR-122 rosną w trakcie wczesnego okna regeneracyjnego. Gdy zespół specyficznie usunął miR-122 w komórkach wątroby myszy, zwierzęta wykazywały większe gromadzenie tłuszczu, silniejsze odpowiedzi zapalne i mniej komórek wątrobowych wchodzących w cykl komórkowy po operacji. Łącznie te wyniki sugerują, że YAP1/TAZ pomagają wątrobie utrzymać ostrożną równowagę podczas naprawy: krótkotrwale magazynując tłuszcz jako źródło energii, ograniczając uszkodzenia związane z hemem i stanem zapalnym oraz wykorzystując miR-122 do tłumienia nadmiernego stresu przy jednoczesnym promowaniu odrostu tkanki. 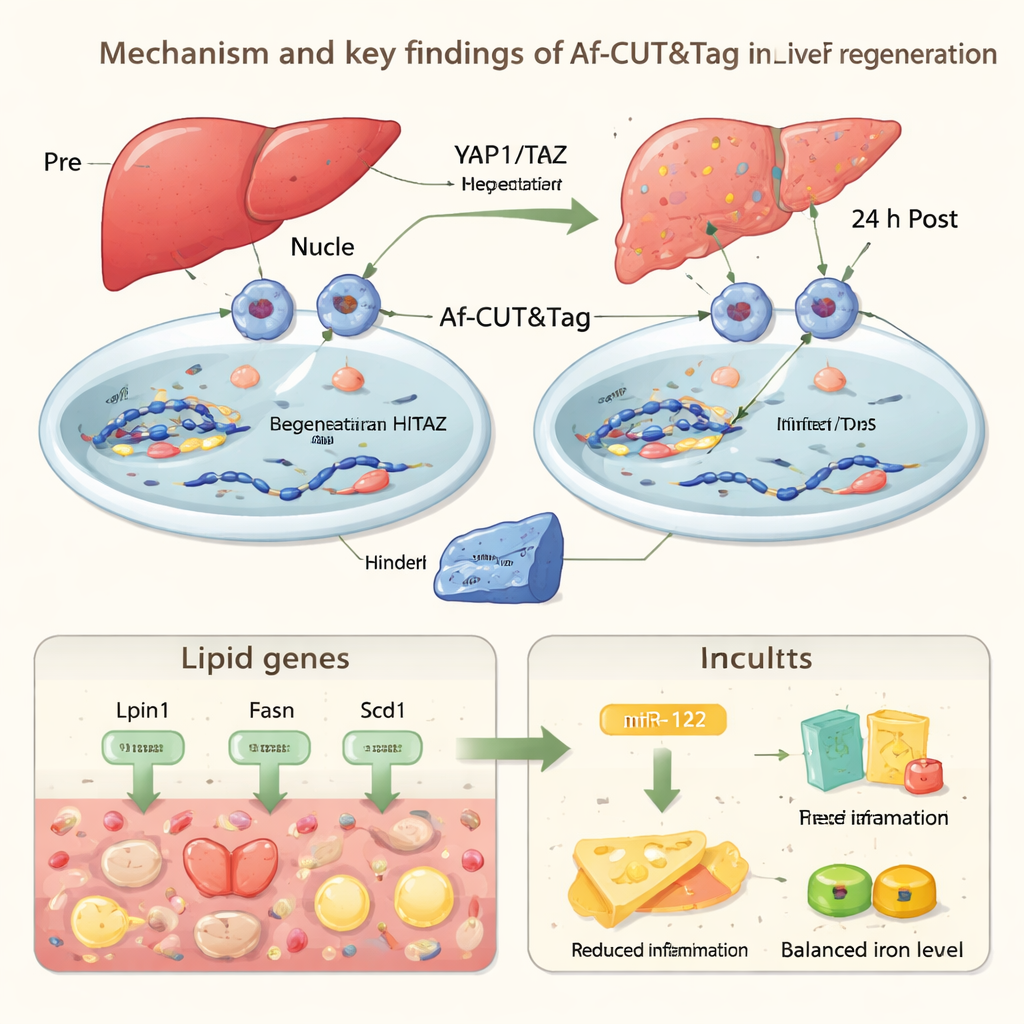
Wszechstronna nowa soczewka na kontrolę genów
Af-CUT&Tag oferuje modułowy, pozbawiony przeciwciał sposób zobaczenia, gdzie kluczowe białka siedzą na DNA w liniach komórkowych, tkankach, a nawet pojedynczych komórkach. Zastępując nieprzewidywalne przeciwciała małymi znacznikami genetycznymi i zaprojektowanymi wiążącymi, zapewnia ostrzejsze, bardziej powtarzalne mapy z dużo mniejszej liczby komórek. Zastosowany do regeneracji wątroby ujawnił, jak YAP1 i TAZ koordynują metabolizm, gospodarkę żelazem i mikroRNA miR-122, by wspierać wczesną naprawę. W miarę jak edycja genomu i projektowane wiążące będą się doskonalić, ta strategia może stać się standardowym narzędziem do rozkładania na czynniki pierwsze, jak regulacja genów przebiega prawidłowo w rozwoju i regeneracji — i jak zawodzi w chorobach, takich jak nowotwór czy niewydolność wątroby.
Cytowanie: Wang, X., Deng, X., Qiu, L. et al. Af-CUT&Tag: a sensitive and antibody-free chromatin profiling method using genetically encoded tags and high-affinity binders fused to Tn5. Nat Commun 17, 1746 (2026). https://doi.org/10.1038/s41467-026-68454-9
Słowa kluczowe: profilowanie chromatyny, epigenetyka, regeneracja wątroby, YAP1 TAZ, microRNA-122