Clear Sky Science · pl
Funkcjonalne warianty w 1p36.23 zwiększają ryzyko schizofrenii poprzez modulację RERE
Dlaczego drobne zmiany w DNA mają znaczenie dla zdrowia psychicznego
Schizofrenia to poważne zaburzenie psychiczne, które wpływa na sposób myślenia, odczuwania i relacji z innymi. Choroba ta silnie występuje w rodzinach, lecz większość zaangażowanych zmian genetycznych to niewielkie, rozproszone modyfikacje w naszym DNA. To badanie przygląda się dokładnie jednemu takiemu rejonowi genomu i pokazuje krok po kroku, jak dwa subtelne warianty DNA mogą zmieniać rozwój i komunikację komórek mózgu w sposób, który może zwiększać ryzyko wystąpienia schizofrenii. 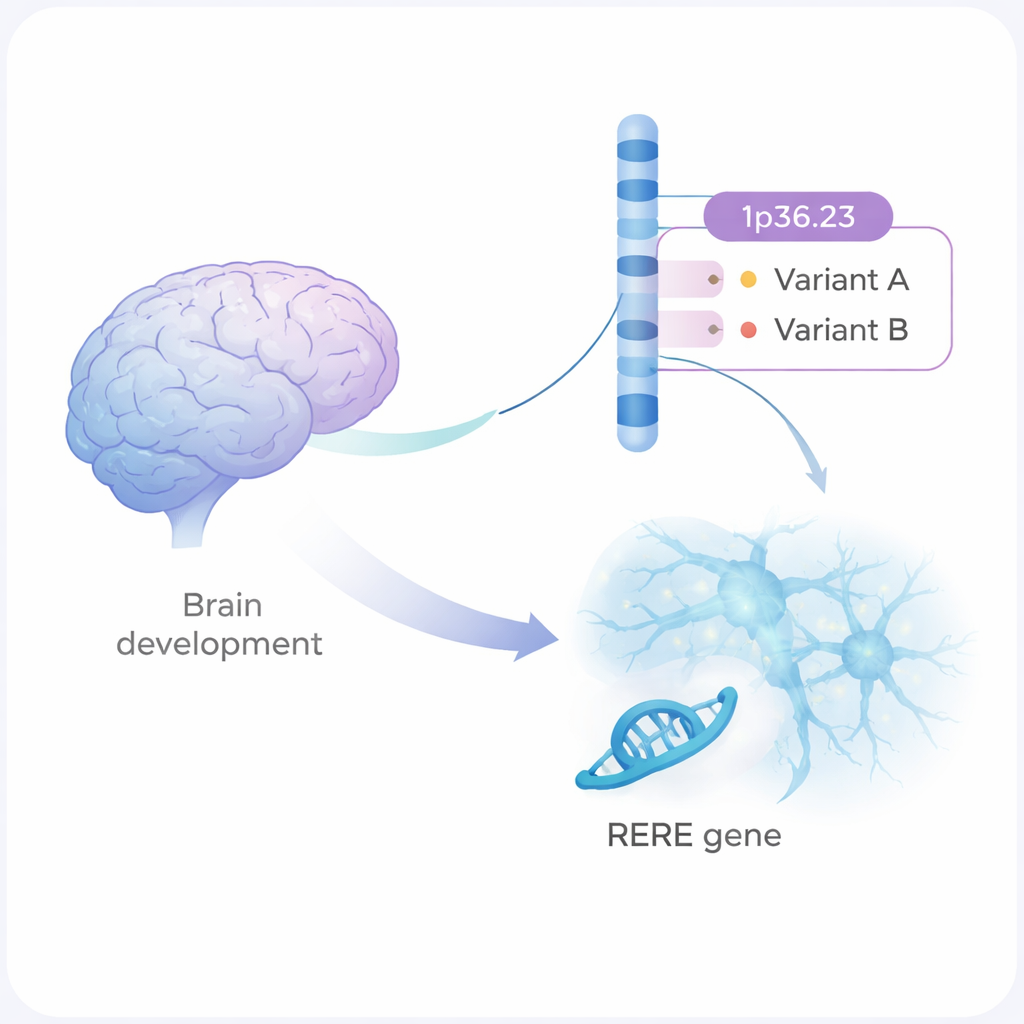
Genetyczne „ognisko” na chromosomie 1
Duże badania genetyczne wskazały ponad 300 rejonów ludzkiego genomu powiązanych ze schizofrenią. Jednym z nich jest odcinek DNA na chromosomie 1, oznaczony jako 1p36.23. Do tej pory naukowcy nie wiedzieli, które dokładne zmiany w tym rejonie ani który gen odpowiadają za rzeczywisty efekt. Autorzy połączyli analizy statystyczne z eksperymentami laboratoryjnymi i wytypowali dwa warianty DNA, nazwane rs159961 i rs301792, znajdujące się wewnątrz genu RERE. Te warianty nie zmieniają samego białka RERE; lokują się natomiast w regulacyjnych „przełącznikach” wewnątrz genu, które kontrolują, jak silnie RERE jest aktywowany.
Jak warianty ryzyka podkręcają aktywność RERE
Zespół najpierw sprawdził, czy te dwa warianty faktycznie działają jako funkcjonalne przełączniki. W testach reporterowych — eksperymentach, w których fragment DNA napędza gen produkujący światło — wykazano, że wersje powiązane ze schizofrenią rs159961 i rs301792 zachowują się jak silniejsze enhancery (wzmacniacze) w komórkach o cechach nerwowych, lecz nie w innych typach komórek. Biochemiczne testy wiązania ujawniły przyczynę: ryzykowna forma jednego wariantu osłabia wiązanie REST, białka, które zwykle tłumi aktywność genów, podczas gdy ryzykowna forma drugiego wzmacnia wiązanie POLR2A, kluczowego elementu mechanizmu transkrypcji. Razem te zmiany w wiązaniu białek zwiększają aktywność segmentów enhancera i podnoszą ekspresję RERE.
Od podwyższonego RERE do zmienionego wzrostu komórek mózgowych
Następnie badacze zastanawiali się, co nadmiar RERE robi w obrębie mózgu. Stwierdzili, że osoby zmarłe ze schizofrenią miały wyższy poziom RERE w tkance mózgowej w porównaniu z osobami bez choroby. Aby to zamodelować, sztucznie zwiększono poziom RERE w mysich komórkach macierzystych nerwowych — niedojrzałych komórkach dających początek neuronom i glejowi. Przy nadprodukcji RERE komórki te dzieliły się mniej, zatrzymywały się w późnej fazie cyklu komórkowego i wytwarzały mniej dojrzałych neuronów, podczas gdy inne typy komórek pozostawały w dużej mierze niezmienione. W hodowlach neuronów nadmiar RERE zmienił ich wzorce rozgałęzień i zmniejszył liczbę oraz rodzaj drobnych wypustek zwanych kolcami dendrytycznymi, które są miejscami tworzenia synaps. Te zmiany pasują do długotrwałych dowodów, że schizofrenia wiąże się z zaburzonym rozwojem mózgu i utratą kolców. 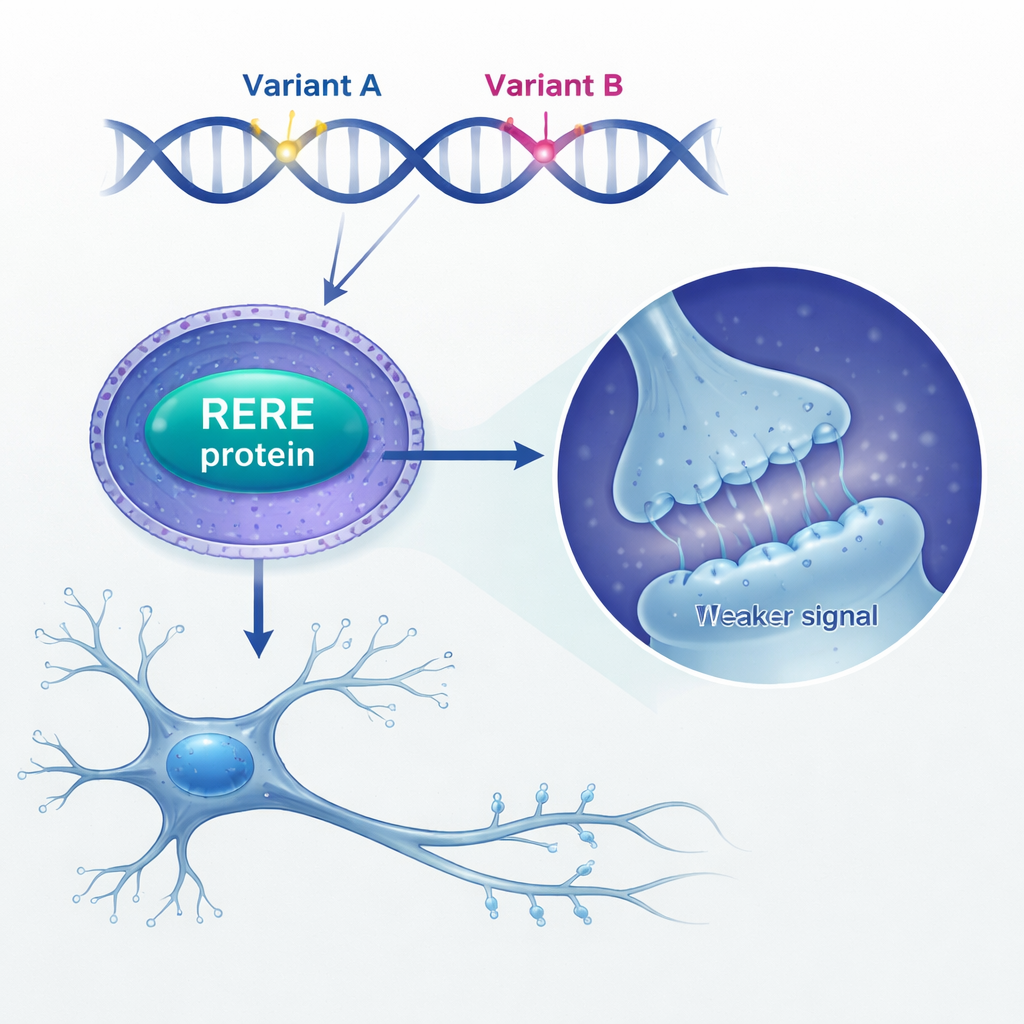
Zakłócenie „rozmowy” glutaminianowej w mózgu
Przy bliższej analizie aktywności genów zespół odkrył, że nadekspresja RERE zaburza sieci genów zaangażowanych w wzrost dendrytów i główne systemy sygnalizacyjne, zwłaszcza szlak glutaminianowy. Wyróżniał się jeden kluczowy cel: gen GRIN2A, kodujący istotną podjednostkę (GluN2A) receptorów NMDA dla glutaminianu, od dawna powiązanych ze schizofrenią. Autorzy wykazali, że RERE współdziała z dwoma innymi białkami jądrowymi, RARB i RXRA, aby bezpośrednio wiązać się z promotorem GRIN2A i osłabiać jego aktywność. W neuronach z nadmiarem RERE poziomy GluN2A spadły, a zapisy elektrofizjologiczne ujawniły słabsze prądy synaptyczne zależne od receptorów NMDA, mimo że częstotliwość zdarzeń synaptycznych nie uległa zmianie. Innymi słowy, „głośność” poszczególnych sygnałów pobudzających została przyciszona.
Powiązanie wariantów DNA z funkcją mózgu
Łącząc genetykę, biologię molekularną, hodowle komórkowe i elektrofizjologię, praca ta przedstawia jasny łańcuch przyczynowy: warianty DNA ryzyka w 1p36.23 wzmacniają elementy regulacyjne wewnątrz genu RERE, co prowadzi do wyższej ekspresji RERE w komórkach mózgu. Podwyższony poziom RERE z kolei upośledza wzrost i dojrzewanie neuronów, zmienia kształt i liczbę ich kolców synaptycznych oraz osłabia sygnalizację glutaminianową za pośrednictwem receptorów NMDA — szczególnie tych zawierających GluN2A. Dla czytelnika nieznającego tematu kluczowe przesłanie jest takie: bardzo małe zmiany w DNA mogą nieznacznie przesunąć aktywność jednego genu, a w skali wielu komórek mózgowych i wielu lat może to stopniowo wypaczyć rozwój i komunikację mózgu w sposób sprzyjający schizofrenii.
Cytowanie: Liu, Y., Wang, J., Yang, H. et al. Functional variants at 1p36.23 confer risk of schizophrenia through modulating RERE. Nat Commun 17, 1742 (2026). https://doi.org/10.1038/s41467-026-68449-6
Słowa kluczowe: genetyka schizofrenii, gen RERE, neurogeneza, sygnalizacja glutaminianowa, funkcja synaps