Clear Sky Science · pl
Poprawa funkcji erekcji u diabetycznych samców myszy przez przywrócenie zdepalmitoylowanego FBP1 w celu zmniejszenia stężenia mleczanu w ciałach jamistych
Dlaczego to ma znaczenie dla mężczyzn z cukrzycą
Problemy z erekcją są częste u mężczyzn z cukrzycą, często pojawiają się wcześniej i słabo reagują na standardowe leki, takie jak Viagra. To badanie na myszach ujawnia zaskakującego winowajcę: nagromadzenie kwasu mlekowego (mleczanu) w tkance erekcyjnej prącia. Naukowcy nie tylko śledzą, jak to nagromadzenie uszkadza tkankę, ale także testują eksperymentalną terapię opartą na RNA dostarczaną w małych lipidowych pęcherzykach, która przywraca funkcję erekcji. Ich praca sugeruje przyszłość, w której leczenie cukrzycowej dysfunkcji erekcyjnej oznacza naprawę podstawowego metabolizmu, a nie tylko tymczasowe zwiększanie przepływu krwi.
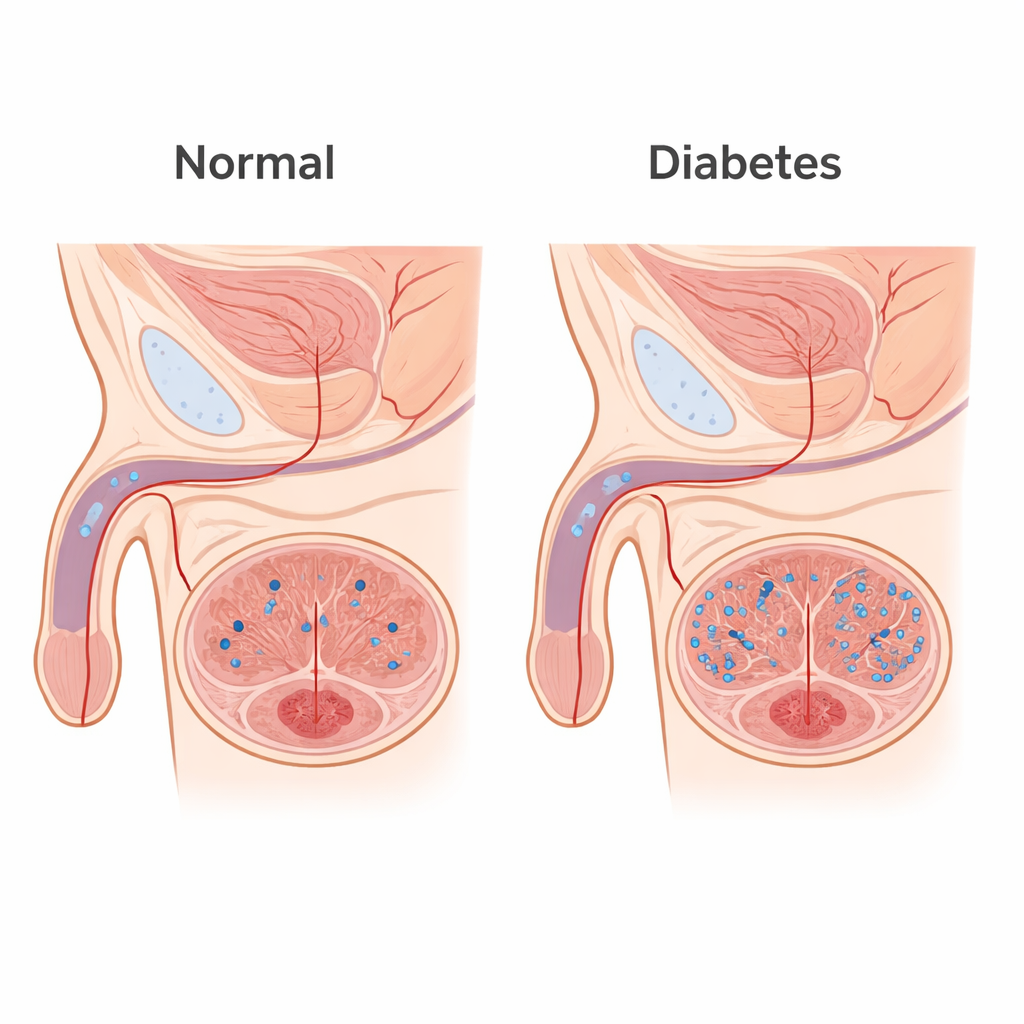
Od marnotrawstwa energii do uszkodzenia tkanki
Mleczan bywa postrzegany jako prosty „odpad” po intensywnej pracy mięśni, ale jest też silnym molekularnym sygnałem. U mężczyzn z cukrzycową dysfunkcją erekcyjną autorzy wykryli wyższe stężenia mleczanu we krwi niż u rówieśników bez cukrzycy. W modelu myszy z cukrzycą mleczan w gąbczastej tkance erekcyjnej prącia (ciało jamiste) stopniowo wzrastał w czasie, podczas gdy ciśnienie generowane podczas erekcji malało. Gdy zdrowym myszom podawano dodatkowy mleczan, ich tkanka prącia akumulowała mleczan, spadało ciśnienie erekcyjne, a badania mikroskopowe wykazywały ubytek mięśnia gładkiego i wzrost bliznowatej tkanki kolagenowej. W hodowlach komórek mięśnia gładkiego pochodzących z prącia wysoki poziom mleczanu spowalniał migrację komórek i przestawiał je z kurczliwej, „gotowej do pracy” formy na syntetyczną, tworzącą blizny, częściowo poprzez nadaktywację szlaków autodigestii znanych jako autofagia.
Kluczowy enzym znika
Aby zrozumieć przyczynę nagromadzenia mleczanu, zespół porównał geny zaangażowane w dwa przeciwstawne szlaki energetyczne: glikolizę, która produkuje mleczan, oraz glukoneogenezę, która przekształca mleczan z powrotem w glukozę. Nie zaobserwowano oznak nadaktywnej glikolizy. Zamiast tego centralny enzym glukoneogenezy o nazwie FBP1 był konsekwentnie obniżony w tkance prącia myszy cukrzyczych, szczurów cukrzyczych oraz w danych pojedynczych komórek od mężczyzn z cukrzycową dysfunkcją erekcyjną. Gdy naukowcy genetycznie obniżyli poziom Fbp1 u myszy, mleczan w prąciu wzrósł, a wydajność erekcyjna pogorszyła się, nawet przy stosunkowo niskich poziomach mleczanu. W komórkach mięśnia gładkiego przywrócenie aktywnego FBP1 chroniło przed szkodliwymi efektami wysokiego mleczanu, podczas gdy nieaktywna warianta FBP1 tego nie robiła. To wykazało, że aktywność enzymatyczna FBP1 jest kluczowa dla kontrolowania poziomu mleczanu i utrzymania zdrowej tkanki erekcyjnej.
Epigenetyczne blokady i tłuszczowe „znaczki” na FBP1
Dlaczego FBP1 jest zmniejszony w cukrzycy? Badanie ujawnia dwuetapowy system kontroli. Po pierwsze, gen Fbp1 jest przygłuszony na poziomie DNA. Chemiczne oznaczenia na białkach histonowych — konkretnie dwa „wyłączające” przełączniki H3K9me3 i H3K27me3 — kumulują się w promotorze Fbp1 w cukrzycowej tkance prącia. Znaki te są zapisywane przez enzymy takie jak SUV39H1 i EZH2 i odczytywane przez białko CBX3, tworząc represyjny kompleks, który utrzymuje Fbp1 wyłączony. Leki i projektowane degradery celujące w te enzymy częściowo zdjąć tę represję w komórkach, lecz dały jedynie umiarkowaną poprawę u myszy cukrzyczych. Po drugie, nawet gdy białko FBP1 jest obecne, może być unieruchomione przez tłuszczową modyfikację nazwaną palmitoylacją na pojedynczym aminokwasie, Cys282. Zespół zidentyfikował enzym ZDHHC13 jako palmitoilotransferazę, która przyłącza tę grupę tłuszczową. Palmitoylacja subtelnie zmienia kształt FBP1 w pobliżu krytycznego resztu, osłabiając jego zdolność do przetwarzania mleczanu. Blokowanie Zdhhc13 w komórkach i myszy nieznacznie poprawiło metabolizm i funkcję erekcyjną, co podkreśla, że ani leki epigenetyczne, ani inhibitory palmitoylacji same w sobie nie wystarczą.
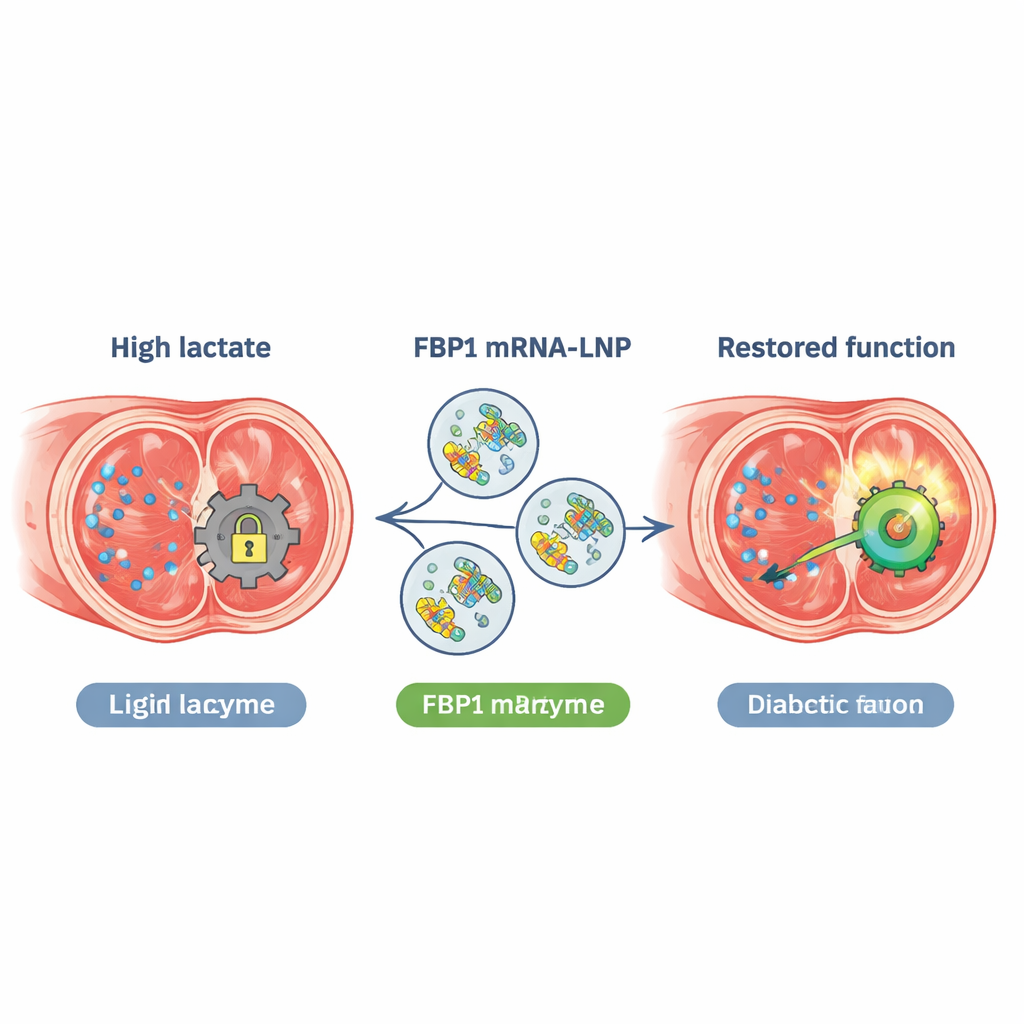
Nanocząstki wypełnione RNA jako zestaw naprawczy
Aby rozwiązać oba problemy jednocześnie, naukowcy zaprojektowali mRNA kodujące wariant Fbp1 oporny na palmitoylację (C282S) i zapakowali go w nanocząstki lipidowe — podobne w duchu do szczepionek mRNA przeciw COVID-19. Wstrzyknięte bezpośrednio do tkanki prącia myszy cukrzyczych, cząstki te były efektywnie pobierane przez komórki mięśnia gładkiego. Leczone myszy wykazywały wyższe poziomy białka FBP1, wyraźnie niższy mleczan w ciałach jamistych, lepsze ciśnienie erekcyjne, więcej mięśnia gładkiego i mniej włóknienia. Dawka umiarkowana działała najlepiej; większe dawki nie przynosiły dodatkowych korzyści. Terapia także normalizowała nadaktywną autofagię obserwowaną w modelach cukrzycy i poprawiła wyniki erekcyjne w różnych typach myszy cukrzyczych, bez wyraźnej toksyczności wątroby czy nerek w okresie badania.
Co to może znaczyć dla przyszłych terapii
Mówiąc prosto, ta praca przekształca problem trudnych erekcji w cukrzycy w problem „kwaśnego” metabolizmu wewnątrz prącia: za dużo mleczanu i zbyt mało funkcjonalnego FBP1. Przywracając niepalmitoylowaną, aktywną wersję FBP1 dokładnie tam, gdzie jest potrzebna, terapia mRNA w nanocząstkach naprawia równowagę energetyczną tkanki, chroni mięsień gładki i pozwala na powrót normalnych erekcji — przynajmniej u myszy. Choć wciąż pozostaje wiele pytań o długoterminowe bezpieczeństwo, dawkowanie i przełożenie na ludzi, badanie wskazuje na nową klasę terapii, które odbudowują metaboliczne zdrowie tkanki erekcyjnej i mogą pewnego dnia uzupełniać lub pomóc pacjentom, którzy nie reagują na obecne leki.
Cytowanie: Xiao, M., Guo, W., Zeng, R. et al. Improving erectile function in diabetic male mice by rescuing depalmitoylated FBP1 to reduce cavernosal lactate. Nat Commun 17, 1740 (2026). https://doi.org/10.1038/s41467-026-68443-y
Słowa kluczowe: cukrzycowa dysfunkcja errekcyjna, metabolizm mleczanu, enzym FBP1, terapia mRNA w nanocząstkach lipidowych, gładkie mięśnie prącia