Clear Sky Science · pl
Udoskonalone in vivo wyciszanie genów o wysokiej specyficzności przy użyciu zmultipleksowanych sgRNA Cas12a
Modyfikowanie genów z większą pewnością
Edycja genów obiecuje nowe sposoby badania biologii, leczenia chorób, a nawet kontroli szkodników owadzich, ale w rzeczywistych organizmach często działa mniej czysto, niż sugerują nagłówki. Wiele komórek unika edycji lub zostaje jedynie częściowo zmienionych, co może zamazywać wyniki eksperymentów i ograniczać zastosowania w praktyce. W tym artykule opisano nową metodę opartą na CRISPR w muszkach owocowych, która sprawia, że wyciszania genów są bardziej kompletne i bardziej precyzyjne, oferując wzorzec dla bardziej niezawodnej edycji genomu w złożonych organizmach.
Dlaczego standardowy CRISPR często zawodzi
Tradycyjne narzędzia CRISPR, takie jak Cas9, przecinają DNA w wybranym miejscu używając pojedynczego lub niewielkiej liczby przewodników RNA. W żywych organizmach podejście to napotyka kilka przeszkód. Niektóre przewodniki po prostu działają słabo; niektóre miejsca docelowe są trudne do osiągnięcia dla enzymu; a mechanizmy naprawcze komórki często „naprawiają” przerwę niewielkimi zmianami, które pozostawiają gen wciąż funkcjonalnym. Efektem jest mozaika: sąsiadujące komórki w tym samym tkance mogą mieć różne mutacje albo wcale ich nie mieć. Ta nierównomierność utrudnia ocenę skutków prawdziwego wyłączenia genu i stanowi wyzwanie dla zastosowań, takich jak terapia genowa czy systemy napędu genowego, które muszą działać wydajnie w większości komórek.
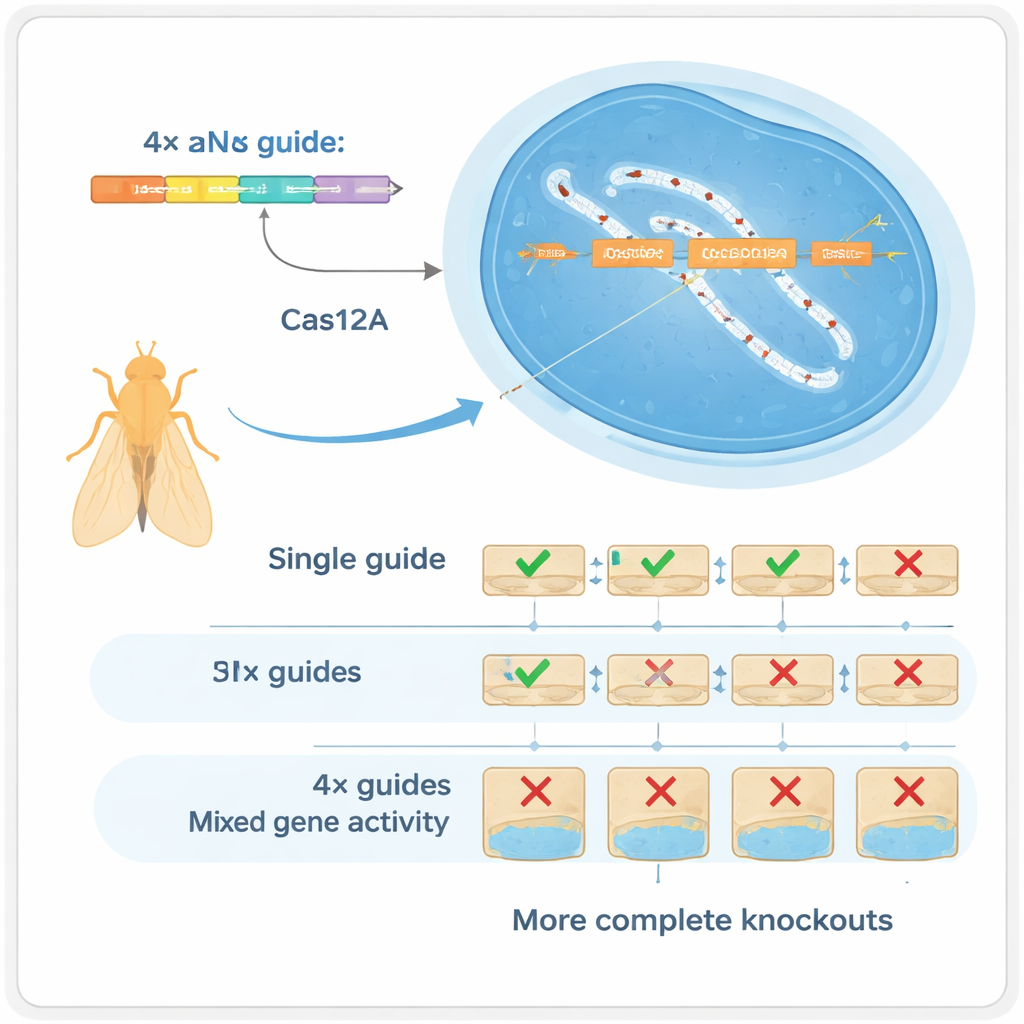
Cztery przewodniki zamiast jednego
Autorzy sięgnęli po inny enzym CRISPR, Cas12a, który znacznie łatwiej przetwarza zwarte szeregi przewodników niż Cas9. Zbudowali narzędziownik dla Drosophila, w którym każdy gen jest celowany przez szereg czterech przewodników RNA, wszystkie zakodowane na jednym małym fragmencie DNA, który można masowo produkować. W starannie kontrolowanych testach wykazali, że użycie czterech przewodników na gen dramatycznie zmienia rodzaje powstających zmian w DNA: zamiast przeważnie drobnych insercji lub delecji w jednym miejscu, system często generuje większe delecje między miejscami cięć, które niemal zawsze niszczą funkcję genu. Ta „multipleksacja” działa na dwa sposoby: jeśli jeden przewodnik zawiedzie, inne mogą wykonać zadanie (nadmiarowość), a gdy kilka przecięć występuje jednocześnie, mogą usunąć większe fragmenty genu (synergia).
Wysoka wydajność bez dodatkowych efektów ubocznych
Wywoływanie większej liczby przerwań w DNA rodzi oczywiste pytania o bezpieczeństwo. Czy wiele cięć w jednym regionie może przypadkowo wymazać pobliskie geny? Czy przewodniki częściej będą działać poza celem w innych miejscach genomu? Aby to zbadać, badacze mierzyli śmierć komórek, analizowali wpływ na sąsiednie geny i opracowali sprytne badanie do wizualizacji zdarzeń naprawy chromosomów zwane utratą heterozygotyczności na dużych odcinkach DNA. Stwierdzili, że skupienie czterech cięć w obrębie jednego genu było dobrze tolerowane: nie zwiększało śmierci komórek w porównaniu z konwencjonalnymi podejściami Cas9 i rzadko zaburzało sąsiednie geny, chyba że przewodnik trafił bardzo blisko elementu regulatorowego. Badania przesiewowe na dużą skalę z wykorzystaniem ponad 2000 przewodników obejmujących jedną trzecią genomu muszki wykazały, że ponad 99% układów przewodników było aktywnych w zamierzonym miejscu, podczas gdy powtarzalna aktywność poza celem wynosiła poniżej 1%, co wskazuje na bardzo wysoką specyficzność nawet w konfiguracji multipleksowanej.
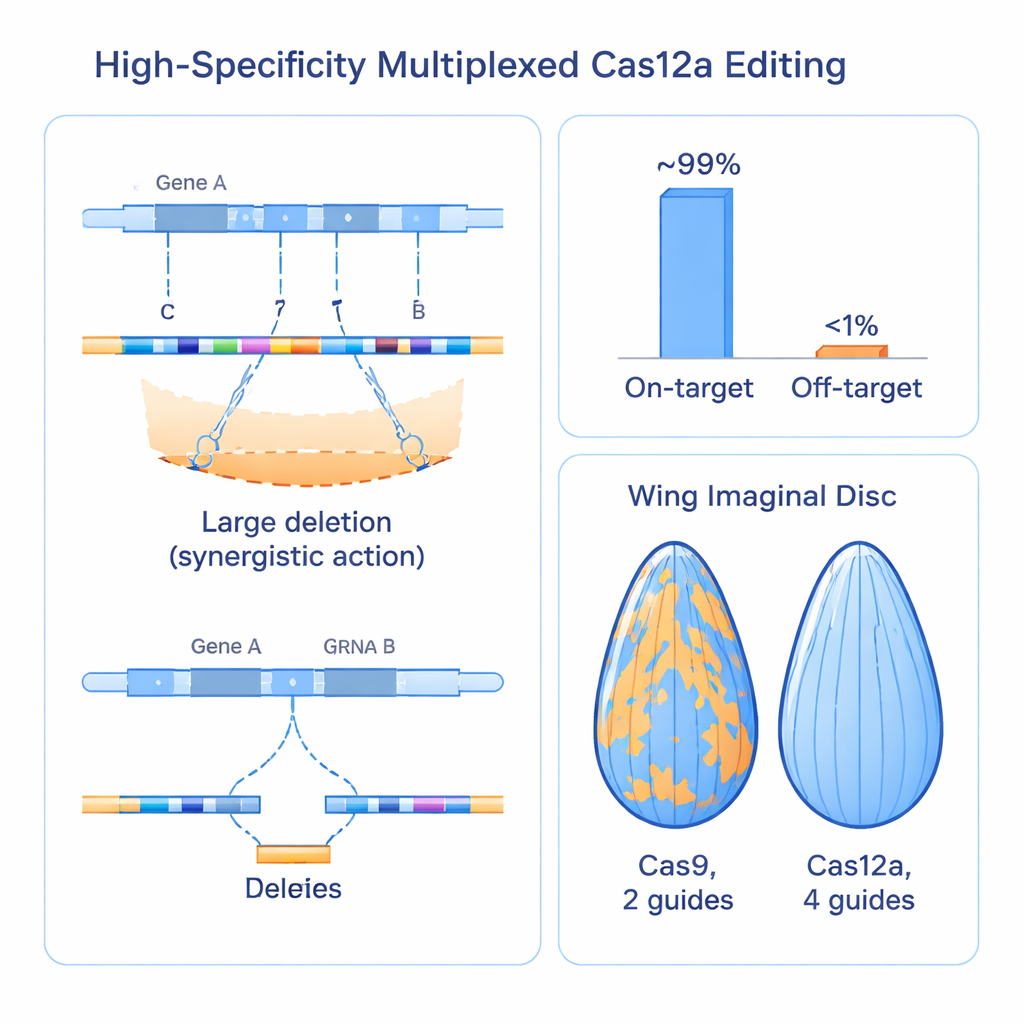
Przewyższając ustalone systemy Cas9 w rzeczywistych tkankach
Aby sprawdzić, czy te molekularne usprawnienia przekładają się na wyraźniejszą biologię, zespół porównał swój system Cas12a z czterema przewodnikami bezpośrednio z powszechnie używanymi zasobami opartymi na Cas9, celując w ponad 100 genów u muszki. W tkankach takich jak oko, jelito i rozwijające się skrzydło, podejście Cas12a dało silniejsze i bardziej jednorodne efekty utraty funkcji niż Cas9, który często pozostawiał widoczne pola nieedytowanej, normalnej tkanki. Kiedy użyto wielkości skrzydła jako ilościowego wskaźnika, nowy system konsekwentnie generował większe i bardziej powtarzalne defekty wzrostu dla znanych regulatorów, ujawniając, że niektóre geny wcześniej ocenione jako słabe lub nieistotne w rzeczywistości były pomijane, ponieważ starsze narzędzia nie inaktywowały ich wystarczająco gruntownie. Zwiększona siła metody odsłoniła nawet wcześniej nieznaną, istotną rolę genu nazwanego trade embargo w rozwoju skrzydła i przeżywalności.
Co to oznacza dla przyszłej edycji genów
Mówiąc wprost, ta praca pokazuje, jak przekształcić CRISPR z czasem nieporęcznego skalpela w bardziej stanowczy przełącznik wyłączający geny w żywych organizmach. Łącząc Cas12a z czterema przewodnikami na gen, autorzy osiągają niemal kompletne knockouty z bardzo niskim odsetkiem niezamierzonych efektów, wszystko w formacie praktycznym do skalowania na setki genów. Chociaż opracowano to w muszkach owocowych, leżące u podstaw zasady — użycie wielu przewodników dla nadmiarowości i synergii oraz staranna kontrola efektów ubocznych na chromosomy — mają szerokie zastosowanie. Ta strategia może usprawnić badania podstawowe, wyostrzyć przesiewy genetyczne i pomóc w projektowaniu bezpieczniejszych rozwiązań dla przyszłych medycznych i ekologicznych zastosowań edycji genów.
Cytowanie: Port, F., Buhmann, M.A., Zhou, J. et al. Improved in vivo gene knockout with high specificity using multiplexed Cas12a sgRNAs. Nat Commun 17, 877 (2026). https://doi.org/10.1038/s41467-026-68434-z
Słowa kluczowe: CRISPR, Cas12a, wyciszanie genów, Drosophila, specyficzność edycji genomu