Clear Sky Science · pl
Kontrola rekrutacji telomerazy i ochrony końców przez niezależne składniki shelterin
Jak komórki chronią końce chromosomów
Przy każdym podziale komórki bardzo końcowe fragmenty jej chromosomów — zwane telomerami — ulegają nieznacznemu skróceniu. Aby nie utracić istotnej informacji genetycznej, komórki wykorzystują specjalny enzym, telomerazę, oraz zestaw białek ochronnych do utrzymania tych końców. W pracy tej badacze analizują, jak dwa z tych białek, TPP1 i POT1, zarządzają delikatną równowagą między dopuszczaniem telomerazy do odbudowy telomerów a utrzymaniem końców chromosomów w stanie zabezpieczenia przed uszkodzeniem.
Problem starzejących się końców chromosomów
Telomery działają jak plastikowe końcówki sznurowadeł, zapobiegając strzępieniu się chromosomów lub ich błędnemu rozpoznaniu jako uszkodzonego DNA. Jeśli komórka pomyli koniec chromosomu z uszkodzeniem, może uruchomić systemy naprawcze, które sklejają chromosomy lub zatrzymują podziały komórkowe. Jednocześnie telomery muszą się od czasu do czasu otwierać, aby telomeraza mogła je wydłużyć, zwłaszcza w komórkach macierzystych dzielących się wielokrotnie. Biolodzy od dawna wyobrażali sobie telomery przełączające się między „zamkniętym” stanem chronionym a „otwartym” stanem umożliwiającym dostęp telomerazy, lecz niosącym ryzyko tymczasowych sygnałów uszkodzenia. Pytanie, czy te dwa stany odzwierciedlają różne kształty fizyczne telomeru, czy też rzeczywiście oddzielne mechanizmy sterujące, pozostawało otwarte.
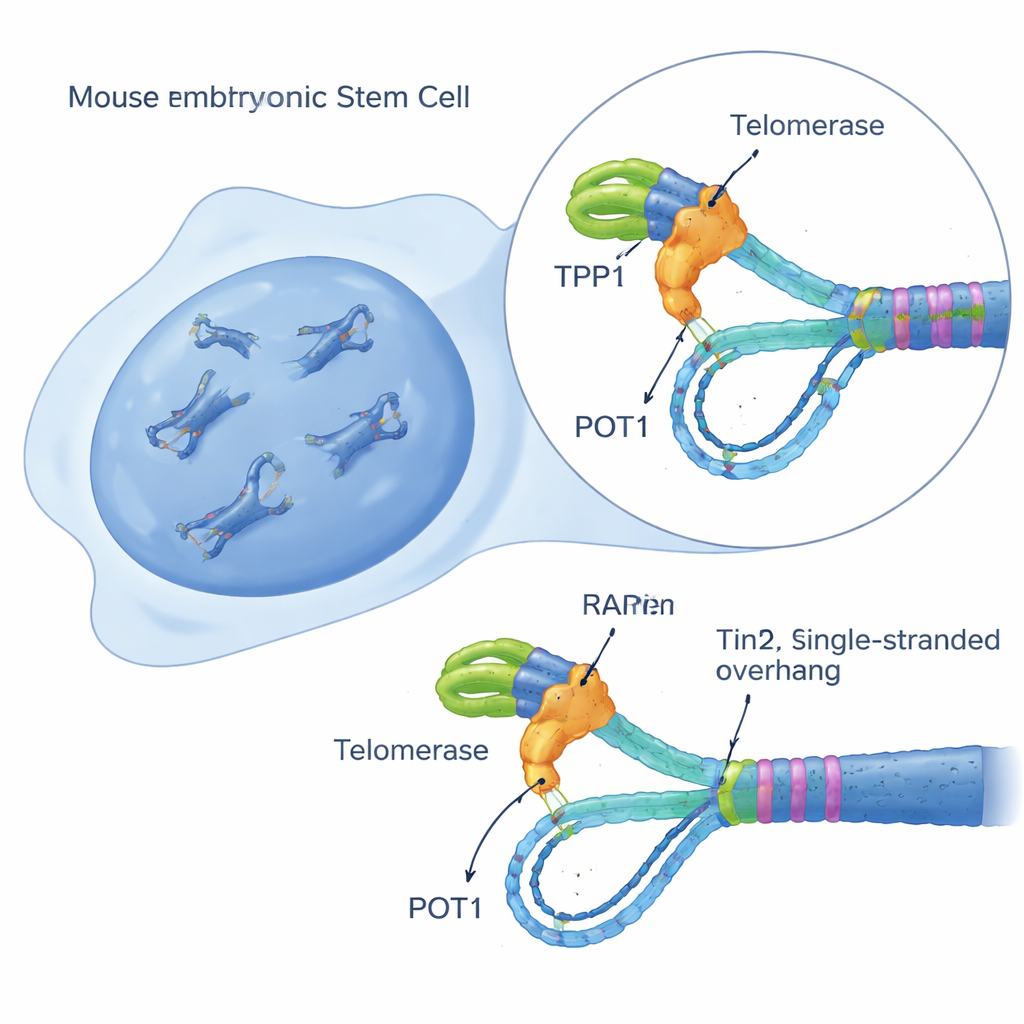
Budowa sensora aktywności telomerazy w pojedynczej komórce
Aby rozplątać tę zagadkę, badacze stworzyli czuły test w żywych komórkach nazwany iTAP (indukowalne Badanie Aktywności Telomerazy) w mysich embrionalnych komórkach macierzystych. Zmodyfikowali komórki tak, by produkowały nieco zmienioną wersję RNA-szkieletu telomerazy tylko po podaniu doksycykliny. Ten „mutantowy” szkielet sprawia, że telomeraza dodaje zmodyfikowaną sekwencję DNA w telomerach, którą można wizualnie odróżnić od normalnego DNA telomerowego. Za pomocą sond fluorescencyjnych, blotów DNA i metody sekwencjonowania wzbogacającej fragmenty telomerowe zespół mógł bezpośrednio obserwować, komórka po komórce, kiedy i gdzie telomeraza była aktywna. Kluczowe było to, że system nie szkodził wzrostowi komórek ani nie wywoływał sam z siebie odpowiedzi na uszkodzenie, co pozwoliło na czyste pomiary zachowania telomerazy w pozornie zdrowych komórkach.
TPP1 przyciąga telomerazę, POT1 ją hamuje
Wykorzystując iTAP, autorzy badali, jak dwa kluczowe białka telomerowe, TPP1 i POT1, wpływają na działanie telomerazy. Oba należą do większego kompleksu zwanego shelterin, który pokrywa telomery. Gdy usunęli TPP1 za pomocą narzędzi edycji genów, mutantowe sekwencje telomerowe niemal zniknęły, mimo że mutantowy RNA telomerazy wciąż był produkowany na normalnym poziomie. Dalsze eksperymenty wykazały, że TPP1 musi fizycznie łączyć się z innym składnikiem shelterin, TIN2, aby rekrutować telomerazę; zakłócenie połączenia TPP1 z TIN2 wyłączyło aktywność telomerazy. Zaskakująco, przerwanie interakcji TPP1 z POT1 nie dawało takiego efektu, a usunięcie samego POT1 nie zmniejszyło działania telomerazy. W rzeczywistości komórki pozbawione POT1 wykazały łagodny wzrost ilości dodanej mutantowej sekwencji, co sugeruje, że POT1 zwykle działa jak hamulec — ograniczając, jak często telomeraza angażuje telomery, zamiast jej pomagać.
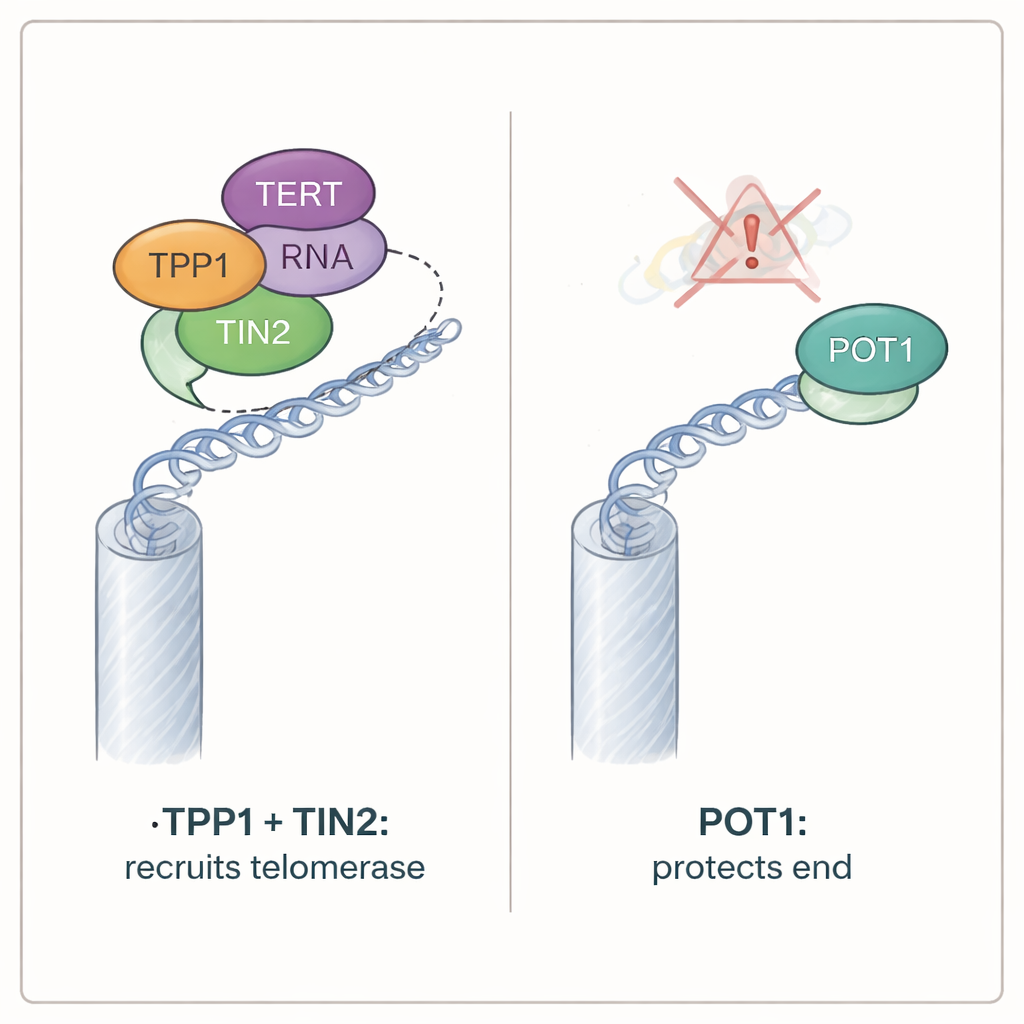
POT1 chroni końce, podczas gdy TPP1 może być niezbędne tylko do rekrutacji
Choć POT1 okazał się niepotrzebny do rekrutacji telomerazy, był kluczowy dla ochrony końców chromosomów. Komórki mysie pozbawione obu form POT1 szybko przestały się dzielić i wykazały wszystkie cechy odsłoniętych telomerów: markery uszkodzeń DNA nagromadziły się na końcach chromosomów, włączono enzym wykrywający uszkodzenia ATR, a końce chromosomów uległy fuzjom. Dla porównania komórki bez TPP1 dalej się namnażały i wykazywały niewiele oznak stresu telomerowego, mimo utraty normalnej aktywności telomerazy. Dodatkowe testy pokazały, że rola obronna POT1 zależy od jego zdolności do wiązania jednoniciowego zwisu telomerowego. Zmutowane białka POT1, które nie potrafiły uchwycić tego odsłoniętego DNA, nie tłumiły sygnałów uszkodzenia, nawet jeśli nadal mogły wchodzić w interakcję z TPP1. Odwrotnie, odmiany POT1 mogące wiązać zwis, ale niełączące się już z TPP1, nadal chroniły końce chromosomów.
Nowe, modułowe spojrzenie na kontrolę telomerów
Te odkrycia obalają prosty obraz telomerów przełączających się między jednym „otwartym” stanem dla telomerazy a jednym „zamkniętym” stanem dla ochrony. Zamiast tego badanie pokazuje, że rekrutacja telomerazy i ochrona końców są kontrolowane przez rozdzielne układy molekularne. TPP1, działając przez TIN2, jest główną bramą przyprowadzającą telomerazę do telomerów, podczas gdy POT1 niezależnie strzeże odsłoniętego DNA na końcach chromosomów i utrzymuje w ryzach odpowiedzi na uszkodzenia. Dla czytelnika niebędącego specjalistą sedno jest takie, że komórki nie polegają na jednym uniwersalnym przełączniku na końcach chromosomów. Zamiast tego używają oddzielnych, lecz skoordynowanych pokręteł — jednego do wpuszczania telomerazy i drugiego do zabezpieczania końców — aby utrzymać stabilność genomu przez całe życie.
Cytowanie: Sandhu, R., Tricola, G.M., Lee, S.Y. et al. Control of telomerase recruitment and end protection by independent shelterin components. Nat Commun 17, 1733 (2026). https://doi.org/10.1038/s41467-026-68433-0
Słowa kluczowe: telomery, telomeraza, komórki macierzyste, uszkodzenia DNA, ochrona chromosomów