Clear Sky Science · pl
Shigella flexneri omija odporność komórkową związaną z septynami dzięki ADP-riboxanacji białek
Jak niektóre bakterie jelitowe wymykają się naszemu wewnętrznemu systemowi ochronnemu
Ciężka biegunka wywoływana przez bakterie Shigella wciąż stanowi poważny problem na całym świecie, szczególnie wśród małych dzieci. Nasze komórki nie są bezbronne: mają wbudowane mechanizmy, które potrafią schwytać i zniszczyć napadające drobnoustroje. Badanie to ujawnia, w jaki sposób Shigella flexneri, czołowy czynnik dyzenterii, wykorzystuje sprytne molekularne sztuczki, by rozmontować jedno z tych narzędzi, ułatwiając rozprzestrzenianie się bakterii z komórki do komórki w jelicie.
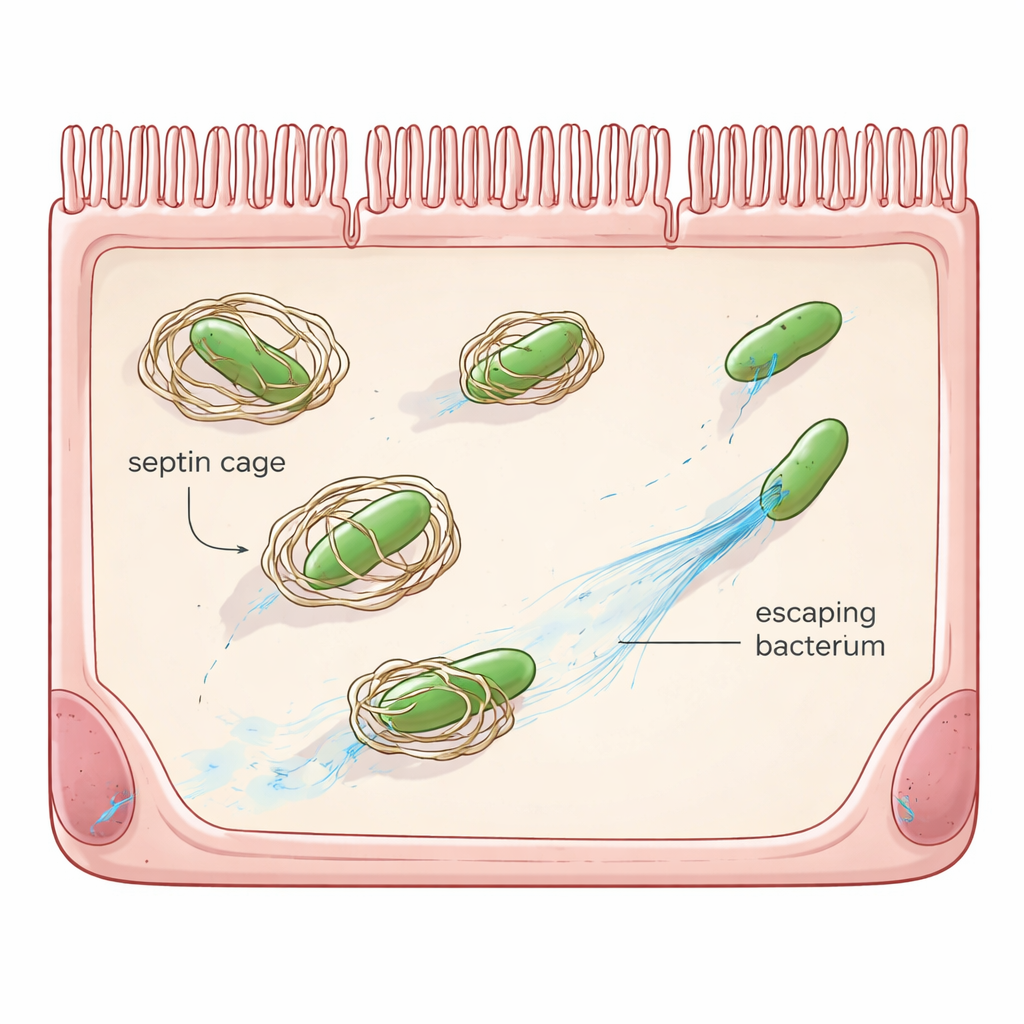
„Zrób to sam” — obrona komórki
Poza leukocytami i przeciwciałami wiele zwykłych komórek posiada własne systemy awaryjne, zwane odpornością komórkową. Jednym z takich systemów są septyny — rodzina białek-szablonów, które tworzą pierścienie i struktury przypominające klatki. Gdy Shigella wnika do komórki i ucieka do galaretowatego wnętrza cytoplazmy, septyny mogą zebrać się wokół bakterii, blokując jej ruch i oznaczając ją do degradacji przez szlaki recyklingu komórkowego. Wcześniejsze prace wykazały, że Shigella ma już jedno przeciwstawne narzędzie, białko OspG, które kieruje septyny na drogę usuwania. Nawet gdy OspG jest nieobecne, większość bakterii nadal unika uwięzienia, co sugeruje, że Shigella dysponuje dodatkowymi sztuczkami.
Demaskowanie drugiego sabotażysty bakterii
Autorzy zwrócili uwagę na inną grupę białek Shigella, zwaną rodziną OspC. Przy użyciu globalnego podejścia mapowania białek w komórkach ludzkich poszukiwali białek gospodarza, które ulegają chemicznej modyfikacji w obecności białek OspC. Obok znanych celów związanych z syntezą białek odkryli, że kilka septyn, w szczególności SEPT9, było konsekwentnie modyfikowanych. Szczegółowe testy biochemiczne wykazały, że trzy białka OspC mogą bezpośrednio przyłączać mały, bogaty w energię znacznik pochodzący z cząsteczki NAD do wielu miejsc w septynach. Ta chemiczna modyfikacja, nazwana ADP-riboxanacją, jest szczególną, nieodwracalną odmianą bardziej powszechnej modyfikacji białek.
Rozrywanie białkowego rusztowania od środka
Aby zrozumieć, jak ten chemiczny znacznik osłabia obronę komórki, zespół skupił się na SEPT9. Septyny zazwyczaj tworzą uporządkowane łańcuchy z ośmiu jednostek, które następnie ustawiają się w filamenty, a w końcu tworzą pełne klatki wokół bakterii. Badacze odkryli, że jedno konkretne miejsce w SEPT9, aminokwas zwany argininą 561, jest głównym miejscem ADP-riboxanacji podczas infekcji. Prace strukturalne i eksperymenty z rekonstrukcją przy użyciu oczyszczonych białek pokazały, że to miejsce leży na krytycznej powierzchni kontaktu, gdzie dwie jednostki SEPT9 się blokują. Gdy ta arginina jest chemicznie zmodyfikowana — lub zastąpiona przez resztę naśladującą dodany ładunek ujemny — oktamerowe łańcuchy rozpadają się na mniejsze fragmenty i nie są już w stanie budować stabilnych filamentów.
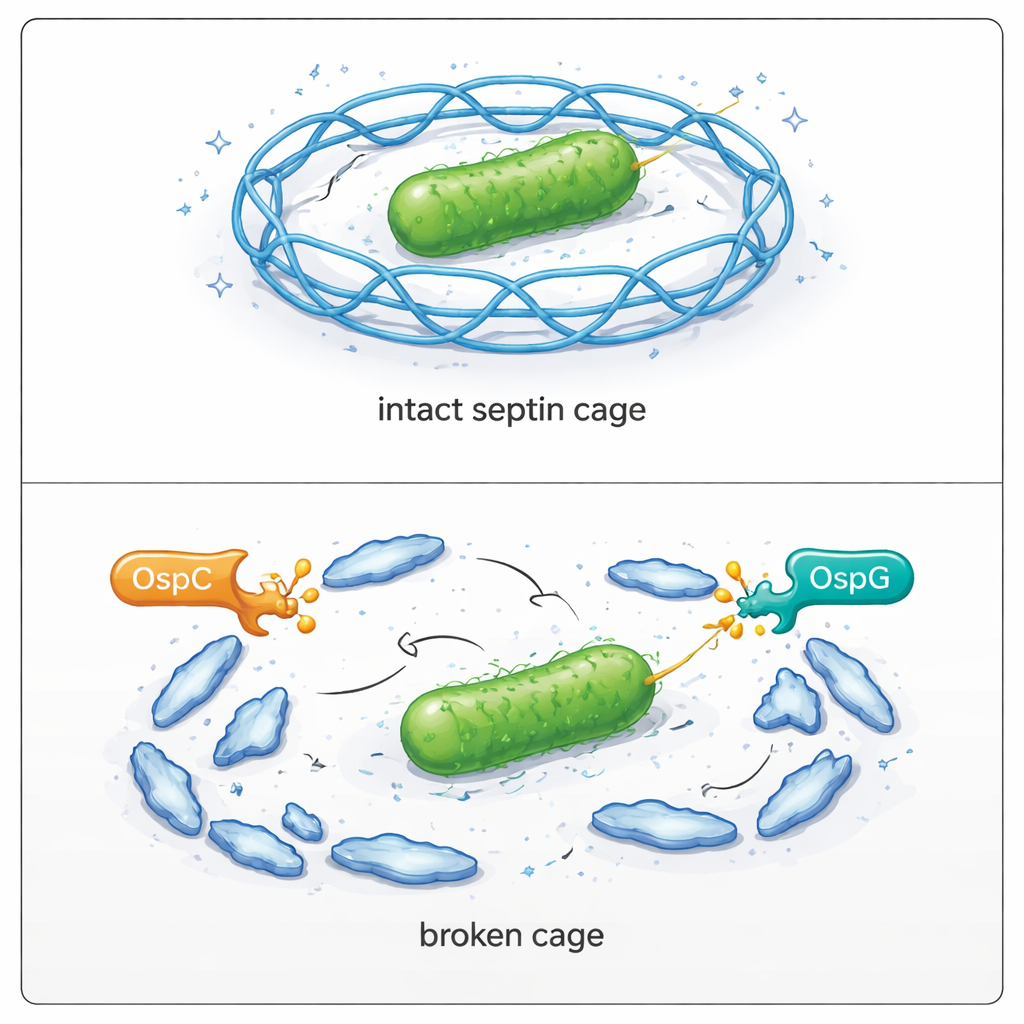
Obserwowanie, jak klatki zawodzą w zakażonych komórkach
Zespół powrócił następnie do badań w żywych komórkach, by zobaczyć konsekwencje. W komórkach ludzkich zakażonych dziką Shigellą tylko mniejszość bakterii znalazła się w klatkach septynowych. Gdy wszystkie białka OspC zostały genetycznie usunięte, odsetek uwięzionych bakterii niemal się podwoił. Usunięcie OspG dało podobny efekt, a jednoczesne usunięcie OspC i OspG jeszcze bardziej zwiększyło tworzenie klatek i poważnie osłabiło zdolność bakterii do rozprzestrzeniania się przez warstwę komórek. Ponowne wprowadzenie aktywnych białek OspC do mutantów przywróciło ich ucieczkę z klatek oraz zdolność do replikacji i tworzenia dużych plakatów zakażeń. Mikroskopia potwierdziła, że gdy SEPT9 nie może być modyfikowany w argininie 561, skutecznie włącza się do klatek; gdy jest zmieniany przez OspC, tworzenie klatek wokół bakterii gwałtownie spada.
Co to oznacza dla walki z Shigellą
Mówiąc przystępnie, praca ta pokazuje, że Shigella posiada dopasowaną parę molekularnych narzędzi zaprojektowanych do wyłamywania prętów wewnątrzkomórkowego „więzienia”. OspC bezpośrednio osłabia białkowe cegiełki potrzebne do budowy klatek septynowych, podczas gdy OspG sprzyja ich usuwaniu inną ścieżką chemiczną. Wspólnie te strategie pozwalają bakteriom uwolnić się, poruszać wewnątrz komórek i nawiązywać inwazję na sąsiednie komórki. Zrozumienie tych precyzyjnych mechanizmów ucieczki pogłębia naszą wiedzę o działaniu odporności wewnątrzkomórkowej i wskazuje nowe możliwości terapeutyczne: leki blokujące OspC lub chroniące kluczowe kontakty septynowe mogłyby przywrócić naturalną zdolność komórek do chwytania i eliminowania tego niebezpiecznego patogenu.
Cytowanie: Tang, Z., Xian, W., Özbaykal Güler, G. et al. Shigella flexneri evades septin-mediated cell-autonomous immunity via protein ADP-riboxanation. Nat Commun 17, 1727 (2026). https://doi.org/10.1038/s41467-026-68425-0
Słowa kluczowe: Shigella, klatki septynowe, odporność komórkowa, czynniki wirulencji bakterii, ADP-rybozylacja