Clear Sky Science · pl
Naturalne peptydy celujące w ClpC1 różnicowo zaburzają proteom Mycobacterium tuberculosis
Dlaczego zaburzanie bakterijnych ekip sprzątających ma znaczenie
Gruźlica nadal należy do najbardziej śmiercionośnych chorób zakaźnych na świecie, a szczepy Mycobacterium tuberculosis oporne na leki utrudniają leczenie. Większość istniejących antybiotyków atakuje ścianę komórkową bakterii albo jej zdolność do produkcji energii i kopiowania materiału genetycznego. To badanie bada zupełnie inny słaby punkt: wewnętrzny „zespół porządkowy” komórki, który dba o jakość białek. Poprzez zrozumienie, jak nowe związki pochodzenia naturalnego zakłócają ten system sprzątający, naukowcy liczą na zaprojektowanie przyszłych leków zdolnych zabić prątki gruźlicy w nowych i trwalszych sposób.
Centralny ośrodek nadzoru białek w komórce
Jak wszystkie żywe komórki, bakteria wywołująca gruźlicę nieustannie wytwarza, składa, naprawia i odzyskuje swoje białka. Kluczowym elementem tej sieci porządkowej jest duży kompleks zwany ClpC1–ClpP1P2. Jedna część (ClpC1) działa jak chaperon, rozpoznając i chwytając uszkodzone lub zbędne białka, podczas gdy druga część (ClpP1P2) rozcina je na kawałki do recyklingu. System ten jest niezbędny dla przeżycia bakterii, zwłaszcza w warunkach stresu, takich jak wysoką temperaturą czy atakiem antybiotyków. Kilka naturalnych peptydów — ecumicyna, ilamycyny (rufomycyny) i cyklomaryny — jest już znanych z wiązania się z ClpC1 i wykazywania silnej aktywności zabijającej prątki, co sugeruje, że ten kompleks może być potężnym celem dla leków. 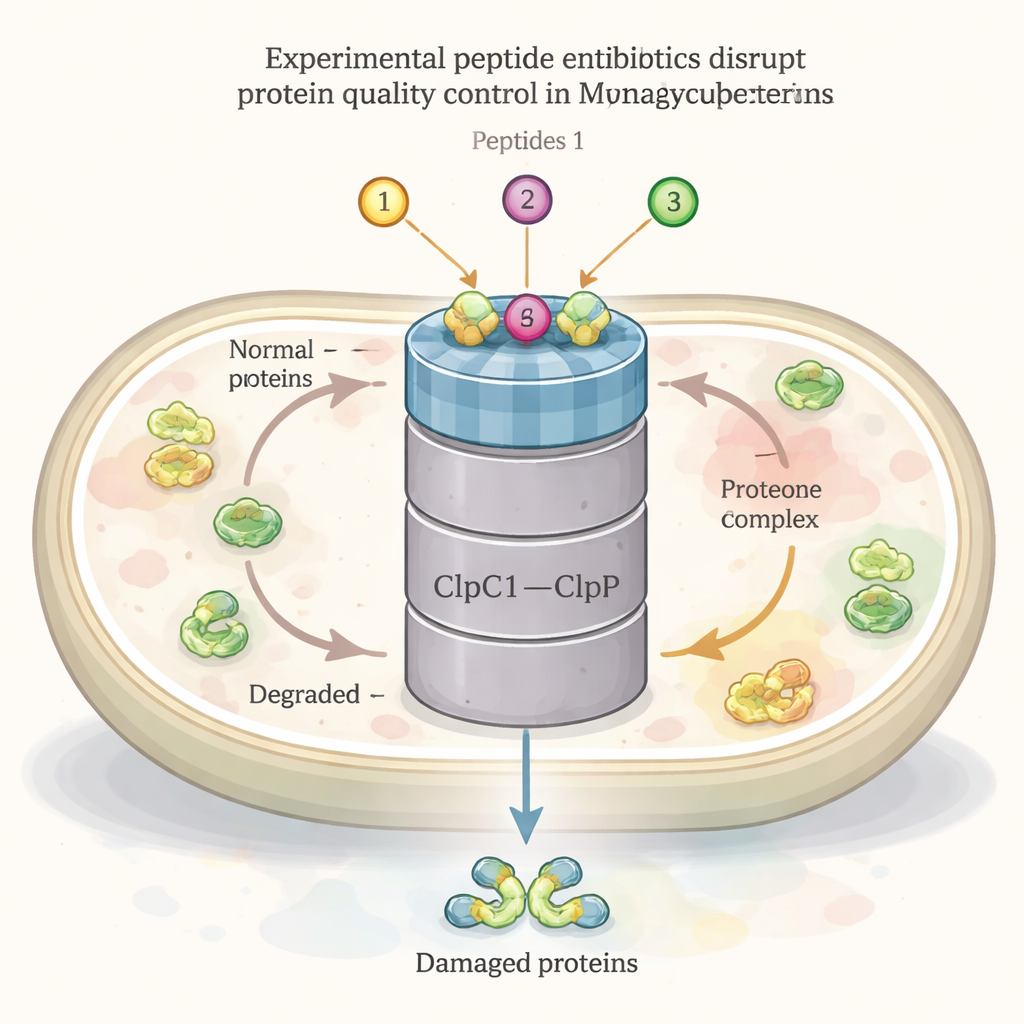
Trzy spokrewnione leki, trzy różne skutki
Naukowcy przeanalizowali po jednym przedstawicielu każdej z trzech rodzin peptydów: analog ecumicyny (Ecu*), ilamycynę E (IlaE) oraz pochodną cyklomaryny (desoksycyklomaryna, dCym). Chociaż wszystkie trzy wiążą się z tym samym obszarem ClpC1, nie zachowują się jednakowo w komórce. Wykorzystując ilościową proteomikę — metodę mierzącą tysiące białek jednocześnie — odkryli, że Ecu* powodował najszersze zaburzenia, istotnie zmieniając poziomy niemal 17% wszystkich białek bakteryjnych. IlaE zmieniła około 12%, a dCym około 7%. Tylko 72 białka były konsekwentnie dotknięte przez wszystkie trzy związki, i większość z nich uległa zmniejszeniu w obfitości. Pokazuje to, że każda cząsteczka wprawia maszynę ClpC1 w inną konfigurację, przekształcając krajobraz białkowy komórki na różne sposoby, zamiast po prostu „wyłączyć maszynę”.
Zapchanie rozdrabniacza versus odcięcie zasilania
Aby umieścić te efekty w kontekście, zespół porównał peptydy z bortezomibem, lekiem przeciwnowotworowym, który szeroko blokuje enzymy degradujące białka. U prątków gruźlicy bortezomib powodował ogólny narastanie wielu białek, co jest spodziewane, gdy „rozdrabniacze” zostają wyłączone. W przeciwieństwie do tego peptydy wywoływały bardziej selektywne wzorce: niektóre znane cele ClpC1 akumulowały się, inne ulegały wyczerpaniu, i nie zaobserwowano globalnej inhibicji całego rozkładu białek. Szczegółowe testy z oczyszczonymi komponentami wykazały, że każdy peptyd zmieniał sposób, w jaki obsługiwane są określone substraty. Na przykład wszystkie trzy zakłócały niszczenie jednego białka regulatorowego (PanD), ale tylko Ecu* blokował rozkład modelowego, nieuporządkowanego białka, a tylko dCym upośledzał degradowanie białka ochronnego przed stresem Hsp20. Różnice te sugerują, że ogólny kształt i elastyczność poszczególnych białek wpływają na to, jak są one dotknięte, gdy ClpC1 zostaje „złe nastrojony” przez dany związek. 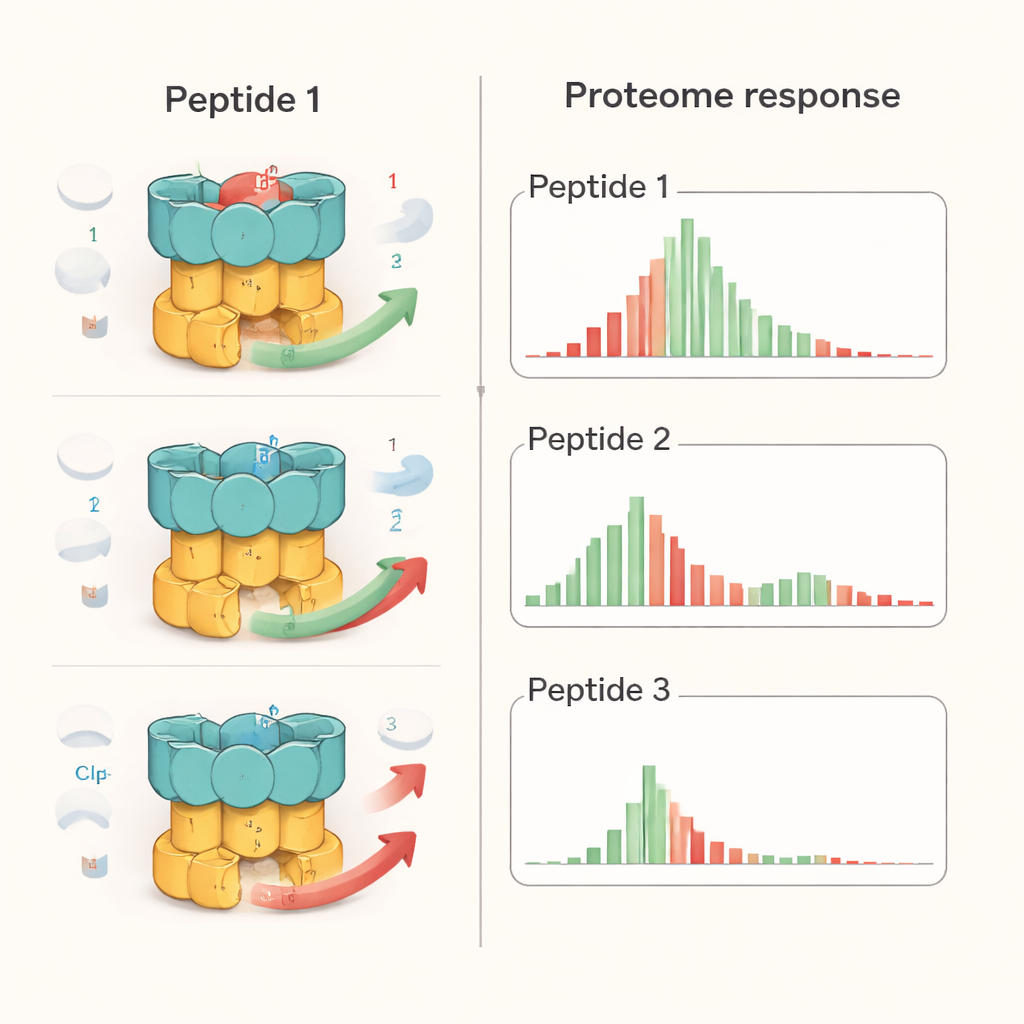
Reakcje na stres i bakteryjne mechanizmy ratunkowe
Prątek gruźlicy posiada systemy zapasowe, które radzą sobie, gdy uszkodzenia białek przytłaczają główną maszynerię sprzątającą. Jednym z takich systemów jest inny chaperon, ClpC2, który może wiązać związki podobne do cyklomaryny i zmniejszać ich wpływ na ClpC1. Badanie wykazało, że chociaż wszystkie trzy peptydy mogą wiązać ClpC2 in vitro, tylko pochodna cyklomaryny (dCym) faktycznie wywołała podwyższenie poziomów ClpC2 w żywych bakteriach i stała się bardziej skuteczna, gdy ClpC2 było eksperymentalnie zmniejszone. W przeciwieństwie do tego Ecu* i IlaE pozostały efektywne nawet przy obniżonym ClpC2, co sugeruje, że w dużej mierze omijają ten bakteryjny mechanizm ratunkowy. Zespół odkrył też silne, specyficzne dla związku powiązanie z Hsp20, małym białkiem zapobiegającym szkodliwym agregatom: Ecu* (a w mniejszym stopniu IlaE) wywoływał dramatyczne wzrosty poziomów Hsp20, a Ecu* wiązał się bezpośrednio z Hsp20, ujawniając nowe połączenie między tymi kandydatami na leki a siecią odpowiedzi na stres w komórce.
Wykorzystywanie stresu jako przewagi terapeutycznej
Ponieważ system ClpC1 jest szczególnie ważny w trudnych warunkach, badacze testowali leki, gdy bakterie były poddane łagodnemu stresowi cieplnemu, który zwiększa ilość nieprawidłowo sfałdowanych białek. W tych warunkach zarówno Ecu*, jak i dCym stały się znacznie bardziej zabójcze, osiągając toksyczność porównywalną z bortezomibem, mimo że działają bardziej selektywnie. To pokazuje, że celowanie w maszynerię kontroli jakości białek może być równie skuteczne jak wyłączenie wszystkich głównych proteaz, lecz z potencjalnie większą precyzją. Praca wykazała również, że wiele zmian wywołanych przez Ecu* w poziomach białek nie odzwierciedlało prosto zmian aktywności genów, podkreślając, że zaburzenie ClpC1 przede wszystkim zakłóca regulację po translacyjnej stronie tworzenia białek.
Co to oznacza dla przyszłych terapii przeciwko gruźlicy
Dla osób spoza specjalności kluczowy wniosek jest taki, że prątki gruźlicy polegają na precyzyjnie wyważonym wewnętrznym systemie sprzątania i odpowiedzi na stres, by przetrwać. Trzy testowane peptydy pochodzenia naturalnego chwytają tę samą centralną maszynę, lecz wprawiają ją w różne tryby, prowadząc do odmiennych i wysoce specyficznych zniekształceń w składzie białkowym bakterii. Co ważne, związki podobne do ecumicyny i ilamycyny unikają wrodzonego mechanizmu ratunkowego bakterii, który może osłabić działanie cyklomaryny, a jednocześnie nadal paraliżują patogen pod stresem. Te właściwości czynią je obiecującymi szkieletem dla przyszłych leków przeciwgruźliczych, w tym zaprojektowanych cząsteczek, które mogłyby zmusić komórki prątka do selektywnego niszczenia własnych niezbędnych białek lub które mogłyby stać się częścią „chimerycznych ukierunkowujących białka” do precyzyjnego skierowania bakteryjnej autodegradacji.
Cytowanie: Barter, I.K., Bedding, M.J., Leodolter, J. et al. ClpC1-targeting peptide natural products differentially dysregulate the proteome of Mycobacterium tuberculosis. Nat Commun 17, 1725 (2026). https://doi.org/10.1038/s41467-026-68423-2
Słowa kluczowe: gruźlica, jakość białek, ClpC1, oporność na antybiotyki, antybiotyki pochodzenia naturalnego