Clear Sky Science · pl
Jednoczesne profilowanie epigenomu i pomiar aktywności regulatorowej przy użyciu e2MPRA
Odczytywanie ukrytych przełączników komórki
Każda komórka w twoim ciele zawiera zasadniczo tę samą sekwencję DNA, a mimo to komórka mózgowa i komórka wątroby zachowują się bardzo inaczej. Sekret tkwi w krótkich fragmentach DNA, które działają jak ściemniacze dla genów — zwiększają, zmniejszają lub wyłączają ich aktywność. W tym badaniu wprowadzono potężne nowe narzędzie, zwane e2MPRA, które pozwala naukowcom przetestować jednocześnie tysiące takich przełączników, a jednocześnie obserwować, jak DNA jest w komórce upakowane i znakowane — kluczowe kroki do zrozumienia rozwoju, ryzyka chorób i tego, dlaczego niektóre warianty genetyczne mają znaczenie, a inne nie.
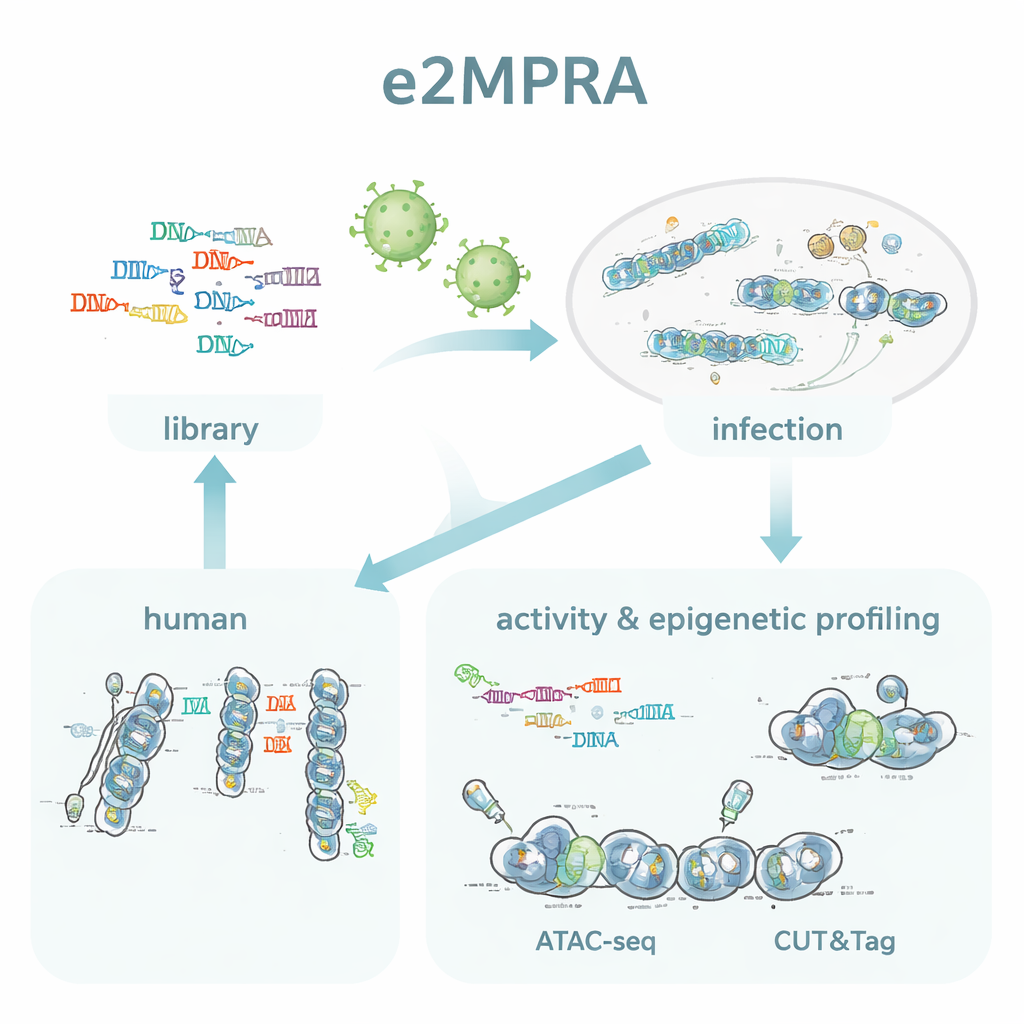
Od map DNA do funkcji DNA
W ciągu ostatniej dekady badacze stworzyli obszerne mapy „kandydatów” na regulatory cis. Stosują metody pokazujące, gdzie DNA jest luźno upakowane (otwarta chromatyna), jakie białka są związane oraz które modyfikacje histonów występują w otoczeniu. Te mapy robią wrażenie, ale w dużej mierze mają charakter opisowy: samo przyłączenie białka czy pojawienie się markera nie dowodzi, że sekwencja rzeczywiście kontroluje aktywność genu. Tradycyjne masowo równoległe testy reporterowe (MPRA) mogą sprawdzić, czy tysiące fragmentów DNA wzmacniają lub tłumią gen raportowy, ale nie informują, które białka się tam wiążą ani jakie zmiany epigenetyczne im towarzyszą.
Dwufunkcyjny test aktywności i znaków epigenetycznych
Autorzy stworzyli e2MPRA, łącząc lentiviralne MPRA z dwoma technikami epigenomicznymi: ATAC-seq i CUT&Tag. Najpierw budują bibliotekę DNA, w której każdy kandydat na element regulatorowy jest połączony z krótkim kodem kreskowym i umieszczony obok minimalnego promotora i genu raportowego. Tę bibliotekę pakują następnie w lentivirusy i integrują wielokrotnie z genomami hodowlanych komórek ludzkich. Z tej samej puli komórek odczytują kody kreskowe w RNA, aby zmierzyć aktywność regulatorową, a także używają ATAC-seq i CUT&Tag, aby zmierzyć dostępność chromatyny i kluczowy marker histonowy (H3K27ac) specyficznie w wstawionych sekwencjach. Normalizując te sygnały do częstotliwości faktycznej integracji każdej sekwencji, otrzymują równoległe pomiary „siły włączania/wyłączania” oraz stanu epigenetycznego dla tysięcy elementów w jednym eksperymencie.
Odszyfrowywanie, jak motywy czynników transkrypcyjnych współdziałają
Aby zobaczyć, co ta technologia może ujawnić, zespół zbudował syntetyczne enhancery z znanych motywów czynników transkrypcyjnych używanych w komórkach wątroby. Ułożyli te motywy w różnej liczbie i kolejności na neutralnych matrycach DNA. Niektóre czynniki, takie jak HNF1A i XBP1, zachowywały się jak klasyczni aktywatory: dodanie kolejnych kopii zwiększało sygnał raportera. Inne, jak HNF1A i ONECUT1, głównie zwiększały dostępność chromatyny, odpowiadając swojej roli „pionierskich” czynników, które otwierają zamknięte fragmenty DNA. PPARA wykazywał inny wzorzec: silnie zmieniał chromatynę i modyfikacje histonów, ale samodzielnie nie inicjował transkrypcji, choć współdziałał z innymi czynnikami, aby podnieść aktywność genów. REST, znany represor, tłumił aktywność, gdy umieszczono go obok aktywatorów. Co uderzające, samo przestawienie kolejności czterech motywów mogło znacznie zmienić siłę enhancera, a aktywatory zwykle działały najlepiej, gdy były bliżej promotora — ujawniając pewną gramatykę w organizacji tych motywów.
Wyszukiwanie wrażliwych zasad w enhancerach pluripotencji
Następnie badacze zwrócili się ku enhancerom ważnym dla tożsamości komórek macierzystych, skupiając się na regionach związanych przez czynniki pluripotencji POU5F1 (znany też jako OCT4) i SOX2. Stworzyli gęste biblioteki mutacyjne, w których każda zasada w 100-nukleotydowych enhancerach była systematycznie zmieniana, wraz z losowo zeskramblowanymi przesunięciami sześciu zasad. Stosując e2MPRA w indukowanych pluripotentnych komórkach macierzystych, mogli zobaczyć, które mutacje osłabiały lub wzmacniały aktywność raportera oraz jak wpływały na otwartość chromatyny i acetylację. Uszkodzenie motywu wiązania POU5F1::SOX2 często redukowało zarówno aktywność genów, jak i znaki epigenetyczne, potwierdzając jego centralną rolę. W dobrze zbadanym enhancerze w pobliżu genu POU5F1 znaleźli też, że zmiana motywu YY1 zwiększała transkrypcję, ale zmniejszała otwarcie chromatyny, sugerując, że niektóre czynniki mogą promować otwarty stan, a jednocześnie ograniczać ekspresję.
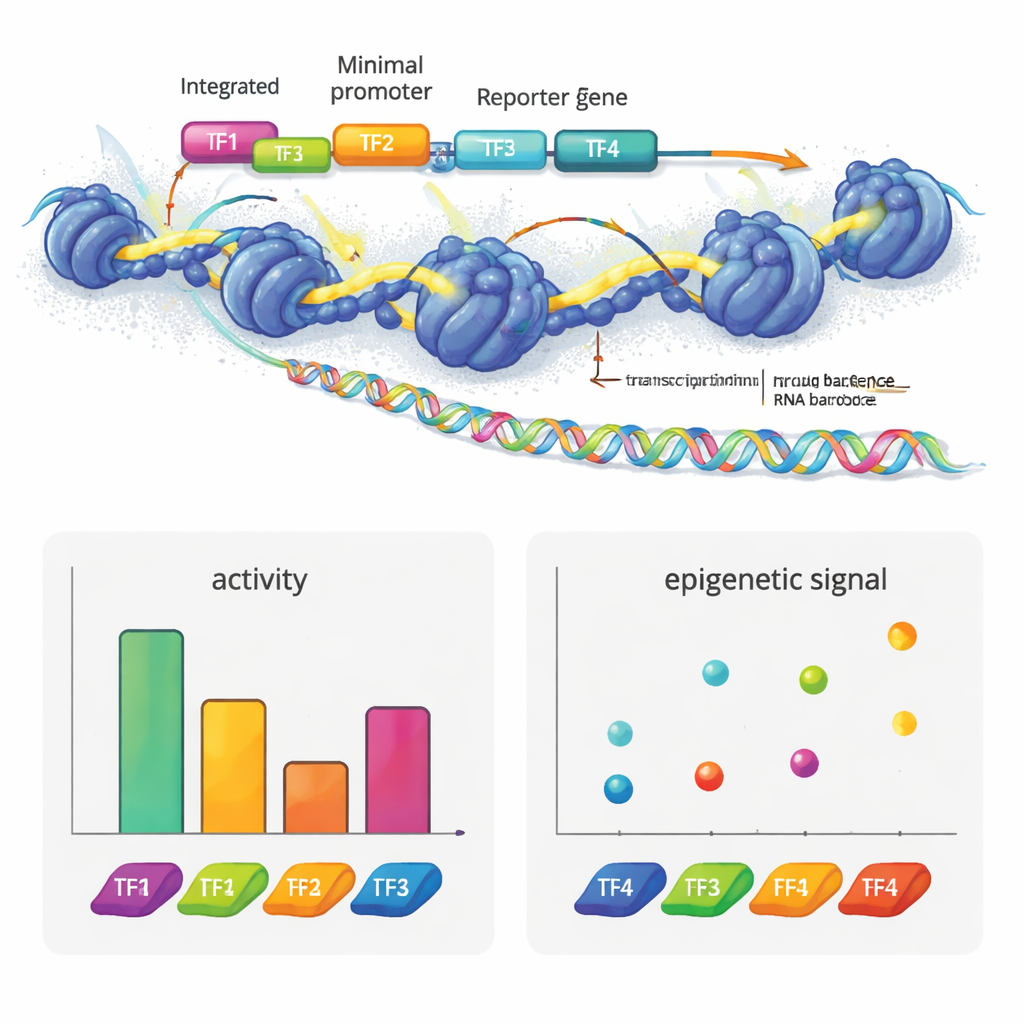
Co to znaczy dla genów i chorób
e2MPRA nie odtwarza idealnie wszystkich niuansów naturalnego trójwymiarowego układu genomu, ale oferuje praktyczny sposób porównywania tysięcy sekwencji regulatorowych i wariantów w tych samych warunkach. Łącząc wynik funkcjonalny (jak silnie fragment DNA napędza gen) z odczytami epigenetycznymi (jak ten DNA jest upakowany i znakowany), ta metoda pomaga wyjaśnić, dlaczego określone motywy czynników transkrypcyjnych, ich kombinacje i pozycje są tak istotne. W dłuższej perspektywie narzędzia takie jak e2MPRA mogą ułatwić interpretację niekodujących wariantów genetycznych związanych z chorobami, projektowanie syntetycznych enhancerów do terapii genowej oraz budowę bardziej kompletnego „kodu regulatorowego” łączącego sekwencję DNA z zachowaniem komórek.
Cytowanie: Zhang, Z., Georgakopoulos-Soares, I., Bourque, G. et al. Simultaneous epigenomic profiling and regulatory activity measurement using e2MPRA. Nat Commun 17, 1724 (2026). https://doi.org/10.1038/s41467-026-68422-3
Słowa kluczowe: regulacja genów, enhancery, epigenetyka, czynniki transkrypcyjne, genomika funkcjonalna