Clear Sky Science · pl
Ligazy ubikwityny E3 „strażnicy” celują w związane z rakiem deaminazy APOBEC3, kierując je na degradację w celu ochrony integralności genomu ludzkiego
Ochrona naszego DNA przed „przyjaznym ogniem”
Nasze komórki używają potężnych enzymów do uszkadzania wirusowego DNA, co pomaga nam odpierać infekcje. Jednak niektóre z tych samych enzymów, jeśli wymkną się spod kontroli, mogą przypadkowo uszkodzić nasz własny genom i przyczynić się do rozwoju raka. Badanie to ujawnia, jak komórki ludzkie nadzorują te ryzykowne enzymy, ukazując wbudowany system „kontroli jakości”, który znakuję potencjalnie niebezpieczne warianty do zniszczenia, zanim będą mogły przepisać nasze DNA.
Wirusobójcy, którzy mogą się obrócić przeciwko nam
Rodzina enzymów APOBEC3 zwykle pomaga w obronie przed wirusami takimi jak HIV, chemicznie modyfikując wirusowe DNA i wywołując błędy śmiertelne dla wirusa. Ludzie noszą siedem wariantów APOBEC3, z których trzy — A3A, A3B oraz forma A3H nazywana haplotypem I (A3H-I) — są silnie powiązane ze wzorcami mutacji obserwowanymi w wielu nowotworach. Te konkretne enzymy mogą przenikać do jądra komórkowego, gdzie znajdują się nasze chromosomy, i wprowadzać charakterystyczne skupiska mutacji w genomie. Sygnatury powiązane z APOBEC pojawiają się w ponad połowie wszystkich nowotworów ludzkich, szczególnie w raku piersi, płuc i pęcherza, gdzie zwiększają pulę zmian genetycznych, z których guzy mogą korzystać, by się adaptować i opierać terapii.
Dlaczego najbardziej niebezpieczne formy są paradoksalnie niestabilne
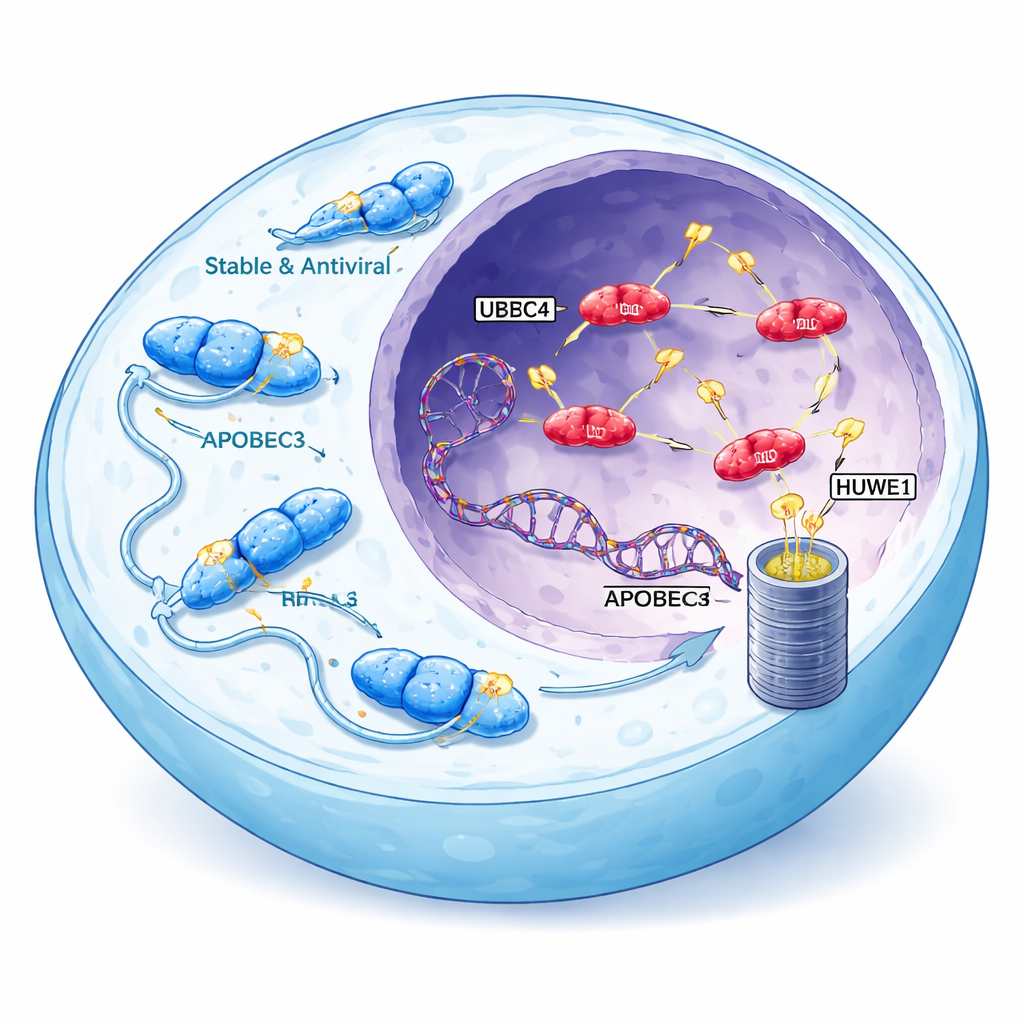
Ciekawie, enzymy APOBEC3 najsilniej związane z rakiem są też najmniej stabilne. W odróżnieniu od kuzynów cytoplazmatycznych, którzy gromadzą się na wysokich poziomach i skutecznie blokują wirusy, A3A, A3B i A3H-I są szybko rozkładane i zwykle występują w niskich stężeniach w jądrze. Badacze założyli, że ta niestabilność może być zamierzona: jeśli komórki aktywnie ograniczają poziomy jądrowych białek APOBEC3, każda utrata tej kontroli mogłaby uwolnić fale mutagenezy. Używając A3H-I jako modelu, wykazali, że związane z rakiem APOBEC3 są niszczone głównie przez proteasom — komórkowy niszczarka białek — po oznaczeniu małymi „flagi” molekularnymi, ubikwityną, na wielu miejscach aminokwasowych.
Odnalezienie komórkowych strażników
Aby wskazać maszynerię odpowiedzialną za znakowanie A3H-I i A3B, zespół połączył przesiew CRISPR z mapowaniem bliskości białek. Zaprojektowali komórki, które świecą inaczej w zależności od stabilności A3H-I i jego nieszkodliwej odmiany A3H-II, a następnie systematycznie wyłączali geny zaangażowane w degradację białek. Trzy ligazy ubikwityny — UBR4, UBR5 i HUWE1 — wyróżniły się. Usunięcie dowolnej z tych ligaz selektywnie zwiększało poziomy niestabilnego, jądrowego A3H-I, nie wpływając na stabilny, cytoplazmatyczny A3H-II. Te same ligazy niezależnie podnosiły poziomy endogennego A3B w liniach komórkowych pochodzenia jelitowego i układu odpornościowego, a usunięcie wszystkich trzech jednocześnie wywołało addytywny skok w obfitości A3B. Doświadczenia biochemiczne pokazały ponadto, że UBR5 i HUWE1 fizycznie wiążą się z A3B i A3H-I i bezpośrednio przyłączają łańcuchy ubikwityny, podczas gdy UBR4 wydaje się wyspecjalizowany we wydłużaniu tych łańcuchów, czyniąc białka łatwiejszymi do skonsumowania.
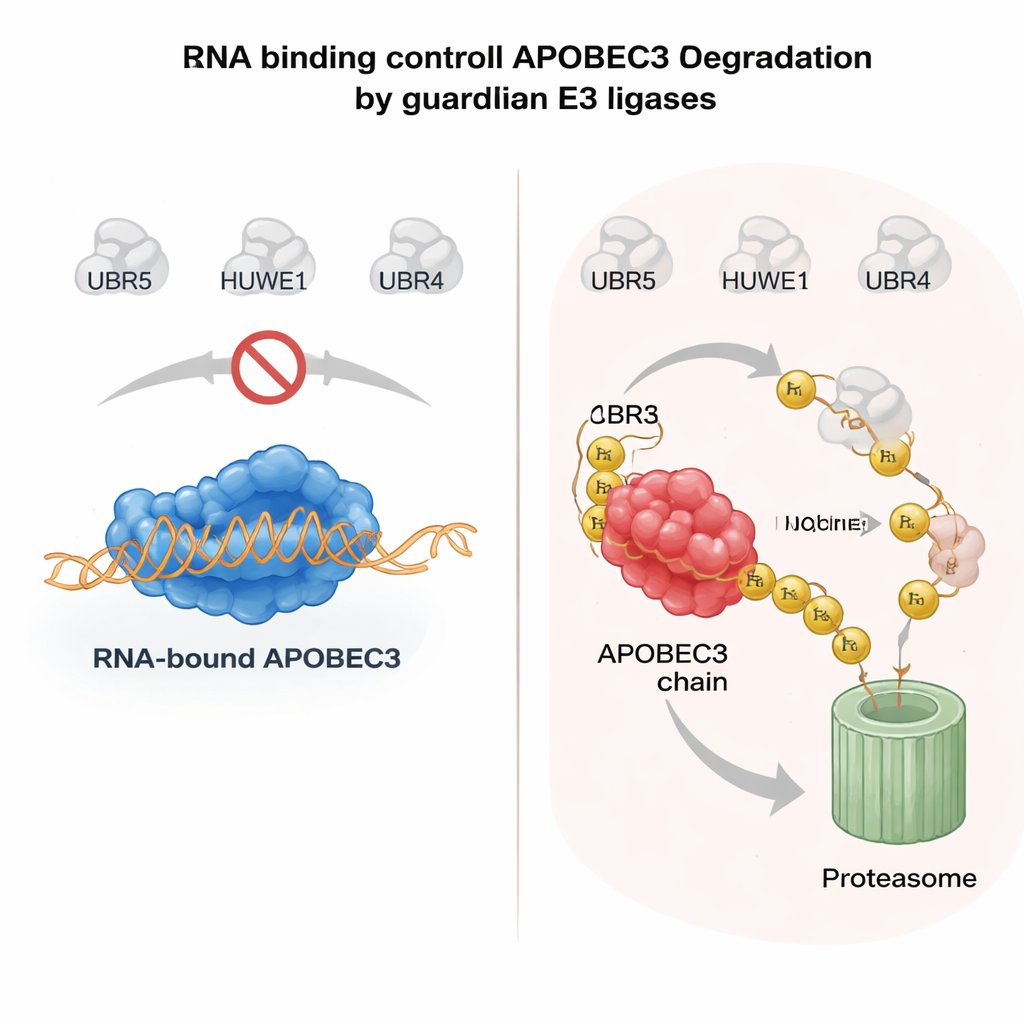
RNA jako pas bezpieczeństwa dla ryzykownych enzymów
Co decyduje o tym, czy enzym APOBEC3 zostanie oszczędzony czy zniszczony? Kluczową wskazówką okazał się sposób, w jaki białka APOBEC3 wiążą się z cząsteczkami RNA w cytoplazmie. Kiedy A3H lub inny członek rodziny, A3G, wiążą RNA, mają tendencję do pozostawania w dużych kompleksach w cytosolu i są stosunkowo stabilne. Mutacje osłabiające wiązanie RNA powodują, że te enzymy przemieszczają się do jądra, tracą ochronne interakcje i stają się wysoce niestabilne. Autorzy pokazali, że gdy białka APOBEC3 nie są związane z RNA, UBR5 i HUWE1 rozpoznają odsłonięte powierzchnie enzymu, dekorują je ubikwityną i kierują do jądrowej degradacji. W systemach oczyszczonych dodanie RNazy, która usuwa RNA, znacznie zwiększało zdolność tych ligaz do wiązania i ubikwitynacji APOBEC3, potwierdzając, że wiązanie RNA działa jak tarcza molekularna. Ten mechanizm pozwala komórkom utrzymywać aktywne w cytoplazmie antywirusowe APOBEC3, jednocześnie szybko usuwając każdą niewiążącą się, zagrażającą genom puli w jądrze.
Gdy strażnicy zawodzą: powiązania z mutacjami nowotworowymi
Jeżeli UBR4, UBR5 i HUWE1 pełnią rolę strażników, ich utrata powinna zwiększać poziom mutacji. Naukowcy sprawdzili to, wyłączając każdą ligazę w komórkach raka jelita grubego i śledząc zmiany DNA w czasie za pomocą czułej metody sekwencjonowania odczytującej „sygnatury” mutacyjne. Usunięcie tych ligaz, szczególnie w komórkach wyrażających A3H-I, wzmocniło wzorce mutacji specyficzne dla APOBEC — dokładnie takie, jakie obserwuje się w guzach ludzkich. Rozszerzając analizę na dane pacjentów, przebadali tysiące genomów nowotworowych i stwierdzili, że guzy z mutacjami w UBR5 lub HUWE1 miały istotnie wyższy udział sygnatur mutacji powiązanych z APOBEC niż guzy z nienaruszonymi ligazami, nawet po uwzględnieniu całkowitego obciążenia mutacyjnego. Sugeruje to, że wadliwe ligazy‑strażnicy u pacjentów mogą pozwolić związanym z rakiem enzymom APOBEC3 wymknąć się spod kontroli i przekształcać genom guza.
Co to oznacza dla przyszłej opieki nad pacjentami z rakiem
Dla osoby niezajmującej się tą dziedziną kluczowy wniosek jest taki, że nasze komórki dysponują wyrafinowanym systemem nadzoru, który zapobiega przypadkowemu sabotowaniu własnego DNA przez pomocne enzymy antywirusowe. UBR4, UBR5 i HUWE1 działają jako strażnicy, wykrywając, kiedy enzymy APOBEC3 nie są już bezpiecznie związane z RNA i zwłaszcza w jądrze kierując je do komórkowej niszczarki. Gdy ten system kontroli jest osłabiony — przez mutacje w ligazach lub przez leki blokujące degradację białek — aktywność APOBEC3 może napędzać genetyczny chaos, który napędza ewolucję nowotworu i oporność na leczenie. Zrozumienie tej sieci strażników otwiera drogę do nowych markerów diagnostycznych, takich jak mutacje ligaz czy poziomy białek APOBEC, i sugeruje, że ostrożne modulowanie tej ścieżki mogłoby kiedyś pomóc ograniczyć szkodliwe fale mutacji w guzach, nie naruszając naszych mechanizmów obrony antywirusowej.
Cytowanie: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
Słowa kluczowe: APOBEC3, stabilność genomu, ligaza ubikwityny, mutageneza nowotworowa, degradacja białek