Clear Sky Science · pl
Wzorcowanie przestrzenne kontraktywności przez samoorganizujący się gradient aktywności mechanogenu leży u podstaw gastrulacji Drosophila
Jak tkanki formują swoje kształty
Wczesne zarodki w jakiś sposób przekształcają proste płaty komórek w złożone struktury trójwymiarowe. W pracy tej postawiono podstawowe pytanie stojące za tym „sztuczkiem”: jak komórki koordynują, gdzie ściskać i zaginąć, aby tkanka złożyła się we właściwym miejscu i kierunku? Obserwując zarodki muszki owocowej z dużą rozdzielczością, autorzy odkrywają sygnał chemiczny zachowujący się jak „mechaniczny morfogen”, który bezpośrednio wzorzecuje miejsca, w których komórki napinają się, napędzając kluczowe zagięcie podczas rozwoju.
Fala, która składa zarodek
U muszki owocowej Drosophila kluczowym etapem wczesnego rozwoju jest gastrulacja, gdy płaska warstwa komórek zapada się do wnętrza, rozpoczynając formowanie jelita. Z tyłu zarodka płat komórek zwany zarodkową prymordium endodermalnym inicjuje ten proces, kurcząc swoje powierzchnie wierzchołkowe (apikalne). To początkowe zagięcie wywołuje przemieszczającą się falę zapadania się tkanki, która przesuwa się naprzód przez przyległe komórki. Autorzy wykazują, że ta fala zależy od sygnału zwanego Fog — wydzielonej cząsteczki aktywującej rodzinę receptorów GPCR, które z kolei włączają komórkowy aparat kontrakcyjny zbudowany z białka motorowego Myosin‑II.
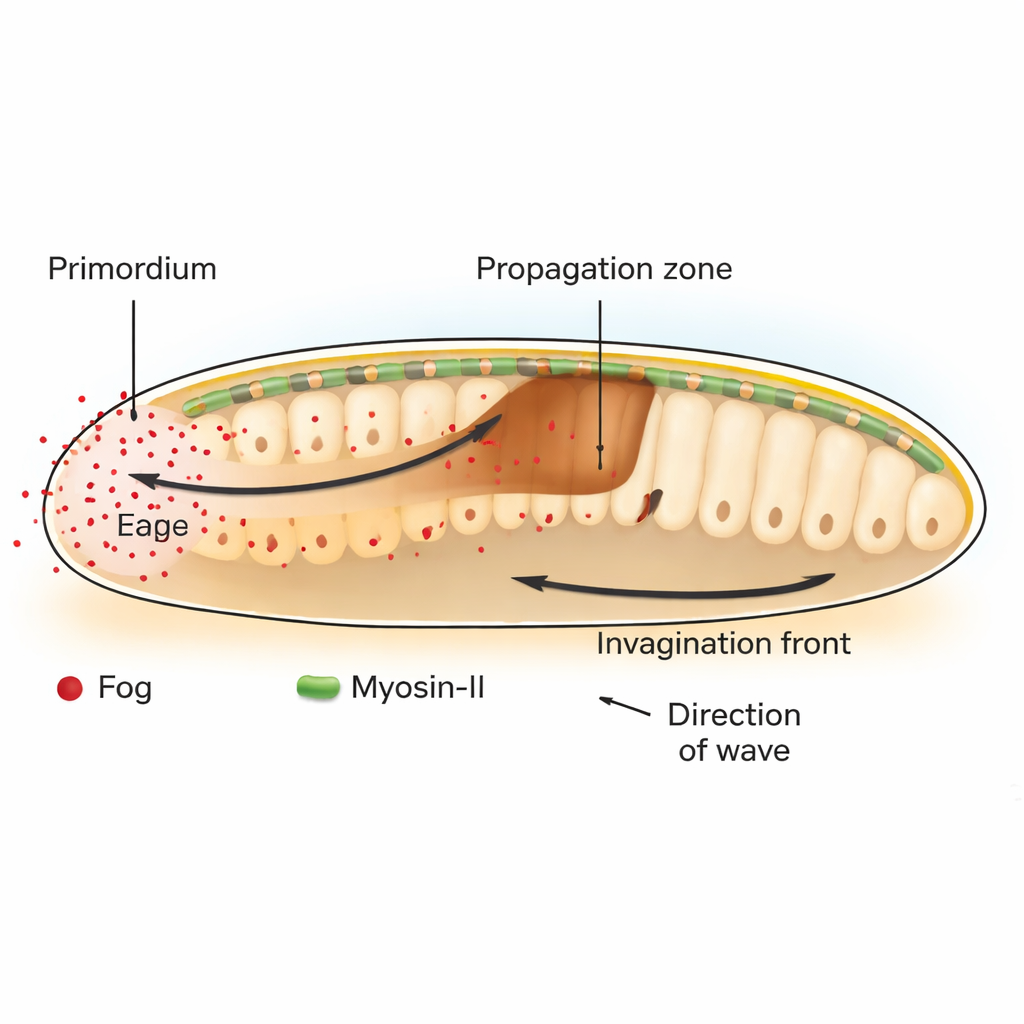
Chemiczny sygnał wzorzecujący siłę, a nie los
Klasycznie biolodzy rozwoju skupiali się na „morfogenach”, dyfundujących cząsteczkach, których gradienty stężeń informują komórki, jaką tożsamość przyjąć. Tutaj Fog zachowuje się inaczej. Zamiast zmieniać, jakiego typu komórką dana okolica się stanie, Fog bezpośrednio reguluje, jak silnie komórki się kurczą. Poprzez selektywne przywracanie lub blokowanie Fog i jego pośrednika Gα tylko w określonych obszarach, badacze pokazują, że Fog produkowany w prymordium jest zarówno niezbędny, jak i wystarczający do wywołania aktywacji Myosin‑II i zaginania tkanki w sąsiedniej strefie propagacji. Gdy Fog jest przytwierdzony tak, że nie może się rozprzestrzeniać, kurczą się tylko komórki produkujące go, a fala invagincji zatrzymuje się po zaledwie jednym lub dwóch rzędach komórek.
Ukryty gradient na powierzchni komórki
Naturalnym pomysłem było, że Fog może tworzyć klasyczny gradient stężenia na zewnątrz komórek. Korzystając z fluorescencyjnie znakowanej wersji Fog i czułych pomiarów fluorescencji, zespół znajduje przeciwny obraz: w cienkiej warstwie płynu między tkanką a jej otoczką (osłonką vitelline) Fog jest wyjątkowo jednorodny. Tymczasem aktywność Myosin‑II tworzy wyraźny, stromy, przemieszczający się gradient, najsilniejszy tuż przed posuwającym się zagięciem i zanikający w odległości kilku średnic komórkowych. Brakuje więc części układanki: Fog nie działa jako prosty wskaźnik stężenia w objętości; zamiast tego niewielka frakcja Fog zostaje krótko uwięziona na powierzchni komórki, wiążąc się z receptorami GPCR i tworząc gradient aktywności związany z powierzchnią, mimo że wolne cząsteczki Fog pozostają równomiernie wymieszane w płynie.
Receptory, endocytoza i adhezja kształtują falę
Autorzy pokazują, że ten powierzchniowy Fog wraz ze swoimi receptorami samoorganizuje się w wzorzec. Tam, gdzie Fog wielokrotnie napotyka receptory, sprzyja grupowaniu i aktywacji receptorów, co rekrutuje więcej Myosin‑II. Proces „sprzątający” na poziomie komórkowym — endocytoza GPCR — usuwa następnie aktywne kompleksy, zapobiegając niekontrolowanej aktywacji i regulując zasięg sygnału. Gdy ta endocytoza jest genetycznie spowolniona, gradient Myosin‑II staje się wyższy i szerszy. Drugim kluczowym uczestnikiem są cząsteczki adhezyjne zwane integrynami. W miarę jak tkanka się zgina, komórki przed fałdem naciskają na osłonkę vitelline; kontakt ten lokalnie aktywuje integryny, które z kolei zwiększają skuteczność sygnalizacji Fog–GPCR. Obszar silnego zaangażowania integryn odpowiada zakresowi gradientu Myosin‑II, a bez integryn fala staje się słaba i krótkodystansowa, nawet jeśli sygnalizacja Fog jest wzmocniona.
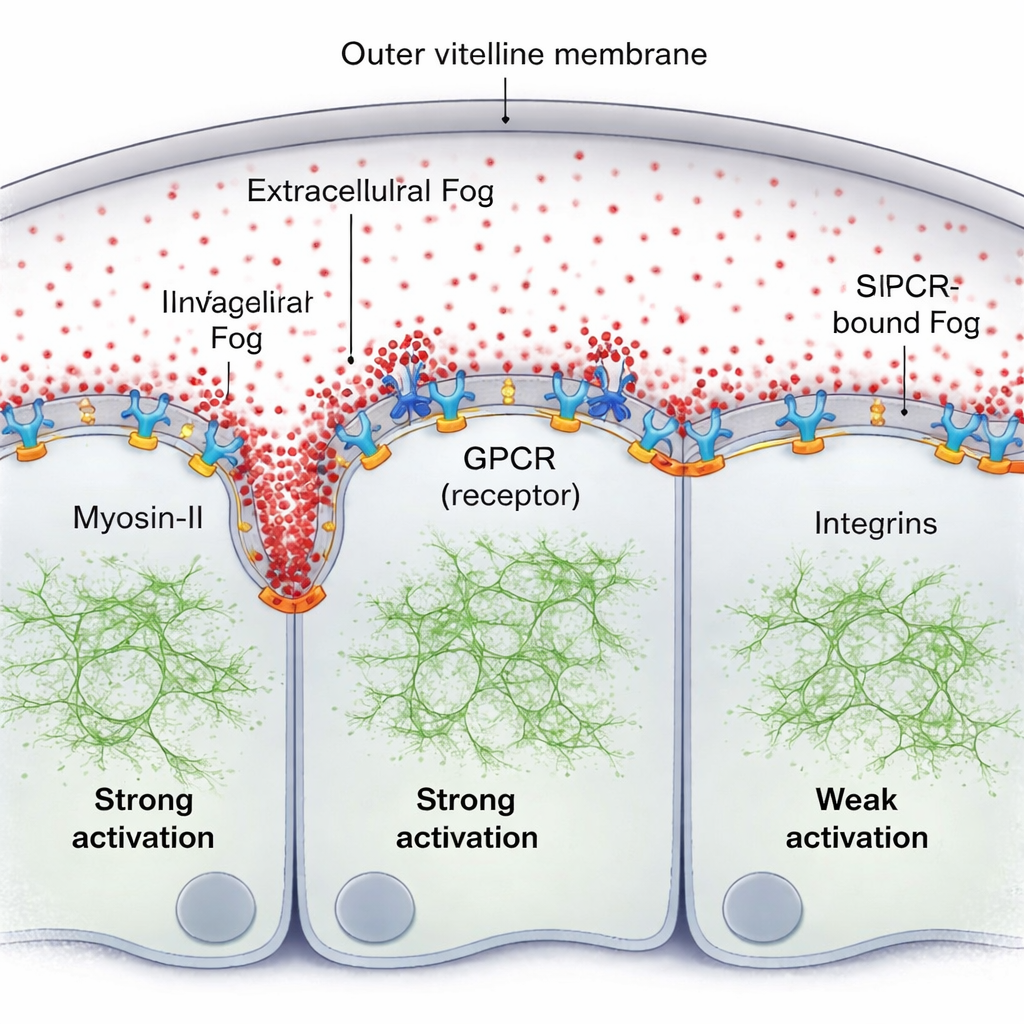
Samoodnawiający się wzorzec mechaniczny
Dla osoby niezwiązanej z dziedziną główne przesłanie jest takie, że zarodek nie polega wyłącznie na wcześniejszych mapach chemicznych, by zdecydować, gdzie się zagiąć. Zamiast tego tworzy w locie ruchomy wzorzec aktywności mechanicznej. Fog rozprowadza się równomiernie, ale jego efektywne działanie jest rzeźbione na powierzchni komórek przez grupowanie receptorów, usuwanie receptorów i zmieniającą się geometrię tkanki, gdy komórki naciskają na otoczenie. To tworzy samoorganizujący się, przemieszczający się gradient sił kontrakcyjnych, który skoordynowaną falą wciąga tkankę do wnętrza. Praca ta dostarcza konkretnego przykładu długo postulowanego „mechanogenu”: dyfundującej molekuły, która bezpośrednio wzorzecuje siły fizyczne w tkance, pomagając wyjaśnić, jak organizmy tak niezawodnie formują swoje kształty podczas rozwoju.
Cytowanie: Mundhe, G., Dunsing-Eichenauer, V., Philippe, JM. et al. Spatial patterning of contractility by a self-organized mechanogen activity gradient underlies Drosophila gastrulation. Nat Commun 17, 1721 (2026). https://doi.org/10.1038/s41467-026-68418-z
Słowa kluczowe: gastrulacja, mechanogen, zarodek Drosophila, mechanika tkanek, szlak Fog