Clear Sky Science · pl
Konfiguracje końców DNA decydują o tworzeniu kompleksu synaptycznego podczas mostkowania końców zależnego od NHEJ
Gdy DNA pęka, komórki muszą działać szybko
Codziennie DNA w naszych komórkach jest nacinane, przecinane i uszkadzane przez normalny metabolizm oraz czynniki środowiskowe. Jednymi z najgroźniejszych urazów są pęknięcia dwuniciowe, gdy obie nici helisy DNA ulegają zerwaniu. Jeśli te przerwy nie zostaną szybko i dokładnie naprawione, komórki mogą obumrzeć lub – co gorsza – przekształcić się w kierunku nowotworu. W tym badaniu zbadano, jak dokładny kształt i chemia pękniętych końców DNA wpływają na to, czy kluczowa droga naprawcza zwana łączeniem niehomologicznym końców (NHEJ) zbliża te końce efektywnie i z możliwie najmniejszą liczbą błędów.
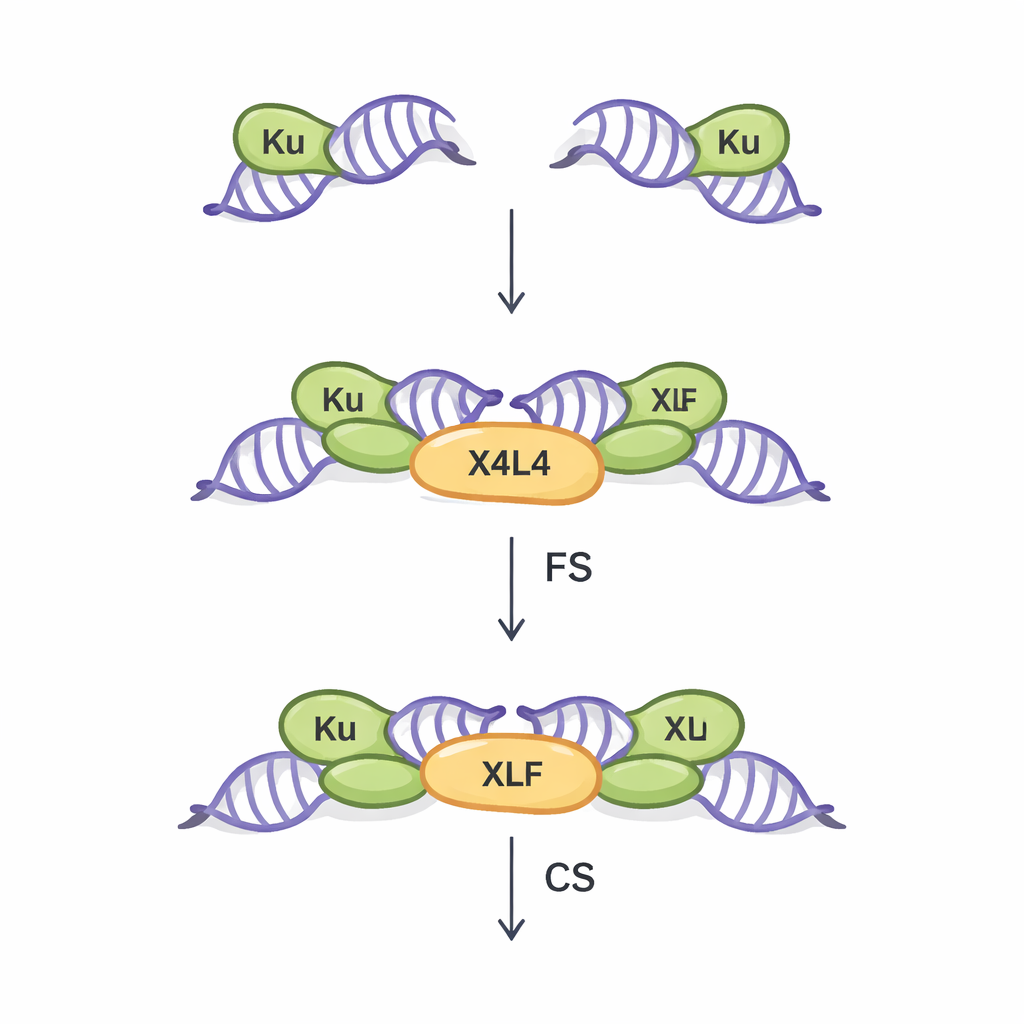
Dwa sposoby zbliżania przerw w DNA
NHEJ jest główną ścieżką naprawczą pęknięć dwuniciowych w większości komórek naszego organizmu. Działa bez potrzeby dopasowanego matrycowego DNA, co czyni go szybkim, lecz stosunkowo podatnym na błędy. Pierwszym kluczowym krokiem w tej ścieżce jest synapsa: fizyczne połączenie dwóch przerwanych końców DNA, aby mogły zostać później złączone. Wcześniejsze prace, głównie z użyciem idealizowanych, prostych końców, ujawniły dwa typy zespołów synaptycznych. W stanie „elastycznej synapsy” (FS) końce są utrzymywane blisko siebie i mogą się poruszać, szukając sposobów parowania. W stanie „bliskiej synapsy” (CS) końce ustawiają się końcem do końca i są gotowe do zespolenia przez enzym ligazy. Trzy podstawowe białka — Ku, XRCC4–Ligase IV (razem określane jako X4L4) oraz XLF — są znane z koordynowania tego procesu, ale wpływ nieregularnych, rzeczywistych końców DNA na wybór stanu synaptycznego pozostawał słabo poznany.
Kształt końca i krótkie dopasowania kierują drogą naprawczą
Naukowcy zastosowali pojedynczą cząsteczkową FRET, technikę fluorescencyjną śledzącą odległości w skali nanometrów, aby obserwować pojedyncze cząsteczki DNA zbliżane przez białka NHEJ. Porównali proste, równe końce z bardziej realistycznymi końcami posiadającymi krótkie ścieżki jednoniciowe — małe ogonki, które mogą się potencjalnie sparować. Stwierdzili, że gdy ogonki są komplementarne, nawet jedynie w kilku nukleotydach, znacznie zwiększa się prawdopodobieństwo utworzenia bliskiego kompleksu synaptycznego. W rzeczywistości trzy pasujące zasady „mikrohomologii” przy pęknięciu wystarczały, by Ku i X4L4 same utworzyły stabilny kompleks CS, bez udziału XLF. Pokazuje to, że samo DNA może dostarczyć części energii i wskazówek zwykle dostarczanych przez białkowe pomocniki.
Jak drobne klapki DNA pomagają stabilizować most
Analizując różne sygnatury FRET, zespół odkrył przynajmniej dwie strukturalne odmiany bliskiego stanu synaptycznego dla końców z nawisami. W jednej z nich same końcówki nawisów łączą się ze sobą, tworząc złącze z nacięciem lub szczeliną. W drugiej miejsca styku, gdzie dwuniciowe DNA spotyka jednoniciowe nawisy, stykają się w linii, podczas gdy nawisy odwracają się na zewnątrz jak małe klapki. Te klapki nadal pozwalają na parowanie zasad i utrzymują końce w bardzo bliskiej odległości, co prawdopodobnie stabilizuje kompleks i daje enzymom przestrzeń do przycinania lub wydłużania DNA przed finalnym zespoleniem. Co ciekawe, powszechne oksydacyjne uszkodzenia w nawisach, takie jak 8-oksoguanina, wpływały na ten proces tylko umiarkowanie, co podkreśla odporność NHEJ na niektóre formy uszkodzeń.
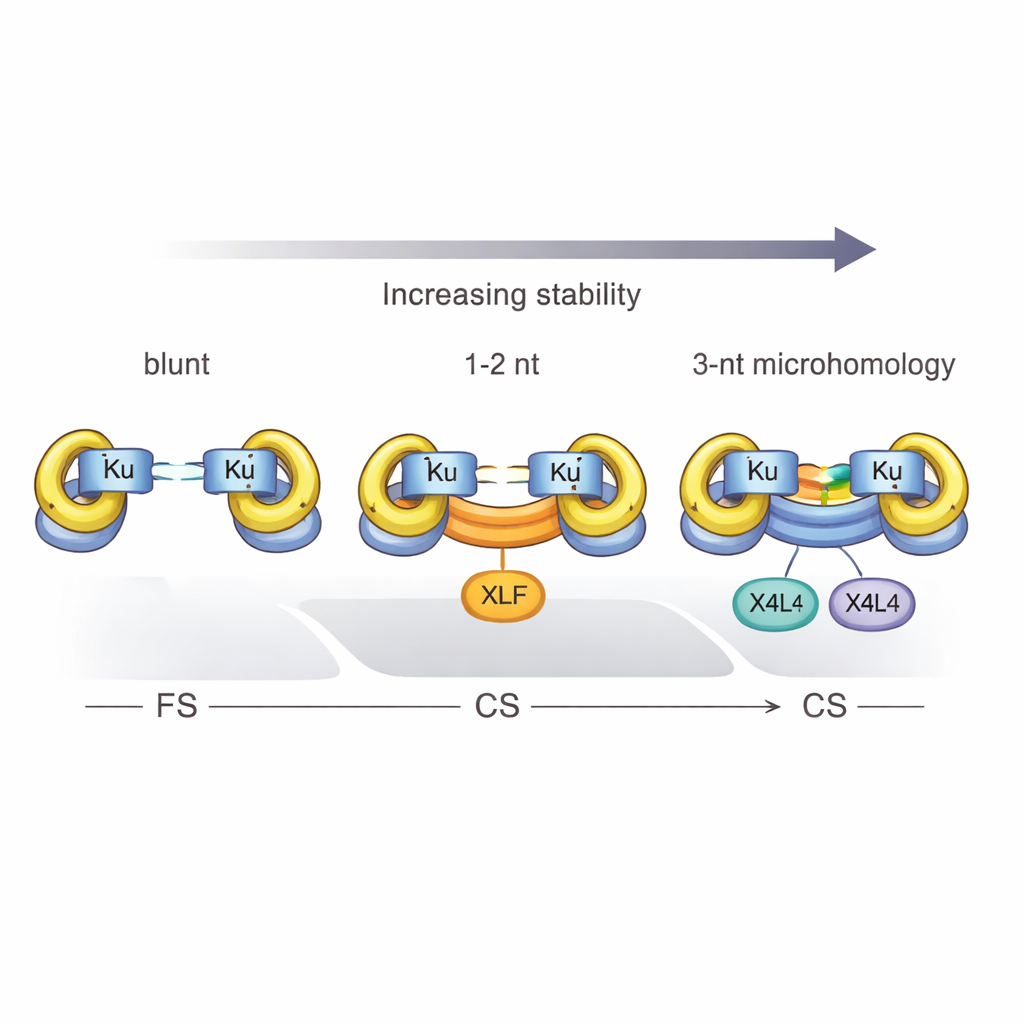
Białka, fosforany i siła trzech
Badanie określiło również twardy próg: co najmniej trzy komplementarne pary zasad są wymagane, aby Ku i X4L4 niezawodnie przekształciły elastyczny kompleks w bliski. Przy tylko jednej lub dwóch zgodnościach system przeważnie utknął w stanie elastycznym, chyba że XLF dołączył, aby pomóc zacisnąć końce. Znaczenie mają także szczegóły chemiczne. Gdy przerwane DNA ma grupę fosforanową 5′ — normalny element wielu fizjologicznych przerw — synapsa staje się bardziej efektywna, a bliskie kompleksy są bardziej prawdopodobne do faktycznego zespalania, przekształcając tymczasowy most w trwałą naprawę. Jednak ten efekt fosforanu nie zastępuje w pełni stabilizującego wpływu parowania zasad przy pęknięciu.
Dlaczego to ma znaczenie dla zdrowia i edycji genomu
Mówiąc prościej, praca ta pokazuje, że pęknięte końce DNA nie są biernymi ofiarami czekającymi na naprawę. Ich dokładne kształty, maleńkie łatki dopasowanej sekwencji i chemiczne etykiety aktywnie kierują tym, jak białka naprawcze chwytają, ustawiają i łączą je ponownie. Gdy obecne są trzy lub więcej pasujących zasad, same końce DNA pomagają zablokować pęknięcie w konfiguracji gotowej do naprawy, czasami czyniąc niektóre białkowe pomocniki opcjonalnymi. Gdy takie dopasowania są rzadkie, niezbędne stają się dodatkowe czynniki białkowe. Te spostrzeżenia pomagają wyjaśnić, dlaczego niektóre pęknięcia są naprawiane schludnie, podczas gdy inne prowadzą do małych mutacji lub przestawień. Dają też wskazówki dotyczące ulepszania narzędzi edycji genomu, takich jak CRISPR, gdzie celowo tworzone pęknięcia DNA są naprawiane przez tę samą maszynerię NHEJ. Poprzez dostrojenie końców tych przerw, naukowcy mogą lepiej kontrolować to, jak przebudowywany jest genom.
Cytowanie: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
Słowa kluczowe: naprawa pęknięć dwuniciowych DNA, łączzenie niehomologiczne końców (NHEJ), synapsa DNA, mikrohomologia, stabilność genomu