Clear Sky Science · pl
Pojedyncza zamiana waliny na leucynę zakłóca wiązanie DNA przez AP2-G Plasmodium falciparum i ujawnia rolę GDV1 w aktywacji ap2-g
Jak pasożyty malarii podejmują krytyczną decyzję o życiu lub śmierci
Pasożyty malarii żyjące we krwi człowieka nieustannie stają przed przełomowym wyborem: dalej rozmnażać się wewnątrz jednego gospodarza, czy przejść w formę zdolną przeskoczyć do następnego gospodarza podczas ugryzienia przez komara. Badanie to ujawnia, jak pojedyncza, drobna zmiana w jednym białku pasożyta może całkowicie zablokować tę zakaźną, gotową na komara fazę, otwierając nowe możliwości hamowania przenoszenia malarii.
Rozdroże pasożyta
We krwi, Plasmodium falciparum w większości koncentruje się na szybkim wzroście, co powoduje chorobę. Jednak niewielka część przechodzi w formy płciowe zwane gametocytami — jedyne stadia, które komary mogą pobrać i przekazać dalej. Jak tylko niektóre komórki w populacji dokonują tego przełączenia, pozostawało długo nierozwiązane. Wcześniejsze prace wykazały, że w centrum tej decyzji leżą dwa białka pasożyta: GDV1 i białko wiążące DNA o nazwie AP2-G. GDV1 pomaga „obudzić” zwykle wyciszony gen ap2-g, a AP2-G z kolei włącza zespół genów napędzających rozwój płciowy. Obecne badanie miało zbadać jeszcze jedno białko — kinazę STK2 — lecz zamiast tego natrafiło na znacznie bardziej dramatyczne odkrycie dotyczące samego AP2-G.
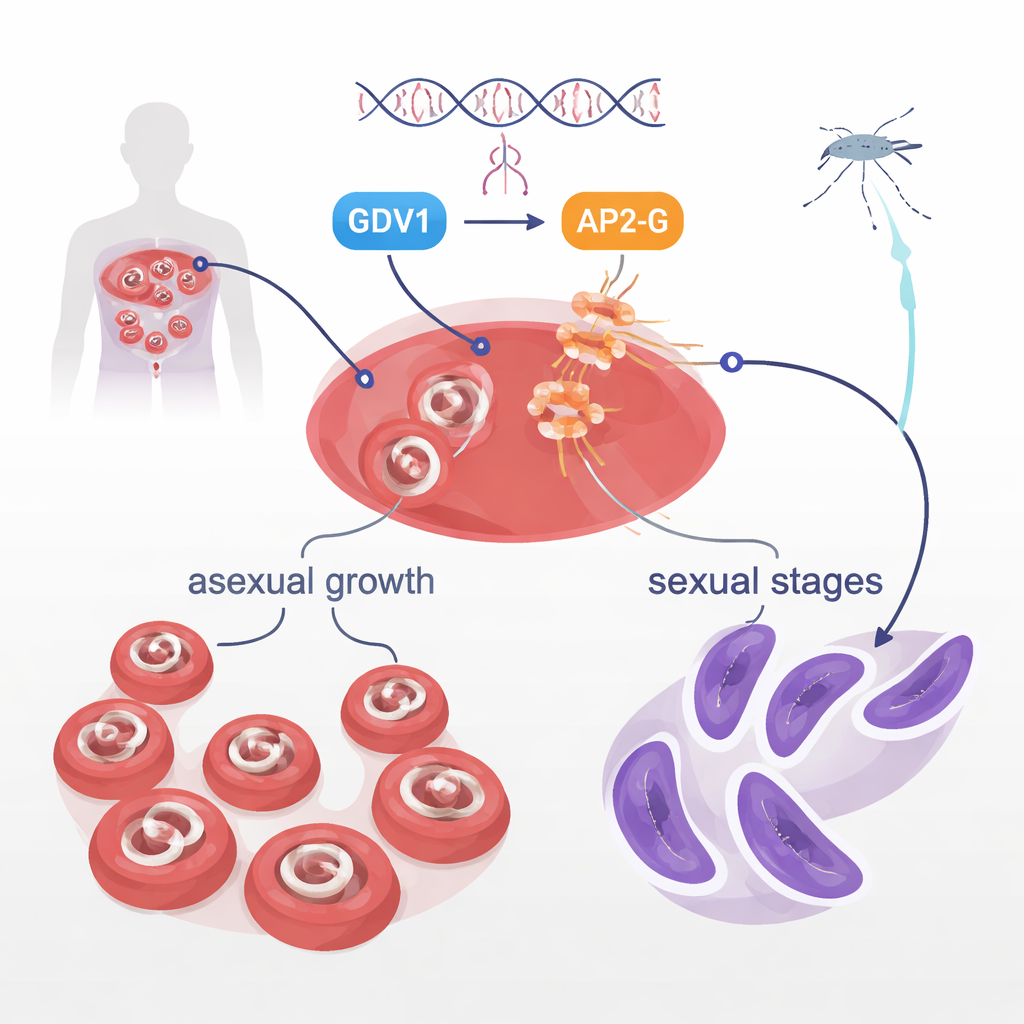
Pojedynczy aminokwas, który zatrzymuje transmisję
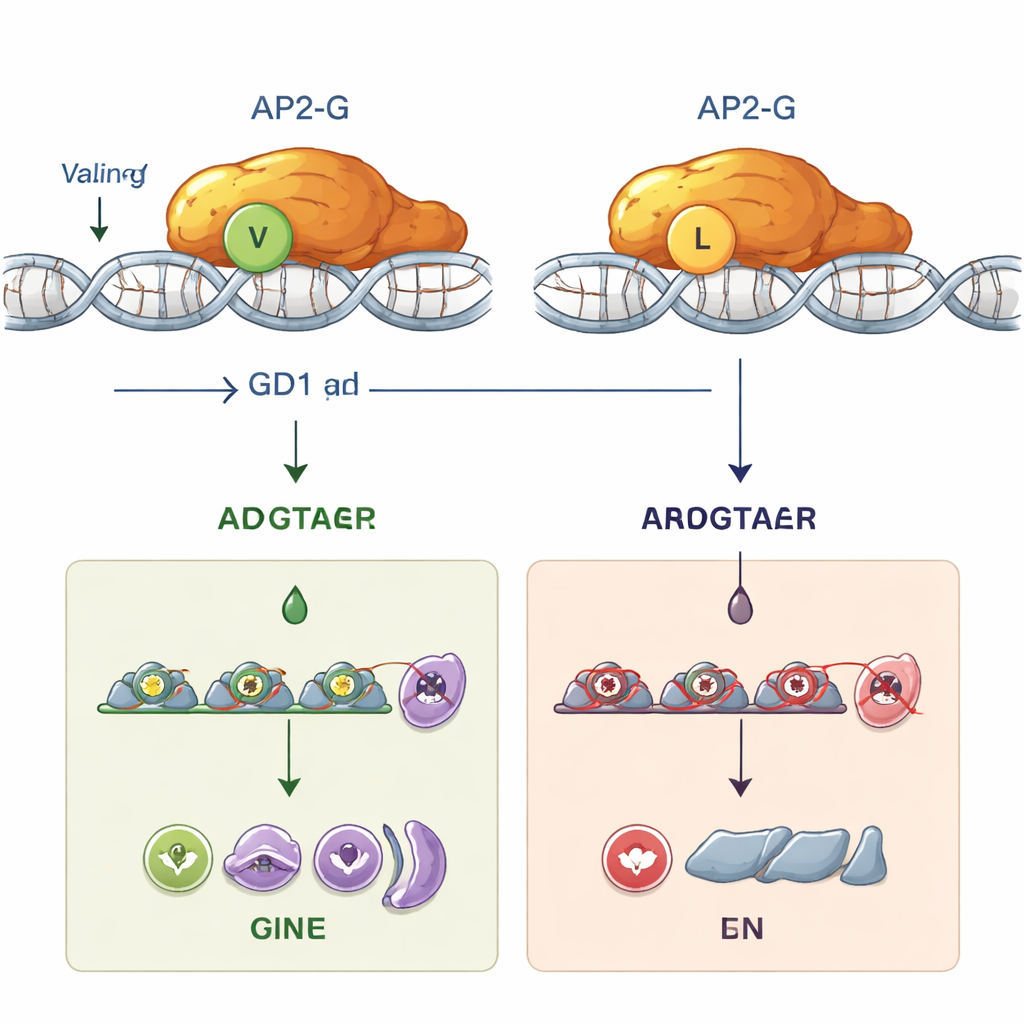
Podczas usuwania genu stk2 w jednej szczepie laboratoryjnym badacze zaobserwowali, że te pasożyty całkowicie utraciły zdolność do wytwarzania gametocytów, mimo że nadal prawidłowo rosły bezpłciowo. Co zaskakujące, powtórzone manipulacje w innym szczepie pozwalały na normalne powstawanie gametocytów. Sekwencjonowanie całego genomu ujawniło ukrytego winowajcę: pojedynczą zmianę „litery” w genie ap2-g, zamieniającą jedną aminokwasową resztę — walinę — na bardzo podobną leucynę w pozycji 2163. Pozycja ta znajduje się na samym początku domeny wiążącej DNA AP2-G, części, która fizycznie chwytuje specyficzne motywy DNA, aby włączać geny. Ta drobna zamiana waliny na leucynę sama w sobie wystarczyła, by zlikwidować formowanie gametocytów. Gdy naukowcy wprowadzili tę mutację do normalnych pasożytów, gametocyty zniknęły; gdy przywrócili walinę, rozwój płciowy został całkowicie odtworzony.
Jak przełączenie łamie molekularny zamek
Aby zrozumieć, dlaczego ta subtelna zmiana jest tak zgubna, zespół połączył modelowanie komputerowe z eksperymentami laboratoryjnymi. Prognozy strukturalne sugerowały, że zastąpienie waliny leucyną przesuwa i destabilizuje precyzyjny kształt domeny wiążącej DNA AP2. W testach in vitro z użyciem oczyszczonych białek normalny AP2-G silnie wiązał preferowaną sekwencję DNA — krótki kod zawierający motyw „GnGTAC”. Natomiast zmutowany AP2-G z leucyną w pozycji 2163 w ogóle nie wiązał tej sekwencji. Bez stabilnego wiązania DNA AP2-G nie był w stanie włączać własnego genu (pętla sprzężenia zwrotnego znana jako autoregulacja) ani aktywować dziesiątek genów podrzędnych potrzebnych do skierowania pasożytów na ścieżkę płciową. Funkcjonalnie zmutowane pasożyty stały się „sterylne”: nie potrafiły wytworzyć form zakaźnych dla komarów, mimo że nadal rozmnażały się w krwinkach czerwonych.
Ukryta rola GDV1 zanim AP2-G przejmie stery
Mutacja dostarczyła także badaczom wyjątkowego narzędzia: pasożyty, w których gen ap2-g można włączyć, ale AP2-G nie potrafi wiązać DNA. Używając reporterów emitujących światło i luminescencję, śledzili, kiedy poszczególne elementy działają w ciągu 48-godzinnego cyklu pasożyta we krwi. Odkryli, że białko GDV1 pojawia się najwcześniej, wczesno w fazie zwanej schizogonią, i jest niezbędne, by uruchomić ekspresję ap2-g z jego wyciszonego stanu. Wczesna aktywacja zachodziła zarówno gdy ap2-g kodował normalny AP2-G, jak i zmutowaną wersję. Dopiero później, gdy zgromadziła się wystarczająca ilość funkcjonalnego AP2-G, nastąpiło silne samonapędzanie i aktywacja innych genów „płciowych”. Kluczowy marker, białko o nazwie MSRP1, zapalał się tylko w pasożytach z funkcjonalnym AP2-G, co dawało wygodny sposób rozróżnienia wczesnych i późnych komórek zaangażowanych w rozwój płciowy. W liniach z mutacją leucynową GDV1 nadal mógł „obudzić” ap2-g, lecz uszkodzone AP2-G nie potrafiło pociągnąć procesu dalej, więc rozwój płciowy utknął.
Znaczenie dla zatrzymania rozprzestrzeniania malarii
Dla czytelnika nieznającego szczegółów wniosek jest prosty: pasożyty malarii polegają na niezwykle czułym molekularnym zamku przy podejmowaniu decyzji o transmisyjności. Badanie pokazuje, że zmiana zaledwie jednego „zęba” w tym zamku — pojedynczej waliny w obszarze AP2-G odpowiedzialnym za chwytanie DNA — uniemożliwia pasożytowi wytworzenie stadiów zakaźnych dla komara. Jednocześnie praca wyjaśnia, że inne białko, GDV1, działa wcześniej jako klucz, najpierw odblokowując wyciszony gen ap2-g, zanim AP2-G wzmocni własną produkcję i uruchomi szeroki program płciowy. Mapując tę sekwencję zdarzeń i tworząc linie pasożytów z reporterami, które świecą na poszczególnych etapach, badanie dostarcza potężnych narzędzi do przesiewu leków lub czynników ludzkich zakłócających zaangażowanie płciowe. W dłuższej perspektywie ukierunkowanie na region wiążący DNA AP2-G lub na krok aktywacji sterowany przez GDV1 może stać się podstawą nowych strategii, które nie tylko leczą malarię u pojedynczego pacjenta, lecz także przerywają łańcuch transmisji.
Cytowanie: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
Słowa kluczowe: przenoszenie malarii, Plasmodium falciparum, rozwój gametocytów, AP2-G, GDV1