Clear Sky Science · pl
Hierarchiczne mechanizmy kontrolują usuwanie zatrzymanej na uszkodzeniu DNA polimerazy RNA II
Gdy maszyny kopiujące geny napotykają przeszkodę
Co sekundę miliony małych maszyn molekularnych zwanych polimerazą RNA II przemieszczają się wzdłuż naszego DNA, przepisyjąc geny na RNA. Gdy jednak DNA jest uszkodzone — na przykład przez ultrafioletowe (UV) światło ze słońca — maszyny te mogą się zatrzymać. Jeśli zatkane kopie się nagromadzą, komórki tracą zdolność prawidłowego odczytywania genów, co jest szczególnie niebezpieczne dla komórek mózgu i może prowadzić do rzadkich chorób, takich jak zespół Cockayne’a. Badanie to szczegółowo ujawnia, jak komórki wyczuwają zablokowane polimerazy i albo je ponownie uruchamiają, albo usuwają, zanim spowodują trwałe szkody.
Nowy sposób obserwowania „korków” w komórkach
Aby zrozumieć, jak komórki usuwają zablokowane polimerazy, badacze zbudowali czasowo-rozdzielczą „kamerę drogową” dla transkrypcji. Użyli leku, który pozwala istniejącym cząsteczkom polimerazy RNA II kontynuować ruch, ale uniemożliwia rozpoczynanie nowych transkrypcji, a następnie stworzyli niewielką strefę uszkodzeń UV w jądrze każdej komórki. Śledząc specyficzny chemiczny znacznik na aktywnej formie polimerazy, mogli obserwować, jak szybko znika ona z uszkodzonego obszaru w porównaniu z resztą genomu. Równolegle opracowali test towarzyszący, który analizował całkowitą ilość aktywnej polimerazy w ekstraktach komórkowych, ujawniając nie tylko moment, kiedy polimerazy znikają z DNA, lecz także kiedy komórka rozkłada je w systemie degradacji.
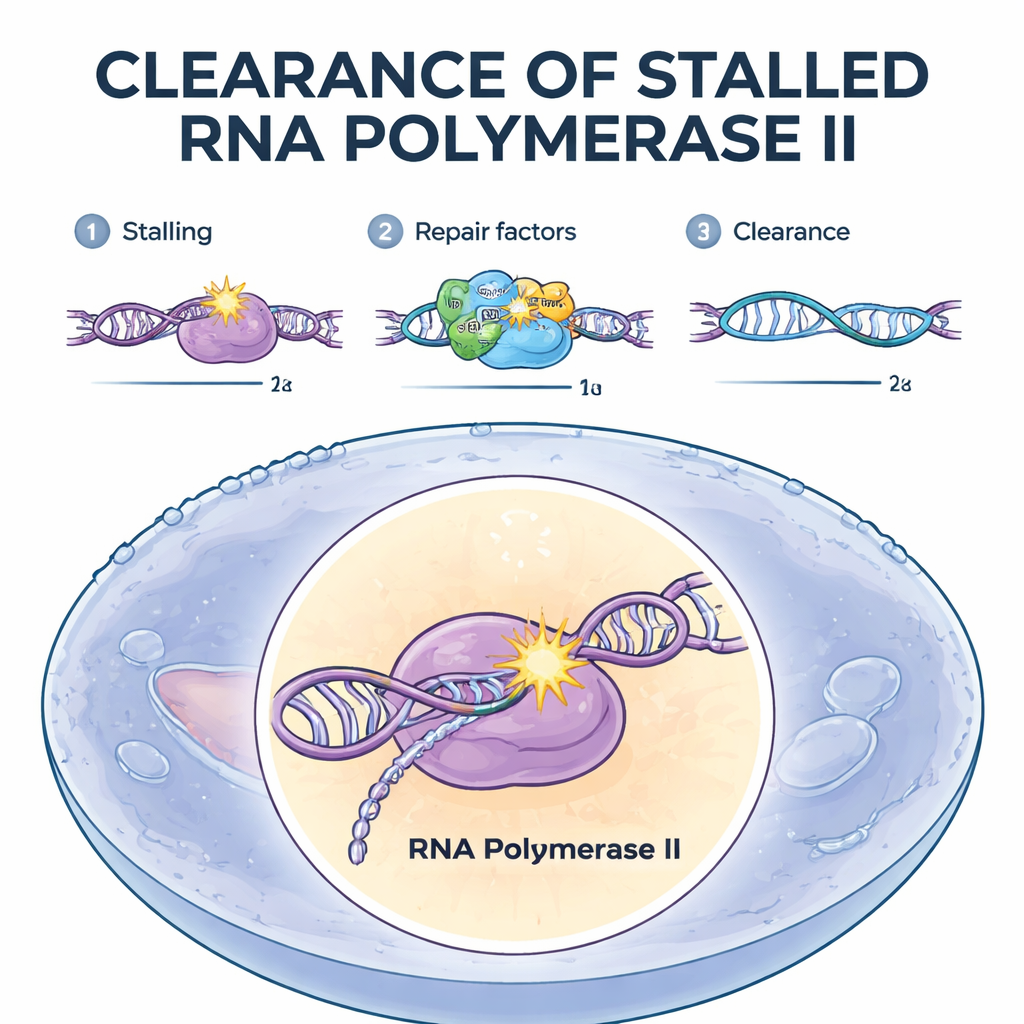
Oznaczanie zatrzymanych maszyn do usunięcia
Zespół skupił się na naprawie sprzężonej z transkrypcją, wyspecjalizowanym systemie naprawczym, który usuwa uszkodzenia na aktywnie odczytywanych genach. Użyli dopasowanej serii ludzkich linii komórkowych, z których każda pozbawiona była innego czynnika naprawczego. Dwa białka, CSB i CSA, okazały się kluczowymi strażnikami. Gdy któregokolwiek z nich brakowało, polimeraza II akumulowała się i uporczywie pozostawała w miejscach uszkodzeń, a komórka nie potrafiła jej zdegenerować. Biochemicznie komórki te nie przyłączały też małych znaczników ubikwityny do kluczowego miejsca na polimerazie. W przeciwieństwie do tego, komórki pozbawione późniejszych białek naprawczych — tych, które wycinają i zastępują uszkodzone DNA — nadal normalnie usuwały polimerazę. To pokazało, że początkowe oznakowanie ubikwityną zatrzymanej polimerazy jest decydującym sygnałem określającym jej los.
Dwie ekipy sprzątające: jedna szybka, druga zapasowa
Po oznaczeniu polimerazy komórka może wybrać jedną z dwóch dróg jej usunięcia. Główna, szybka trasa opiera się na dużym kompleksie naprawczym zwanym TFIIH, a w szczególności na jego podjednostce helikazowej XPD, która zużywa energię do rozwijania DNA. Białka pomocnicze, w tym ELOF1, UVSSA i STK19, przyprowadzają TFIIH do zablokowanej polimerazy i ustawiają XPD na DNA tuż przed nią. Przy użyciu nowych testów w komórkach pacjentów niosących mutację XPD pozbawiającą helikazy autorzy pokazali, że gdy XPD nie potrafi rozwijać DNA, usuwanie polimerazy dramatycznie zwalnia, mimo obecności pozostałych elementów aparatu naprawczego. Wskazuje to, że mechaniczne działanie XPD jest tym, co zwykle „potrząsa” polimerazą i uwalnia ją z uszkodzenia, aby enzymy naprawcze mogły dotrzeć do zniszczonego miejsca.
Wolny, ale istotny plan B
Badanie ujawniło także wolniejszą, awaryjną ścieżkę usuwania zatrzymanej polimerazy. Droga ta zależy od VCP (znanego także jako p97), białka rozpoznającego znaczniki ubikwityny i potrafiącego siłowo wyciągać białka z chromatyny. W zdrowych komórkach z w pełni funkcjonującym TFIIH zablokowanie VCP miało jedynie niewielki efekt. Jednak w komórkach, w których TFIIH był nieobecny, źle ustawiony lub pozbawiony aktywności helikazy, usuwanie polimerazy stało się niemal całkowicie zależne od VCP. W takich sytuacjach VCP wciąż potrafił wyciągnąć oznakowaną polimerazę z DNA, nawet gdy normalna naprawa nie mogła postąpić dalej. Co kluczowe, trasa zapasowa wciąż wymagała pewnego oznakowania ubikwityną, co wyjaśnia, dlaczego komórki pozbawione CSB lub CSA — a tym samym znaczników ubikwityny — zawodzą zarówno w głównej, jak i zapasowej ścieżce.
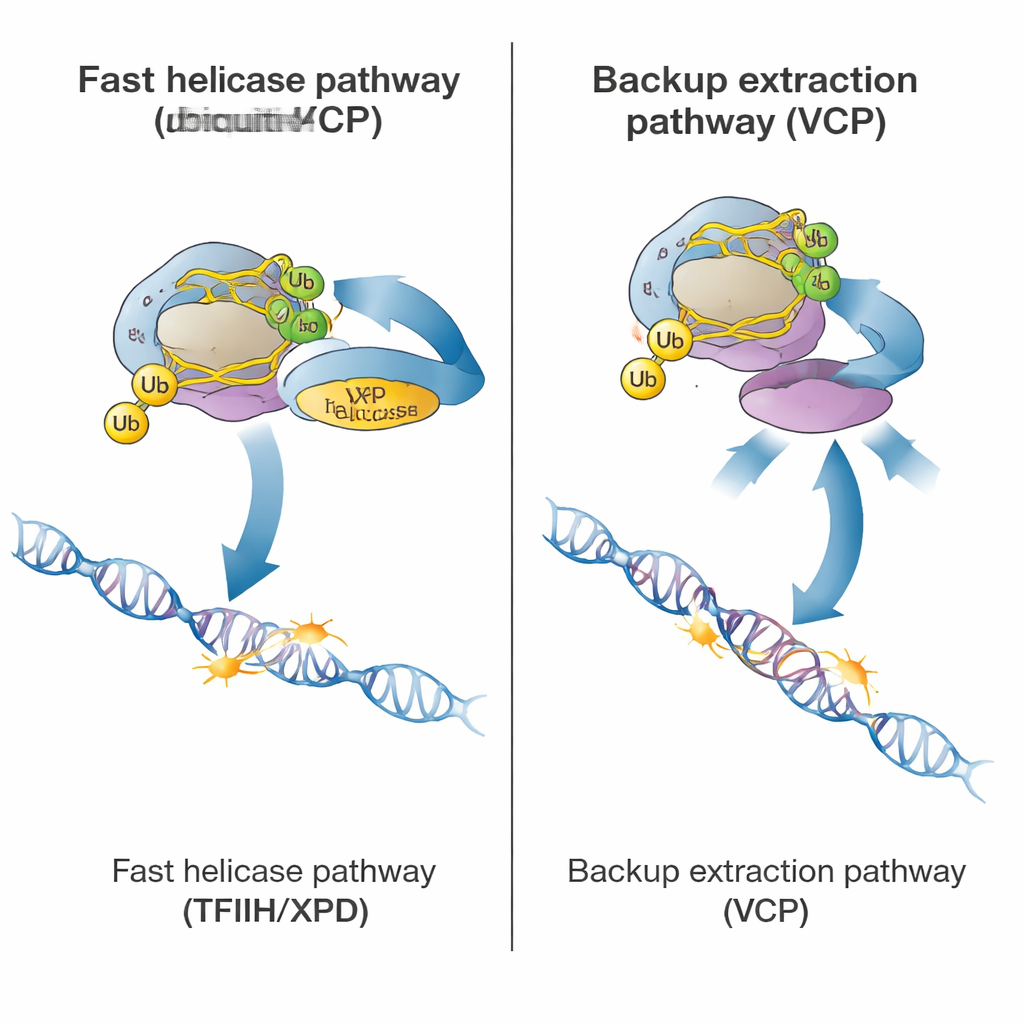
Dlaczego to ma znaczenie dla zdrowia i chorób
W całości praca opisuje hierarchiczny program bezpieczeństwa, którego komórki używają za każdym razem, gdy polimeraza RNA II natrafia na uszkodzenie DNA. Najpierw CSB i CSA oznaczają zatrzymaną maszynę za pomocą ubikwityny. Jeśli wszystko działa prawidłowo, TFIIH i jego helikaza XPD szybko wysuwają polimerazę, aby uszkodzenie mogło zostać wycięte i naprawione. Jeśli TFIIH nie może wykonać swojej funkcji, VCP wkracza, by wydobyć polimerazę i skierować ją do degradacji, zapobiegając zablokowaniu ekspresji genów, choć samo uszkodzenie DNA pozostaje. Ten schemat pomaga wyjaśnić, dlaczego dziedziczne defekty w CSB lub CSA powodują szczególnie ciężkie problemy neurologiczne: bez oznakowania ubikwityną komórki tracą zarówno główną drogę naprawczą, jak i zapasową drogę ekstrakcji, pozostawiając zatrzymane polimerazy przyklejone do uszkodzonych genów i prowadząc do przewlekłego zablokowania transkrypcji.
Cytowanie: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
Słowa kluczowe: naprawa DNA sprzężona z transkrypcją, polimeraza RNA II, uszkodzenia DNA wywołane promieniowaniem UV, ubikwitynacja białek, zespół Cockayne’a