Clear Sky Science · pl
Wizualizacja in situ heterogenności fenotypowej i morfologii pojedynczych komórek Clostridioides difficile podczas zakażenia jelit
Dlaczego bakterie jelitowe nie zachowują się jednakowo
Clostridioides difficile, często nazywany C. diff, to niesławny drobnoustrój szpitalny, który może powodować ciężką, czasem zagrażającą życiu biegunkę po zaburzeniu równowagi normalnej flory jelitowej przez antybiotyki. Nawet jeśli te bakterie są genetycznie identyczne i żyją w tym samym środowisku, pojedyncze komórki mogą zachowywać się bardzo różnie. Badanie to ujawnia z bezprecedensową dokładnością, jak pojedyncze komórki C. diff włączają lub wyłączają produkcję toksyn, a nawet zmieniają kształt podczas zakażenia jelita myszy, dając wskazówki, dlaczego choroba bywa tak uporczywa i trudna do leczenia.
Śledzenie groźnego najeźdźcy jelit w czasie rzeczywistym
Aby zrozumieć, jak pojedyncze komórki C. diff zachowują się wewnątrz organizmu, badacze potrzebowali sposobu, by wyraźnie je zobaczyć w gęstej i różnorodnej społeczności mikrobiomu jelitowego. Zaprojektowali szczepy C. diff, które świecą jasnymi kolorami pod mikroskopem, wykorzystując specjalne białka fluorescencyjne, które nie zakłócają zdolności bakterii do wzrostu ani wywoływania choroby. Zakażając myszy poddane antybiotykoterapii tymi świecącymi szczepami, a następnie krojąc i barwiąc okrężnicę, mogli określić dokładne położenie i zachowania tysięcy pojedynczych komórek bakteryjnych w nienaruszonej tkance jelita. 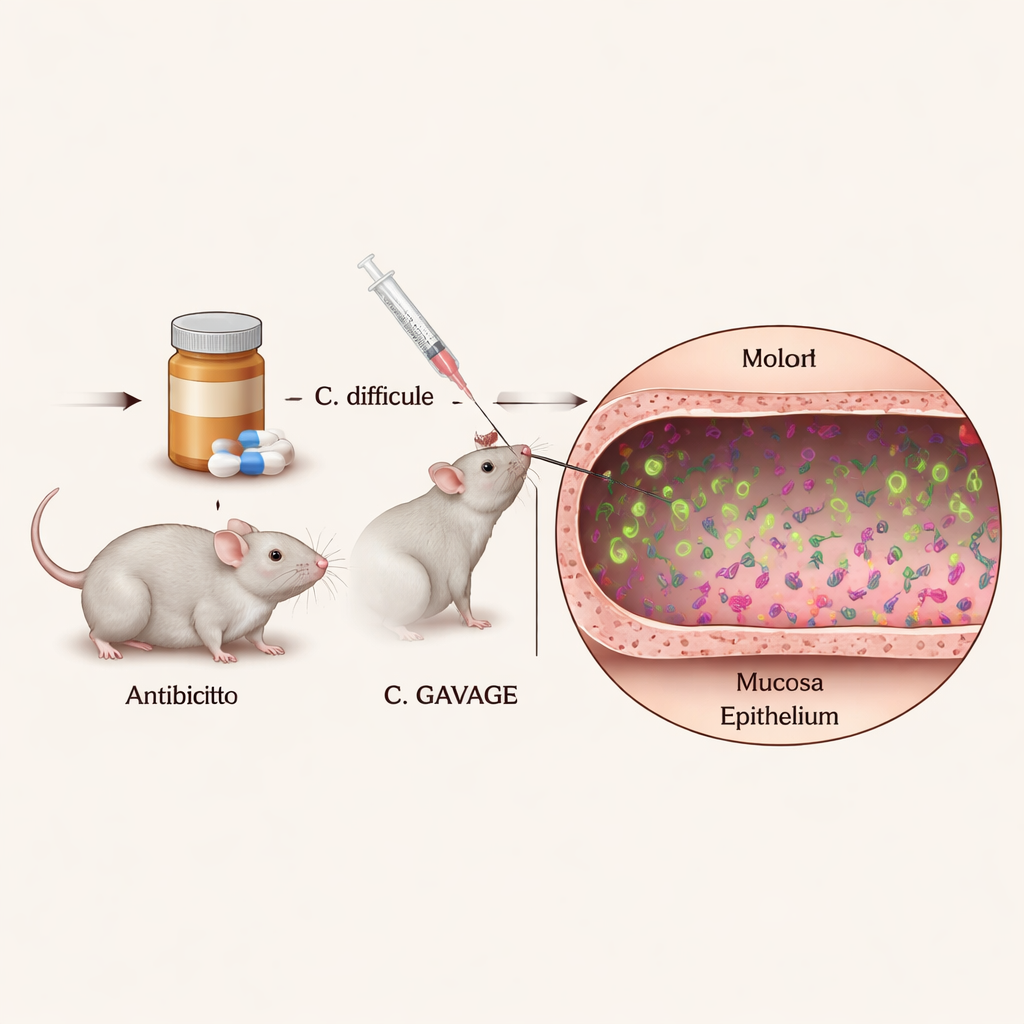
Gdzie bakterie żyją w okrężnicy
Obrazy pokazały, że większość komórek C. diff znajduje się w centrum treści jelitowej, zwanej światłem jelita (lumen), potwierdzając, że organizm ten jest głównie wolnopływającym patogenem „luminalnym”. Jednak zauważalna mniejszość komórek konsekwentnie występowała w pobliżu warstwy śluzu i bezpośrednio obok nabłonka — cienkiej warstwy komórek wyściełającej okrężnicę i pełniącej rolę bariery. Ta podpopulacja stykająca się bezpośrednio z nabłonkiem nie była wcześniej wyraźnie widoczna u konwencjonalnych myszy z prawidłowym układem odpornościowym. Co ważne, wprowadzone znaczniki fluorescencyjne nie osłabiły zauważalnie bakterii u zwierząt, co sugeruje, że obrazy prawdopodobnie odzwierciedlają rzeczywiste zachowanie C. diff podczas infekcji.
Kto produkuje toksynę i gdzie?
Zespół dodał następnie drugi sygnał fluorescencyjny, który włącza się tylko wtedy, gdy C. diff aktywuje geny toksyn. Toksyny to uszkadzające białka, które ranią wyściółkę jelita i powodują objawy choroby; są też tym, co lekarze mierzą w badaniach stolca, aby rozpoznać zakażenie. Ku zaskoczeniu, bakterie nie produkowały toksyn jednocześnie. Raczej tylko część komórek świeciła jako „toksyna-ON” w danym momencie, zarówno we wczesnej, jak i późnej fazie zakażenia. Ten odsetek był wyższy w szczepie-mutancie genetycznie zaprogramowanym do nadprodukcji toksyny, ale nawet tam nie wszystkie komórki uczestniczyły. Równie uderzające było to, że pozycja komórki — unosząca się w świetle jelita, osadzona w śluzie czy stykająca się z nabłonkiem — nie zmieniała znacząco ani częstości produkcji toksyny, ani siły włączenia tych genów. 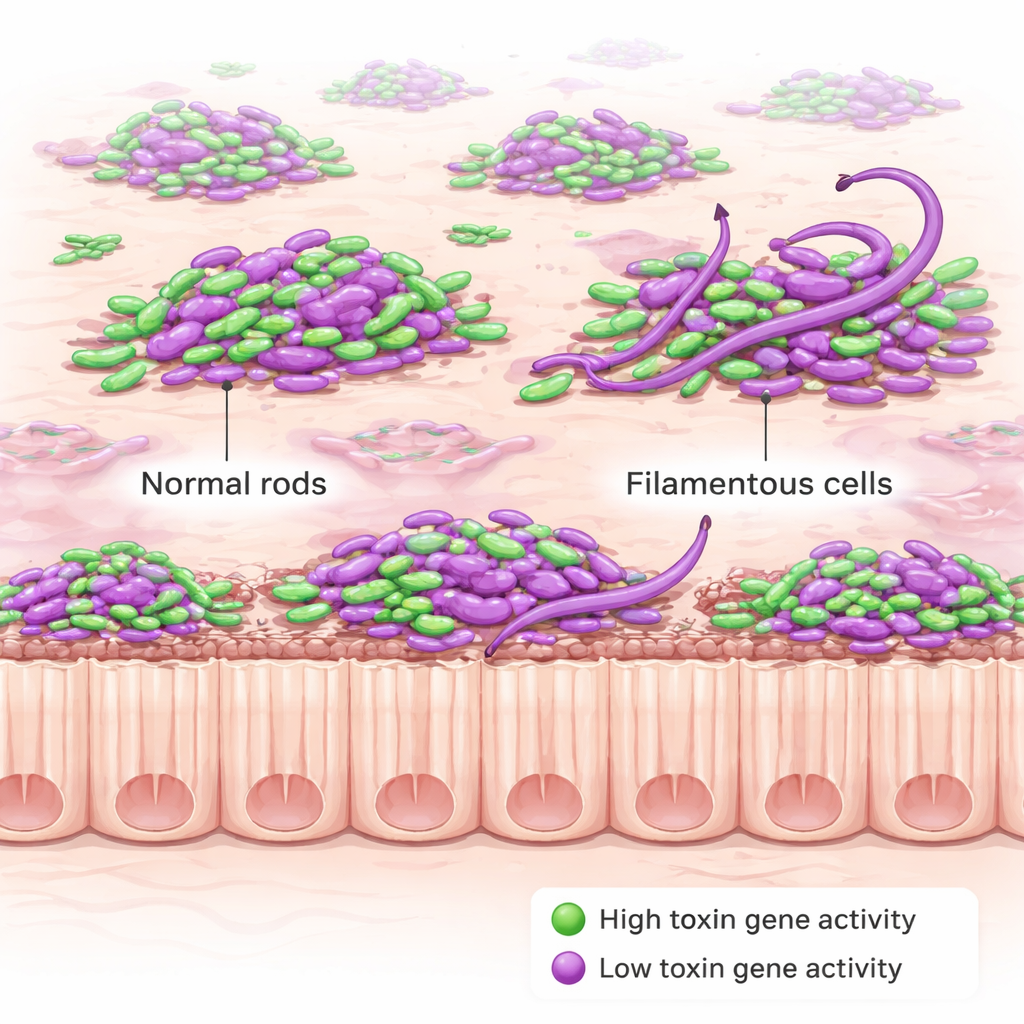
Komórki zmieniające kształt pod wpływem stresu
Podczas mapowania produkcji toksyn badacze natrafili na zaskakujące nowe zachowanie. U myszy zakażonych mutacyjnym szczepem nadprodukującym toksynę wiele komórek C. diff w ostrej fazie choroby stało się niezwykle długimi, zakrzywionymi filamentami, niektóre ponad dziesięć razy dłuższe od normalnych krótkich pręcików. Ta „strunowata” morfologia występowała głównie we wczesnym, ciężkim etapie zakażenia i zanikała później; nie pojawiała się, gdy ten sam szczep był hodowany w pożywce laboratoryjnej. To sugeruje, że stresujące warunki w zapalnym jelicie — a nie tylko zmiany genetyczne — wyzwalają tę dramatyczną przemianę. Dalsze eksperymenty wykazały, że utrata białka regulatorowego o nazwie RstA, które kontroluje zarówno geny toksyn, jak i inne odpowiedzi na stres, sprzyja tworzeniu takich filamentów.
Co to oznacza dla choroby wywoływanej przez C. diff
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że nawet pojedynczy szczep C. diff zachowuje się jak podzielony zespół roboczy. Niektóre komórki ponoszą koszt energetyczny produkcji toksyny i uszkadzania jelita, uwalniając składniki odżywcze, z których korzystają ich wolne od toksyn sąsiedzi. Taka wspólna „podział pracy” może pomagać infekcji przetrwać i nawracać, ponieważ nie każda komórka jest jednakowo wrażliwa na terapie celujące w toksynę lub w szybko rosnące bakterie. Nowo opracowany system reporterów fluorescencyjnych daje naukowcom potężne narzędzie do obserwowania, komórka po komórce, jak C. diff i powiązane mikroby jelitowe adaptują się w czasie i przestrzeni wewnątrz organizmu. Ta wiedza może w końcu pomóc w opracowaniu terapii skierowanych nie tylko na zabijanie bakterii, ale na zakłócanie szkodliwych ról konkretnych subpopulacji, które napędzają chorobę i nawroty.
Cytowanie: DiBenedetto, N.V., Donnelly-Morell, M.L., Kumamoto, C.A. et al. In situ visualization of Clostridioides difficile phenotypic heterogeneity and single-cell morphology during gut infection. Nat Commun 17, 1716 (2026). https://doi.org/10.1038/s41467-026-68411-6
Słowa kluczowe: Clostridioides difficile, mikrobiom jelitowy, toksyny bakteryjne, heterogenność fenotypowa, obrazowanie fluorescencyjne