Clear Sky Science · pl
Nanosystem celujący w inhibitor tkankowy metaloproteinaz‑1 do ciągłej terapii idiopatycznego włóknienia płuc w ujęciu czasowo‑przestrzennym
Dlaczego uporczywe bliznowacenie płuc ma znaczenie
Idiopatyczne włóknienie płuc (IPF) to nieustępliwa choroba płuc, w której normalna, gąbczasta tkanka płuc stopniowo zostaje zastępowana sztywną tkanką bliznowatą. Osoby z IPF odczuwają duszność przy codziennych czynnościach, a większość przeżywa tylko kilka lat od rozpoznania. Obecne leki mogą u niektórych spowalniać przebieg choroby, ale rzadko cofają już istniejące blizny i często powodują działania niepożądane. W tym badaniu analizowano inteligentną, wziewną „nano‑terapię” zaprojektowaną nie tylko do hamowania IPF, lecz także do aktywnego usuwania blizn i wspierania naprawy płuc.
Problem: lepkie blizny i stres chemiczny
W IPF przestrzenie, w których tlen normalnie przenika do krwi, wypełniają się nadmiarem białek takich jak kolagen, zamieniając elastyczne pęcherzyki płucne w sztywne ogniska. Autorzy skupili się na białku zwanym TIMP‑1, które działa jak hamulec dla naturalnych enzymów rozkładających nadmiar kolagenu. Analiza próbek płuc od pacjentów i od myszy z wywołanym włóknieniem wykazała, że poziomy TIMP‑1 były wielokrotnie wyższe niż w płucach zdrowych i rosną wraz z odkładaniem kolagenu. Równocześnie uszkodzone płuca wykazywały wzrost poziomów reaktywnych form tlenu (ROS) — chemicznych „iskier”, które uszkadzają komórki — oraz utratę kluczowych markerów zdrowych komórek wyściełających pęcherzyki płucne. Razem te obserwacje wskazują na błędne koło: nadmiar TIMP‑1 hamuje rozkład blizn, a stres oksydacyjny dodatkowo uszkadza strukturę płuca.
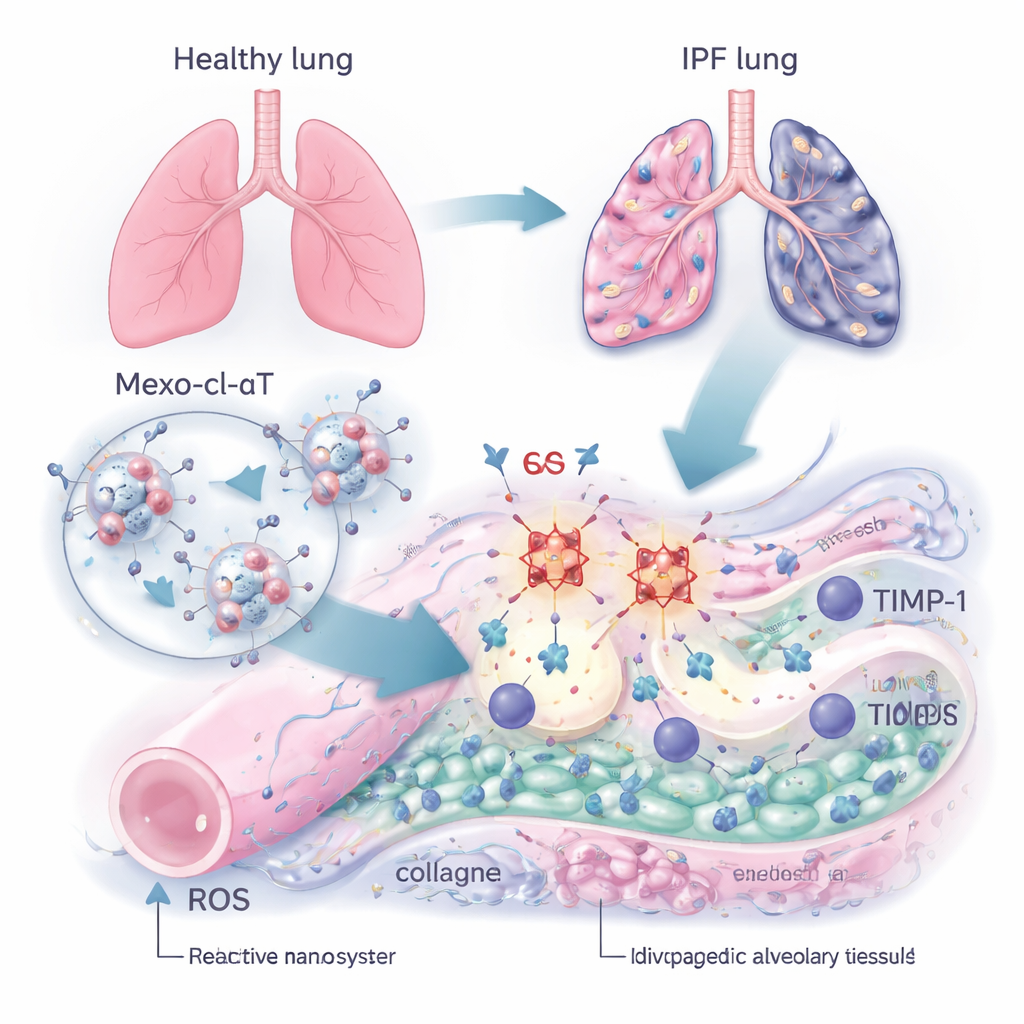
Inteligentny nośnik: maleńkie pakiety naprawcze
Aby przerwać to koło, zespół skonstruował nanoskalową terapię nazwaną Mexo‑cl‑aT. Zaczęli od egzosomów — naturalnych, pęcherzykowatych cząstek uwalnianych przez komórki macierzyste, które wykazują tendencję do kierowania się ku uszkodzonym tkankom i wspierania regeneracji. Na powierzchnię tych egzosomów przytwierdzili przeciwciała wiążące się specyficznie z TIMP‑1. Połączenie między egzosomem a przeciwciałem wykonano przy użyciu specjalnego chemicznego łącznika, który może być przecięty przez ROS. Innymi słowy, surowe chemiczne środowisko zbliznowaciałego płuca służy jako sygnał: gdy egzosom dociera do uszkodzonego obszaru bogatego w ROS, łącznik pęka, pochłaniając część ROS i uwalniając przeciwciało dokładnie tam, gdzie występuje dużo TIMP‑1, podczas gdy sam egzosom dalej wspiera naprawę tkanki.
Jak zachowuje się i działa nanosystem
W badaniach komórkowych badacze wykazali, że Mexo‑cl‑aT pozostaje stabilny w płynach, ale szybko uwalnia przeciwciała po wystawieniu na stężenia nadtlenku wodoru podobne do tych występujących w chorych płucach. Równocześnie znacznie obniża on ilość nadtlenku, potwierdzając swoją rolę jako środek oczyszczający ROS. W modelach komórkowych przypominających blizny uwolnione przeciwciała zmniejszały poziomy TIMP‑1 i uwalniały enzymy rozkładające kolagen, podczas gdy składnik egzosomowy ograniczał śmierć komórek, pobudzał wzrost komórek i przyspieszał zamykanie ran zarówno w komórkach płucnych, jak i śródbłonka naczyń. W porównaniu z wersjami, w których łącznik nie mógł zostać przecięty, projekt reaktywny na ROS usuwał więcej kolagenu i skuteczniej redukował stres chemiczny, podkreślając znaczenie kontrolowanego uwalniania.
Testy w modelu zaawansowanego bliznowacenia płuc
Zespół następnie przetestował terapię na myszach z zaawansowanym włóknieniem płuc wywołanym lekiem bleomycyną — modelu wybranym, by naśladować stadium zaawansowane IPF. Pojedyncza dawka wziewnego Mexo‑cl‑aT utrzymywała się w płucach przez dni i wiązała więcej przeciwciała niż proste połączenie jego składników. Leczone płuca wyglądały zdrowiej zarówno gołym okiem, jak i pod mikroskopem: przestrzenie powietrzne się ponownie otworzyły, grubość blizn zmniejszyła się, a całkowita zawartość kolagenu niemal wróciła do normy. Markery aktywowanych komórek tworzących blizny spadły, podczas gdy białka związane ze zdrowymi komórkami wyściełającymi pęcherzyki i naczynia krwionośne wzrosły. Pomiary chemiczne wykazały, że leczenie ostro obniżyło poziomy TIMP‑1, przywróciło równowagę enzymów rozkładających kolagen i usunęło około trzech czwartych nadmiaru ROS. Co ważne, wskaźniki stanu zapalnego zmalały, a badania krwi i oględziny narządów nie wykazały oczywistej toksyczności.
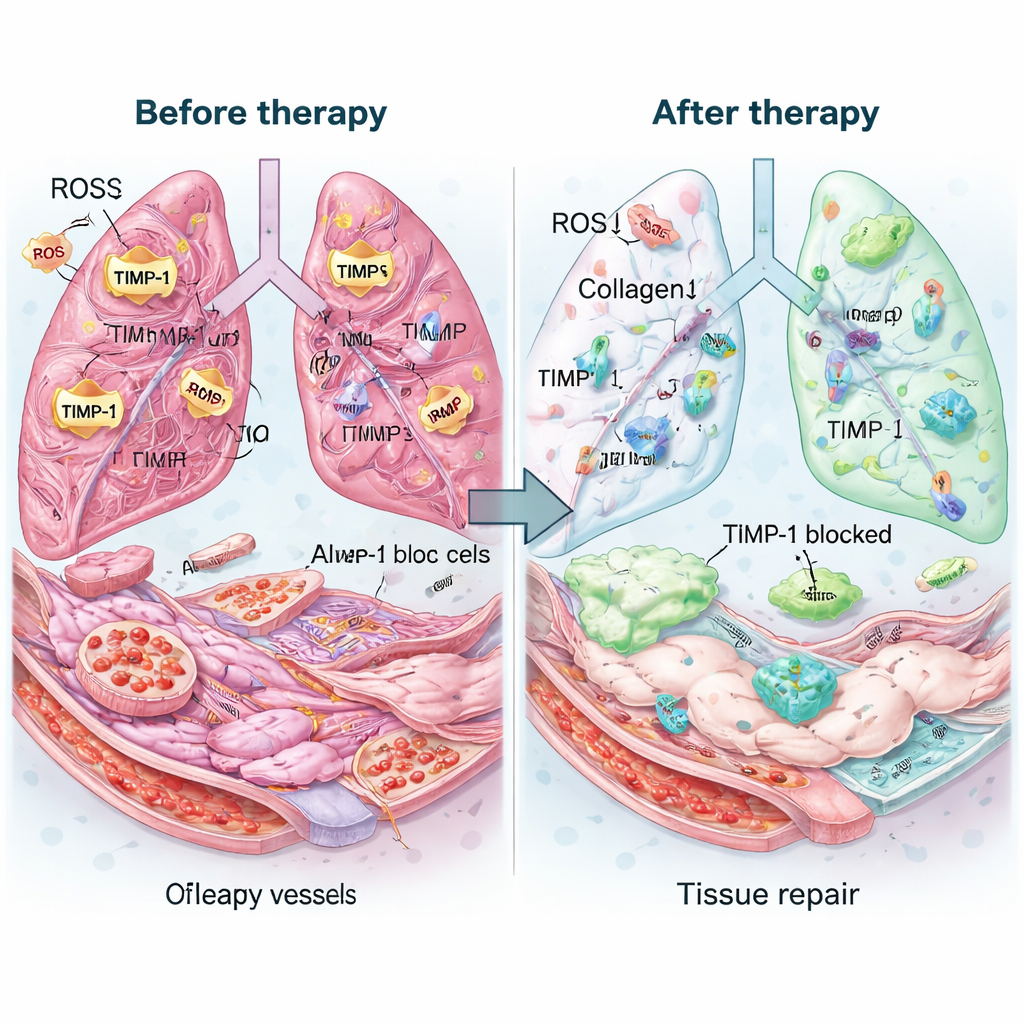
Co to może znaczyć dla pacjentów
Dla osób żyjących z IPF ta praca jeszcze nie oferuje natychmiastowego wyleczenia, ale przedstawia obiecującą strategię. Zamiast jedynie spowalniać nowe uszkodzenia, nanosystem Mexo‑cl‑aT ma na celu aktywne cofanie istniejących blizn, łagodzenie szkodliwego stresu chemicznego i wspieranie odbudowy kruchej tkanki płucnej — wszystko w ukierunkowanej, wziewnej formie, która koncentruje leczenie tam, gdzie jest najbardziej potrzebne. Choć wyzwania takie jak produkcja egzosomów na dużą skalę i testy na ludziach pozostają, badanie sugeruje, że precyzyjne nano‑terapie dostosowane do patologicznego środowiska mogą pewnego dnia zrewolucjonizować leczenie uporczywego bliznowacenia płuc, a być może także innych chorób włóknieniowych.
Cytowanie: Li, C., Lu, G., Chen, H. et al. A nanosystem targeting tissue inhibitor of metalloproteinase-1 for continuous spatiotemporal idiopathic pulmonary fibrosis therapy. Nat Commun 17, 1694 (2026). https://doi.org/10.1038/s41467-026-68398-0
Słowa kluczowe: idiopatyczne włóknienie płuc, bliznowacenie płuc, nanomedycyna, terapia egzosomowa, TIMP‑1