Clear Sky Science · pl
Stany uszkodzonych komórek nabłonkowych wpływają na przeżywalność przeszczepu nerki po odrzuceniu zależnym od limfocytów T
Dlaczego te badania nad nerką są ważne dla pacjentów
Przeszczepy nerek mogą ratować życie, ale wiele z nich kończy się niepowodzeniem po latach, nawet gdy lekarze wydają się kontrolować reakcję immunologiczną zwaną odrzuceniem zależnym od limfocytów T. Badanie stawia proste, lecz kluczowe pytanie: jeśli reakcja immunologiczna wygląda „wyleczona” pod mikroskopem, dlaczego niektóre przeszczepione nerki i tak szybciej się zużywają? Przez przyjrzenie się pojedynczym komórkom w przeszczepionych nerkach myszy i ludzi, badacze odkrywają ukrytą warstwę uszkodzeń w obrębie kanalików filtracyjnych, co pomaga wyjaśnić, które przeszczepy przeżywają, a które nie.
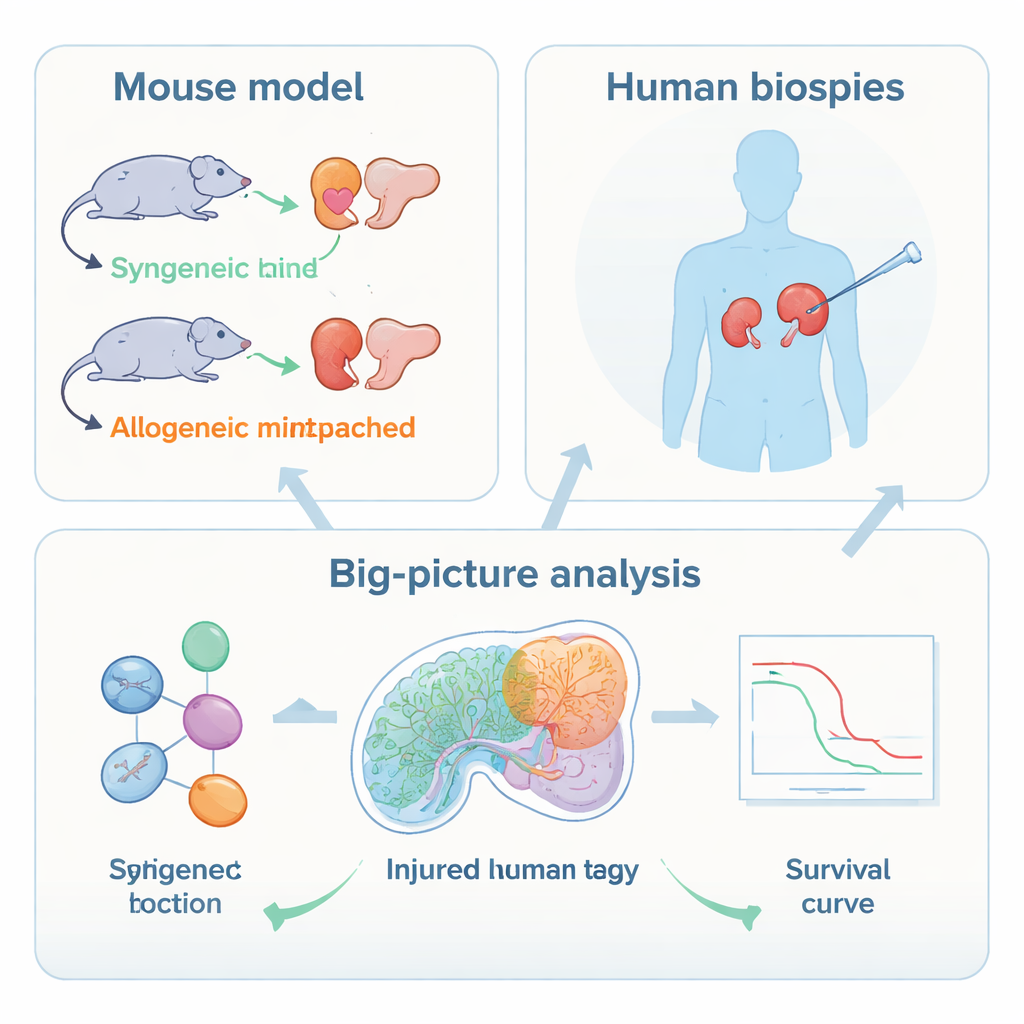
Patrząc poza klasyczne objawy odrzucenia
Lekarze zwykle rozpoznają odrzucenie zależne od limfocytów T po stwierdzeniu nacieku białokrwinkowego w nerce i ataku na drobne kanaliki zaangażowane w przetwarzanie moczu. Silne leki przeciwodrzutowe często mogą wypędzić te komórki immunologiczne i poprawić wygląd biopsji. Mimo to pacjenci z tym typem odrzucenia nadal są obciążeni wysokim ryzykiem uszkodzenia przeszczepu. Wcześniejsze badania na dużą skalę sugerowały, że sygnały uszkodzenia tkanki wewnątrz komórek nerkowych przewidują wynik lepiej niż miary liczby komórek immunologicznych. Autorzy postanowili zdefiniować te sygnały uszkodzenia z rozdzielczością pojedynczej komórki i sprawdzić, jak ściśle wiążą się one z długoterminową przeżywalnością przeszczepu.
Analiza odrzucenia komórka po komórce
Zespół najpierw użył kontrolowanego modelu mysiego, transplantując nerki albo między genetycznie identycznymi myszami, albo między różnymi szczepami, aby wywołać odrzucenie. Następnie zastosowali sekwencjonowanie RNA z pojedynczych jąder (single‑nucleus RNA sequencing), które odczytuje aktywność tysięcy genów w pojedynczych komórkach, oraz transkryptomikę przestrzenną, która pokazuje, gdzie te komórki znajdują się w przekroju tkanki. Te narzędzia ujawniły, że podczas odrzucenia najsilniejsze zmiany molekularne zachodzą nie w komórkach odpornościowych, lecz we własnych komórkach nabłonkowych nerki wyściełających kanaliki proksymalne i odcinek zwany grubą częścią wstępującą ramienia pętli Henlego. W tych obszarach komórki włączały geny związane z urazem i stresem, sygnały zapalne oraz markery bardziej prymitywnego, mniej wyspecjalizowanego stanu, przy jednoczesnym obniżeniu funkcji transportowych niezbędnych do prawidłowej filtracji.
Ukryte ogniska ciężko uszkodzonych komórek kanalikowych
Klasteryzując komórki o podobnej aktywności genów, badacze odkryli kilka odrębnych „stanów uszkodzenia” wśród komórek kanalikowych w nerkach mysich. Niektóre odzwierciedlały wczesne reakcje stresowe, podczas gdy inne reprezentowały silnie uszkodzone, mocno zmienione komórki, które utraciły normalną tożsamość i produkowały liczne molekuły zapalne oraz związane z bliznowaceniem. Mapowanie przestrzenne pokazało, że te stany nie rozkładały się równomiernie: pewne ciężkie stany uszkodzenia tworzyły łatkowe ogniska w korze i zewnętrznej części rdzenia nerki i występowały w złożonych sąsiedztwach z limfocytami T, makrofagami i fibroblastami. Dla kontrastu, niektóre uszkodzone komórki w głębszych rejonach były zaskakująco odizolowane od komórek odpornościowych, co sugeruje różne mechanizmy powstawania i utrzymywania się uszkodzeń.
Przyporządkowanie mysich stanów uszkodzenia do przeszczepów ludzkich
Autorzy zapytali następnie, czy podobne stany komórkowe występują u ludzi. Przeanalizowali biopsje z ludzkich przeszczepów nerek z aktywnym odrzuceniem zależnym od limfocytów T oraz z przeszczepów stabilnych. Dane z pojedynczych komórek ponownie ujawniły uszkodzone komórki cewek proksymalnych i grubej części wstępującej, których wzorce genowe ściśle odpowiadały najciężej uszkodzonym stanom komórek mysich. Wykorzystując te ludzkie sygnatury, zespół „dekonwolucjonował” tysiące starszych profili ekspresji genów uzyskanych z mieszanin tkanek (bulk) i stwierdził, że ciężkie stany uszkodzenia cewek występowały częściej w odrzuceniu zależnym od limfocytów T oraz w odrzuceniu mieszanym niż w odrzuceniu wyłącznie przeciwciałowym lub braku odrzucenia. Co ważne, opracowali zwarte zestawy genów reprezentujące każdy stan uszkodzenia i oceniali je w dużej kohorcie z długim okresem obserwacji.
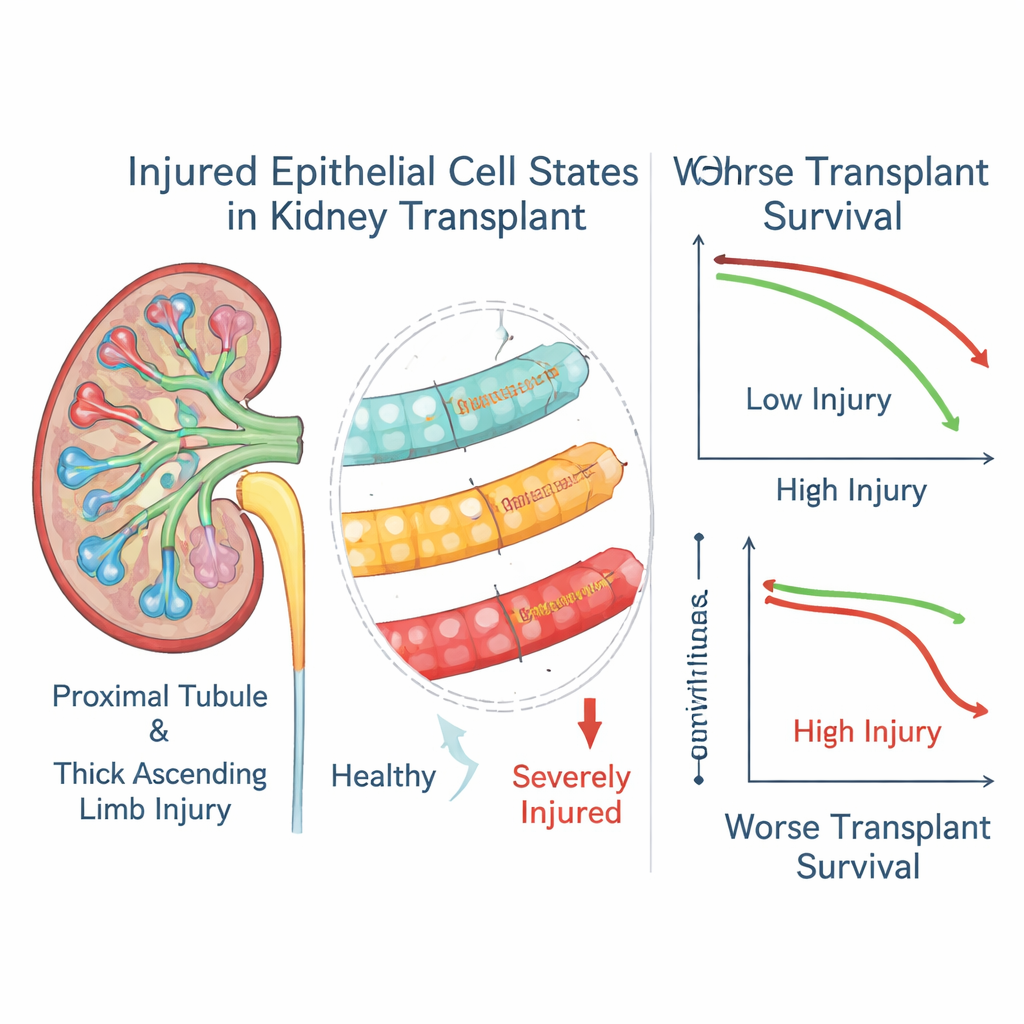
Uszkodzone komórki kanalikowe jako predyktory losu przeszczepu
Gdy autorzy powiązali te wyniki genowe ze stanem klinicznym po trzech latach u ponad tysiąca biorców przeszczepów, wyłonił się wyraźny schemat. Wysoki poziom markerów najbardziej ciężkich stanów nabłonkowych zarówno w kanaliku proksymalnym, jak i w grubej części wstępującej silnie wiązał się z wyższym ryzykiem utraty przeszczepu, nawet wśród pacjentów, których biopsje były inaczej klasyfikowane jako wyleczone odrzucenie. Łagodniejszy stan uszkodzenia cewek wykazywał przeciwny trend i był związany z lepszą przeżywalnością, co sugeruje, że może reprezentować skuteczniejszy program naprawczy. W podgrupie pacjentów z powtarzanymi biopsjami, oceny „ciężkiego uszkodzenia” często pozostawały wysokie długo po tym, jak epizod odrzucenia pozornie ustąpił, co sugeruje, że te zmienione komórki mogą utrzymywać się i nadal wpływać na przebieg choroby.
Co to oznacza dla opieki nad przeszczepem
Dla osób niebędących specjalistami kluczowe przesłanie jest takie, że nie całe uszkodzenie w odrzuconej nerce pochodzi bezpośrednio od komórek odpornościowych i nie wszystkie urazy znikają, gdy atak immunologiczny ucichnie. Badanie pokazuje, że uporczywe ogniska mocno uszkodzonych komórek kanalikowych działają jak wczesny system ostrzegawczy przed przyszłą utratą przeszczepu. W dłuższej perspektywie proste testy oparte na tych genowych sygnaturach uszkodzenia — być może nawet wykorzystujące komórki złuszczane do moczu — mogą pomóc lekarzom zidentyfikować pacjentów wysokiego ryzyka, dostosować leczenie i monitorować, czy nerki naprawdę się regenerują. Praca wskazuje również na te uszkodzone komórki nabłonkowe jako potencjalne cele nowych terapii mających na celu ochronę przeszczepionych nerek poza standardową immunosupresją.
Cytowanie: Pfefferkorn, A.M., Jahn, L., Gauthier, P.T. et al. Injured epithelial cell states impact kidney allograft survival after T-cell-mediated rejection. Nat Commun 17, 1060 (2026). https://doi.org/10.1038/s41467-026-68397-1
Słowa kluczowe: odrzucenie przeszczepu nerki, uszkodzenie komórek cewek, sekwencjonowanie pojedynczych komórek, przeżywalność przeszczepu, stany komórek nabłonkowych