Clear Sky Science · pl
Modelowanie tkankowo-specyficznego metabolizmu Drosophila ujawnia wywołane dietą o wysokiej zawartości cukru zaburzenia metaboliczne w mięśniach na poziomie reakcji i szlaków
Dlaczego to badanie na muszce owocowej ma znaczenie dla zdrowia ludzi
Za duża ilość cukru w diecie może przeciążyć zdolność organizmu do gospodarowania paliwem, ostatecznie przyczyniając się do cukrzycy typu 2. To badanie wykorzystuje muszki owocowe, aby w zaskakująco dużych szczegółach ujawnić, jak różne tkanki radzą sobie z metabolizmem i jak dieta bogata w cukier zaburza funkcję mięśni. Ponieważ muszki dzielą z ludźmi wiele genów metabolicznych i układów narządów, te obserwacje pomagają wyjaśnić, co może pójść nie tak w naszych własnych mięśniach przy długotrwałym nadmiarze cukru.
Mapowanie metabolizmu tkanka po tkance
Nasze ciała, podobnie jak u muszek, składają się z tkanek pełniących bardzo różne role metaboliczne: mięśnie spalają paliwo, tkanka tłuszczowa je magazynuje, jelito przetwarza pokarm i tak dalej. Zamiast mierzyć każdą enzymatyczną reakcję bezpośrednio, badacze zbudowali duże „mapy” metabolizmu — zwane modelami metabolicznymi w skali genomu — dla 32 odrębnych tkanek muszki. Połączyli istniejącą, skuratowaną sieć reakcji chemicznych z danymi o ekspresji genów z pojedynczych komórek, które wskazują, które geny metaboliczne są w danej tkance aktywne. Pozwoliło to porównać, ile reakcji, metabolitów i genów jest aktywnych w każdym tkankowo-specyficznym modelu oraz zobaczyć, które szlaki są eksponowane w mięśniach, tkance tłuszczowej, jelicie i różnych typach komórek nerwowych.
Różne zadania paliwowe poszczególnych organów
Porównanie ujawniło wyraźne metaboliczne „osobowości” poszczególnych tkanek. Tkanka tłuszczowa i oenocyty — odpowiedniki u muszki ludzkiego tłuszczu i wątroby — zawierały najbogatszy zestaw reakcji, szczególnie tych spalających tłuszcze przez beta-oksydację. Mięsień natomiast nie miał największej sieci, ale wykazywał największy odsetek reakcji transportujących substancje do i z komórek, co sugeruje, że mięsień jest głównym węzłem wymiany paliw i bloków budulcowych z resztą organizmu. Naukowcy sprawdzili również, czy przewidywane szlaki odpowiadają rzeczywistym wzorcom metabolitów zmierzonych w różnych regionach ciała. Przy użyciu celowanej metabolomiki przeanalizowali setki małych cząsteczek z głów, tułowi, jelit i odwłoków muszek, a następnie sprawdzili, czy wzbogacone w danych szlaki pokrywają się z tymi przewidywanymi przez modele. W mięśniach i tkance tłuszczowej dopasowanie było silne, co zwiększa pewność, że modele tkankowo-specyficzne odzwierciedlają rzeczywistą biologię lepiej niż sama ekspresja genów.
Co dieta o wysokiej zawartości cukru robi z przepływem paliwa w mięśniach
Mając zweryfikowany model mięśnia, zespół zasymulował, co dzieje się, gdy muszki są karmione długotrwale dietą wysokocukrową, dobrze ustalonym modelem cukrzycy typu 2. Ograniczyli model, używając znanych cech mięśni cukrzycowych, takich jak zmniejszone pobieranie glukozy i spowolniona aktywność centralnego cyklu energetycznego w mitochondriach. Obliczeniowe analizy „strumieni” (flux) — kalkulacje, jak szybko mogą przebiegać reakcje — wykazały szerokie ograniczenia reakcji zależnych od pary redoks NAD/NADH, cząsteczek przenoszących elektrony i niezbędnych do produkcji energii. W szczególności spowolniły reakcje w centralnej ścieżce spalania cukru, glikolizie, w tym reakcje katalizowane przez enzym GAPDH. Model przewidział także około 25% spadek zdolności mięśnia do produkcji NADH ogółem, co sugeruje zaburzenie równowagi redoks. Bezpośrednie pomiary w mięśniach tułowiowych muszek potwierdziły, że stosunek NAD do NADH faktycznie zmalał w warunkach diety wysokocukrowej.
Śledzenie znakowanego cukru i utlenionych białek
Aby sprawdzić, czy przewidywane wąskie gardła rzeczywiście występują w żywych zwierzętach, badacze podali muszkom dietę wysokocukrową zawierającą jednorodnie znakowaną glukozę z węglem-13 i następnie śledzili, dokąd trafiał znakowany węgiel. Stwierdzili, że wczesne pośrednie produkty glikolizy, znajdujące się przed GAPDH, gromadziły się, podczas gdy produkty po tej reakcji i ich frakcje znakowania spadały, co sygnalizuje rzeczywiste spowolnienie na tym etapie i poniżej niego. Podobnie zmniejszyły się wkłady atomów węgla z glukozy do centralnego cyklu energetycznego. Równocześnie proteomika redoks — metoda wykrywająca oksydacyjne modyfikacje konkretnych aminokwasów w białkach — wykazała zwiększoną oksydację wielu enzymów glikolitycznych, w tym licznych miejsc na GAPDH. W całej glikolizie enzymy, które miały więcej modyfikacji oksydacyjnych, miały też tendencję do większych spadków przewidywanego strumienia, mimo że ich całkowite poziomy białkowe pozostały w większości niezmienione. Sugeruje to, że chemiczne uszkodzenie wynikające ze stresu oksydacyjnego, a nie utrata ilości enzymu, jest kluczowym czynnikiem upośledzającym przetwarzanie cukru w mięśniu.
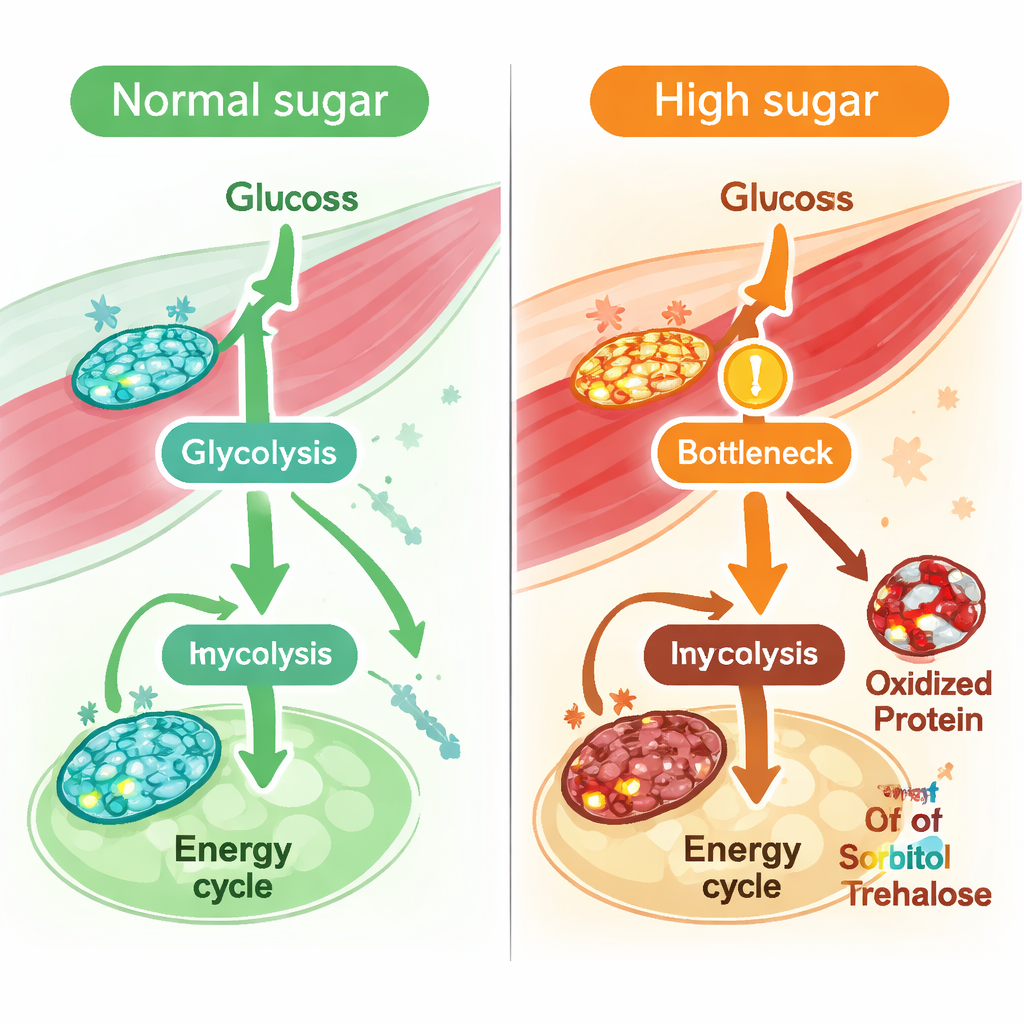
Ukryte problemy z metabolizowaniem fruktozy i sacharozy
Patrząc poza pojedyncze reakcje, zespół uśrednił strumienie w całych szlakach, aby zobaczyć, które z nich są najbardziej zaburzone przez wysoki cukier. Glikoliza, cykl energetyczny i fosforylacja oksydacyjna wykazywały spadki, ale jedną z najsilniej przewidywanych redukcji dotyczył metabolizm fruktozy. Profilowanie metabolitów mięśnia potwierdziło ten pomysł: wzrosły poziomy sorbitolu oraz trehalozy/sacharozy, a kluczowy enzym przekształcający trehalozę w glukozę, trehalaza, wykazał zarówno zmniejszoną przewidywaną aktywność, jak i zwiększoną oksydację w wrażliwym reszcie metioniny. Razem te ustalenia wskazują na szersze zaburzenie w sposobie, w jaki mięsień radzi sobie z cukrami pokarmowymi — zwłaszcza paliwami pochodzącymi od fruktozy i sacharozy — w warunkach przewlekłego przeciążenia cukrem.
Co to oznacza dla zrozumienia cukrzycy
Mówiąc prosto, praca ta pokazuje, że za dużo cukru nie tylko przeciąża krew; cicho przekształca też sposób, w jaki komórki mięśniowe kierują i spalają paliwo. Budując szczegółowe, tkankowo-specyficzne mapy metaboliczne dla muszki i weryfikując je za pomocą metabolomiki, śledzenia izotopów i proteomiki redoks, badacze wykazują, że wysoki cukier napędza stres redoks, utlenia kluczowe enzymy glikolityczne, takie jak GAPDH, spowalnia rozkład cukrów i zaburza szlaki związane z fruktozą. Te wnioski, uzyskane w wysoce przystępnym organizmie modelowym, oferują silne ramy do wskazywania reakcji i szlaków, które mogą być najważniejsze do ochrony lub przywrócenia w ludzkich mięśniach w celu zapobiegania lub leczenia cukrzycy typu 2.
Cytowanie: Moon, S.J., Hu, Y., Dzieciatkowska, M. et al. Modeling tissue-specific Drosophila metabolism identifies high sugar diet-induced metabolic dysregulation in muscle at reaction and pathway levels. Nat Commun 17, 1692 (2026). https://doi.org/10.1038/s41467-026-68395-3
Słowa kluczowe: metabolizm Drosophila, tkankowo-specyficzne modele metaboliczne, dieta o wysokiej zawartości cukru, glikoliza w mięśniach, regulacja redoks