Clear Sky Science · pl
Mechaniczne odmładzanie sennych komórek macierzystych i starzejących się kości poprzez przebudowę chromatyny
Dlaczego warto utrzymywać kości w młodości
W miarę starzenia się nasze kości stopniowo tracą wytrzymałość, stają się cieńsze i bardziej kruche. Zwiększa to ryzyko złamań, utraty samodzielności i przewlekłego bólu. Większość dostępnych terapii koncentruje się na lekach hamujących rozpad kości lub uzupełniających minerały, ale nie naprawiają bezpośrednio starzenia się komórek macierzystych odpowiedzialnych za tworzenie kości. W tym badaniu zbadano inne podejście: wykorzystanie precyzyjnie kontrolowanych sił fizycznych — zamiast leków — do „odmłodzenia” starzejących się komórek macierzystych tworzących kość oraz poprawy zdrowia kości i ogólnej sprawności starszych myszy.
Kiedy budowniczowie kości się starzeją
Głęboko w naszych kościach znajdują się mezenchymalne komórki macierzyste szpiku, główni budowniczowie, które mogą przekształcać się w komórki tworzące kość. Wraz z wiekiem te komórki dzielą się rzadziej, tworzą mniej tkanki kostnej i wykazują klasyczne cechy starzenia komórkowego, takie jak uszkodzenia DNA i sygnały zapalne. Badacze porównali komórki od młodszych i starszych dawców ludzkich i stwierdzili, że starzejące się komórki macierzyste różnią się nie tylko biochemicznie — były też mechanicznie słabsze. Wytwarzały mniejsze wewnętrzne siły naprężenia, miały luźniejszy wewnętrzny szkielet i gorzej przekazywały sygnały mechaniczne do jądra komórkowego. W tkance kostnej starych myszy zaobserwowano podobny spadek: sieć gąbczastej tkanki kostnej była przerzedzona, kluczowe białka sygnalizacji mechanicznej były zredukowane, a markery starzenia podwyższone.
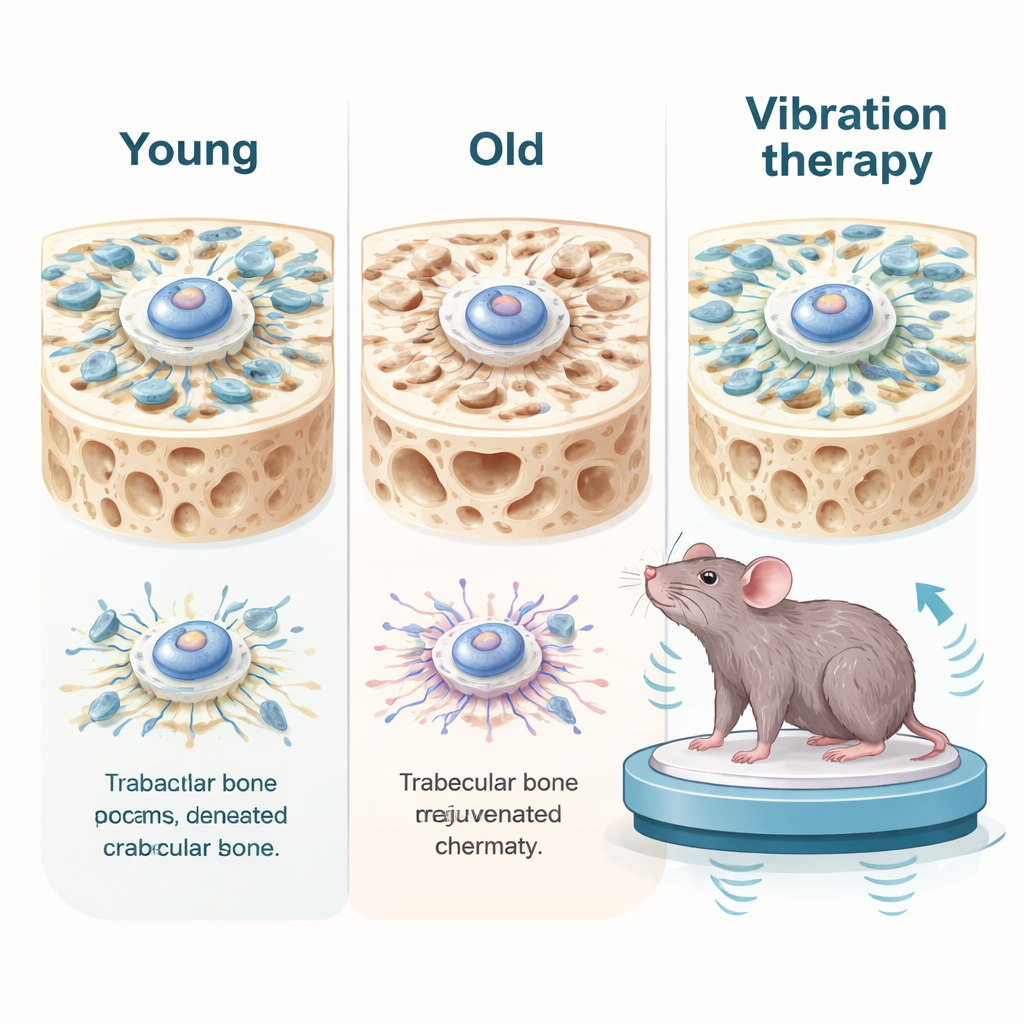
Delikatne przywracanie komórek do młodości
Zespół postawił następnie pytanie, czy przywrócenie sił mechanicznych może odwrócić te cechy starzenia. W hodowlach zastosowali łagodne rozciąganie do sennych komórek macierzystych lub użyli leku zwiększającego aktywność molekularnych motorów. Te zabiegi wzmocniły siły naprężenia w komórkach i poprawiły organizację wewnętrznego szkieletu. Co zaskakujące, starzejące się komórki zaczęły wyglądać i zachowywać się młodziej: spadły markery senescencji, zmniejszyły się uszkodzenia DNA, a komórki namnażały się szybciej. Odwrotny efekt również wystąpił — gdy zmiękczono środowisko pod młodymi komórkami lub chemicznie osłabiono ich maszynerię kontrakcyjną, komórki weszły w stan podobny do starzenia, spowalniając i uruchamiając markery starzenia nawet w trójwymiarowym żelu naśladującym kość.
Jak siła komunikuje się z genami
Aby zrozumieć, jak siły fizyczne mogły tak głęboko zmieniać zachowanie komórek, badacze zwrócili uwagę na chromatynę — upakowaną formę DNA w jądrze. W starych komórkach macierzystych chromatyna była bardziej skondensowana i mniej dostępna, co utrudniało uruchamianie korzystnych genów. Przywrócenie sił mechanicznych powodowało lokalne rozluźnienie chromatyny i zwiększenie chemicznych znaków związanych z otwartą, aktywną formą DNA. Przy użyciu badania dostępności chromatyny obejmującego całe genom, zespół odkrył, że delikatna stymulacja mechaniczna otwierała regiony przy genach zaangażowanych w kontrolę starzenia. Jeden gen, nazwany FOXO1, wyróżniał się szczególną wrażliwością na siłę. Po zwiększeniu naprężenia obszar DNA FOXO1 stawał się bardziej otwarty, jego aktywność rosła, a komórki stawały się mniej senescentne. Zablokowanie FOXO1 niwelowało korzyści stymulacji mechanicznej, ujawniając go jako kluczowy przełącznik łączący obciążenie fizyczne z programami genetycznymi odporności i naprawy.
Znajdowanie optymalnej dawki terapii mechanicznej
Następnie badacze przetestowali stymulację mechaniczną na żywych myszach. Starsze zwierzęta umieszczono na platformie o niskiej intensywności drgań na krótkie codzienne sesje przez miesiąc, podczas gdy inne miały odciążone tylne kończyny poprzez zawieszenie za ogon, co naśladowało skrajną brak aktywności. U starych myszy delikatne drgania zwiększyły sygnalizację mechaniczną w kości, zmniejszyły markery starzenia i zapalenia oraz częściowo odbudowały sieć gąbczastej tkanki kostnej. Poprawiły też siłę chwytu, wytrzymałość podczas ćwiczeń, zadania związane z pamięcią oraz obniżyły stan zapalny we krwi, wątrobie i nerkach. Jednak gdy drgania stosowano ciągle bez dni przerwy, korzyści znikały, a nawet odwracały się: struktura kości pogorszyła się, uszkodzenia DNA wzrosły, a stan zapalny się nasilił. W badaniach komórkowych zbyt silne lub zbyt częste rozciąganie powodowało pęknięcia DNA i wpychało komórki z powrotem w senescencję, pokazując, że siła mechaniczna może leczyć lub szkodzić w zależności od dawki.
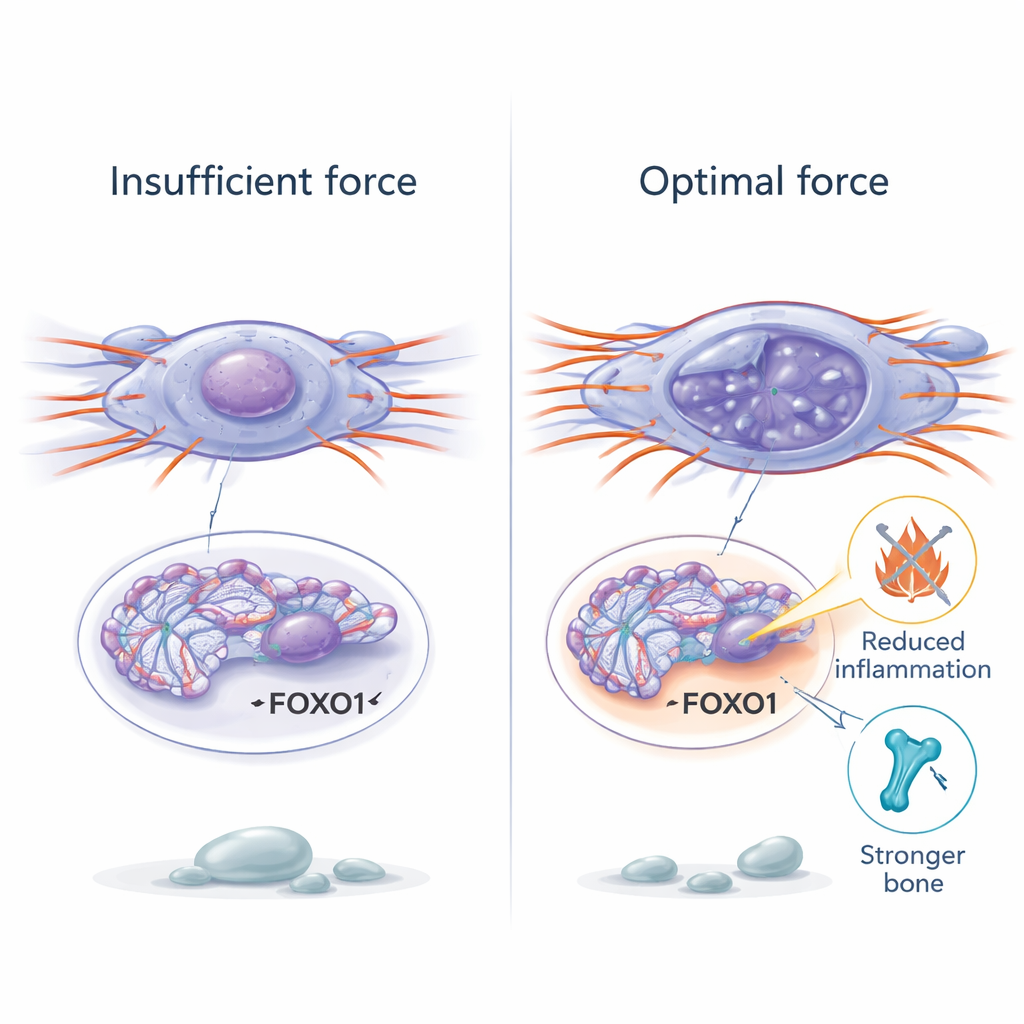
Od imitacji ćwiczeń do przyszłych terapii
Dla laika główny przekaz jest taki, że nasze komórki reagują nie tylko na hormony i związki chemiczne — one równie uważnie „słuchają” sił fizycznych. W tej pracy autorzy pokazują, że umiarkowana, dobrze dobrana stymulacja mechaniczna może przebudzić starzejące się komórki macierzyste kości, uruchomić ochronne programy genowe takie jak FOXO1, odbudować osłabioną kość i złagodzić przewlekłe zapalenie u starszych myszy. Jednocześnie zbyt mało lub zbyt dużo siły przyspiesza zużycie komórkowe. Wyniki te sugerują, że starannie zaprojektowane terapie mechaniczne — być może określone programy ćwiczeń lub bezpieczne urządzenia wibracyjne — mogłyby kiedyś uzupełniać leki w utrzymaniu zdrowszych kości i być może innych tkanek przez dłuższy czas.
Cytowanie: Liu, X., Ye, Y., Li, Z. et al. Mechanical rejuvenation of senescent stem cells and aged bone via chromatin remodeling. Nat Commun 17, 1684 (2026). https://doi.org/10.1038/s41467-026-68387-3
Słowa kluczowe: starzenie się kości, stymulacja mechaniczna, odmładzanie komórek macierzystych, przebudowa chromatyny, FOXO1