Clear Sky Science · pl
Precyzyjne wycięcie powiększonych powtórzeń GGC w NOTCH2NLC za pomocą CRISPR/Cas9 w leczeniu neuronalnej choroby z miejscowymi inkluzjami jądrowymi
Edytowanie DNA w walce z tajemniczą chorobą mózgu
Neuronowa choroba z inkluzjami jądrowymi (NIID) to rzadka, lecz wyniszczająca choroba mózgu, która może powodować otępienie, zaburzenia ruchowe, a nawet przedwczesną śmierć. Obecnie nie ma lekarstwa. Badanie to sprawdza, czy potężne narzędzie do edycji genów, CRISPR, może wyciąć maleńki, lecz toksyczny odcinek DNA, który napędza NIID, dając wgląd w to, jak przyszłe terapie mogłyby przepisać nasze geny, by zwalczać choroby mózgu. 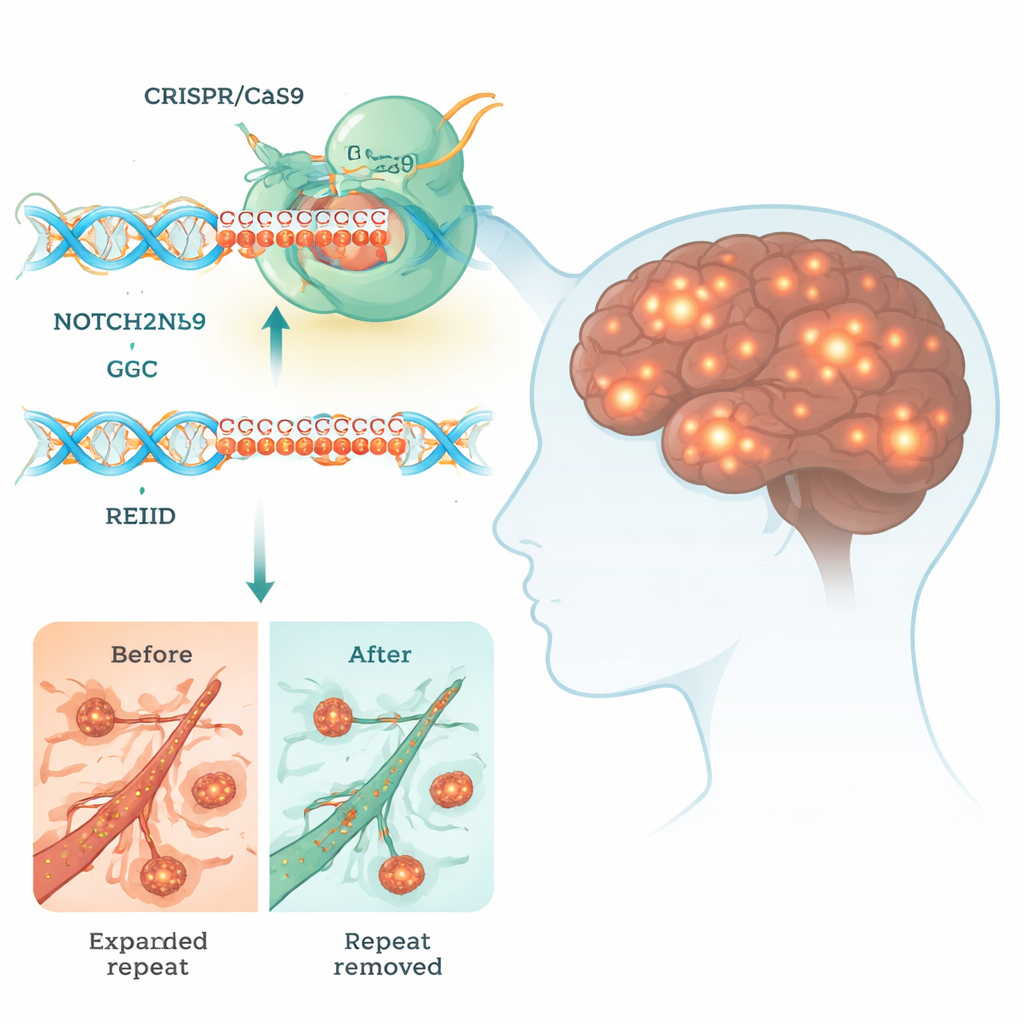
Ukryty genetyczny sprawca
Wiele dziedzicznych chorób mózgu jest spowodowanych przez krótkie sekwencje DNA, które urosły znacznie ponad normalną długość. W NIID problemem jest nadmiernie wydłużony ciąg trzykodowych jednostek „GGC” w genie o nazwie NOTCH2NLC. Chociaż ten odcinek znajduje się w regionie, który nie koduje klasycznego białka, komórkowe maszyny mogą go i tak odczytywać, produkując nieprawidłowe łańcuchy poliglicyny (polyG). Te lepkie łańcuchy zlepiają się w grudki wewnątrz jądra komórek nerwowych i innych tkanek, zaburzając istotne procesy, takie jak produkcja energii, przetwarzanie RNA oraz transport cząsteczek między jądrem a cytoplazmą.
Wyzwanie precyzyjnej chirurgii genowej
Opracowanie terapii edytującej geny dla NIID jest wyjątkowo trudne, ponieważ NOTCH2NLC ma kilka niemal identycznych genów siostrzanych, które są ważne dla rozwoju ludzkiego mózgu. Jeśli CRISPR utnie niewłaściwy gen, może wyrządzić więcej szkody niż pożytku. Naukowcy starannie przeanalizowali DNA wokół powtórzenia GGC i znaleźli drobne różnice sekwencji, które odróżniają NOTCH2NLC od jego krewnych. Następnie zaprojektowali pary przewodników RNA CRISPR, które kierują „molekularnymi nożyczkami” Cas9, by ciąć tuż przed i tuż za powiększonym powtórzeniem. Ta strategia dwu-cięcia pozwala systemowi naprawczemu komórki usunąć toksyczny fragment, pozostawiając resztę rodziny genów nietkniętą.
Od komórek w naczyniu do neuronów pochodzących od pacjenta
Zespół najpierw przetestował swój projekt CRISPR w standardowych ludzkich komórkach oraz w komórkach inżynierowanych tak, by zawierały duże powtórzenie NOTCH2NLC. W tych modelach edytor skutecznie wycinał powtórzenie, a poziomy grudek polyG zmniejszyły się o około połowę lub więcej. Następnie przeszli do indukowanych pluripotencjalnych komórek macierzystych (iPSC) pochodzących od pacjenta z NIID i przekształcili je w progenitorowe komórki nerwowe, wczesny etap komórek mózgowych. Za pomocą CRISPR albo usuwano rozszerzone powtórzenie, albo zastępowano je wersją o prawidłowej długości. Szczegółowe sekwencjonowanie DNA i całego genomu wykazało, że edycja była wysoce dokładna, z niewielkimi dowodami na niepożądane cięcia, a zmodyfikowane komórki nadal dzieliły się i dojrzewały prawidłowo. 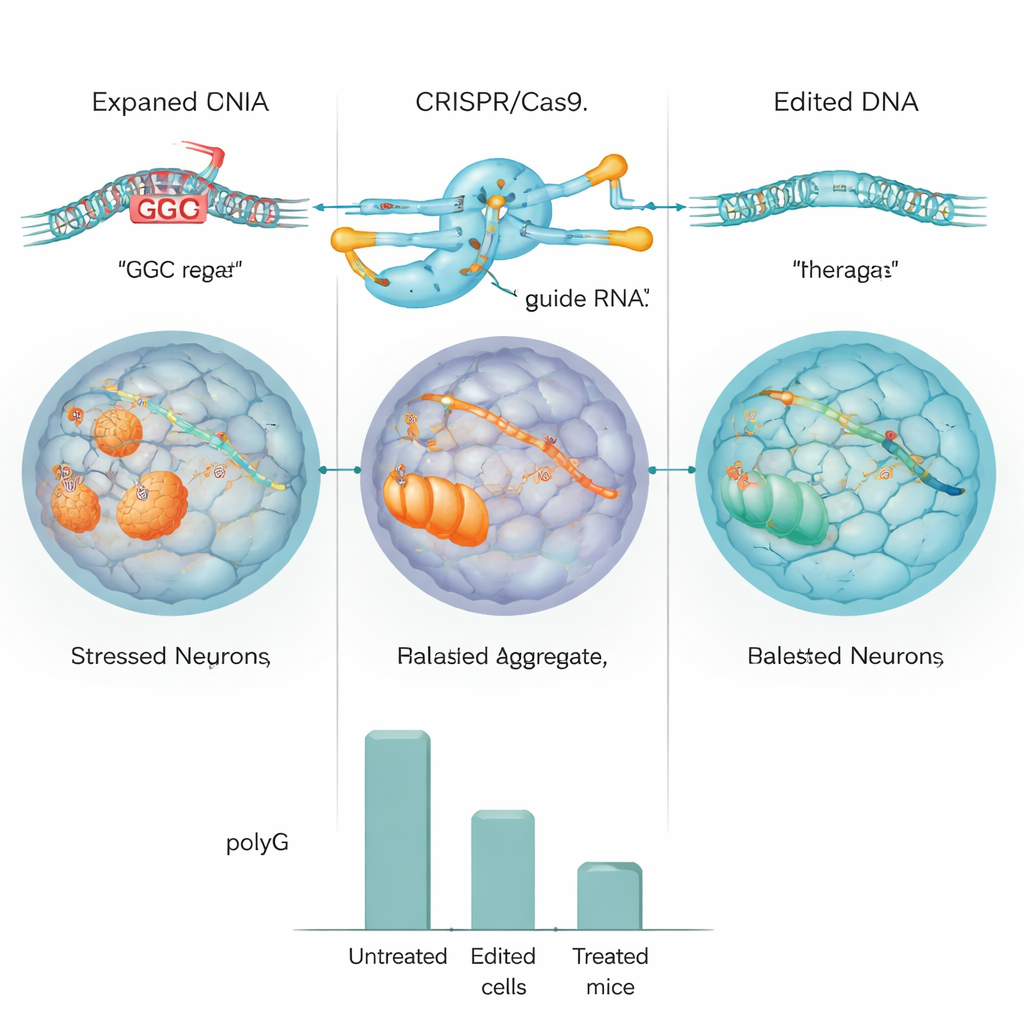
Ratowanie mózgu i organizmu w modelu myszy
Aby sprawdzić, czy podejście to rzeczywiście może poprawić przebieg choroby, badacze sięgnęli po myszy zmodyfikowane tak, by nosiły ludzki wariant powtórzenia NOTCH2NLC i rozwijały cechy przypominające NIID, w tym inkluzje jądrowe, zaburzenia ruchowe i skróconą długość życia. Spakowali system CRISPR do zmodyfikowanego wirusa, który po prostym wstrzyknięciu do krwiobiegu noworodków może rozprzestrzenić się po całym mózgu. U leczonych zwierząt rozszerzone powtórzenie zostało skutecznie usunięte w tkance mózgowej. W rezultacie poziomy toksycznego polyG gwałtownie spadły, poprawiły się markery zdrowia komórek nerwowych, a nieprawidłowa aktywacja komórek wspierających mózg zmniejszyła się. Testy behawioralne wykazały, że leczone myszy poruszały się więcej, miały lepszą równowagę i żyły dłużej niż ich nieleczone rodzeństwo. Podobne korzyści zaobserwowano w sercu, które w tym modelu także gromadzi polyG.
Co to może znaczyć dla przyszłych terapii
Dla laika główny wniosek jest taki, że NIID wydaje się być napędzana w dużej mierze przez jedno konkretne nadmiernie wydłużone powtórzenie DNA, a jego precyzyjne usunięcie może odwrócić wiele objawów choroby w komórkach i u myszy. Praca ta nie przekłada się jeszcze na gotową do użycia terapię dla ludzi: naukowcy nadal muszą dopracować długoterminowe bezpieczeństwo, ulepszyć metody dostarczania i przetestować podejście w większych, bardziej podobnych do ludzi modelach zwierzęcych. Jednak badanie stanowi mocne dowody koncepcji, że starannie ukierunkowana edycja genów może bezpiecznie uciszyć toksyczne powtórzenie, oszczędzając blisko spokrewnione geny. Tę strategię można pewnego dnia zaadaptować nie tylko dla NIID, lecz także dla innych chorób mózgu i mięśni wywołanych podobnymi ekspansjami powtórzeń.
Cytowanie: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
Słowa kluczowe: Edytowanie genów CRISPR, neuronalna choroba z inkluzjami jądrowymi, choroby związane z ekspansją powtórzeń, NOTCH2NLC, neurodegeneracja