Clear Sky Science · pl
Igłowe mikronakłucia z nanomotorami napędzanymi światłem bliskiej podczerwieni do aktywnej terapii bakteryjnego trądziku
Dlaczego to badanie nad trądzikiem ma znaczenie
Trądzik bywa lekceważony jako problem estetyczny, ale dla nastolatków i dorosłych może być bolesny, prowadzić do blizn i obciążać psychicznie. Standardowe terapie, zwłaszcza antybiotyki, mogą wywoływać skutki uboczne i sprzyjać powstawaniu opornych szczepów. W pracy opisano plaster igłowy zasilany nieszkodliwym światłem bliskiej podczerwieni, który dostarcza maleńkie „nanomotory” bezpośrednio do zmian trądzikowych. Te inteligentne cząstki wytwarzają własny tlen, poruszają się aktywnie przez śluzowe warstwy biofilmu bakteryjnego i nagrzewają się na tyle, by zabić zarazki i złagodzić stan zapalny — dając przedsmak przyszłej opieki nad trądzikiem bardziej celowanej i mniej zależnej od antybiotyków.
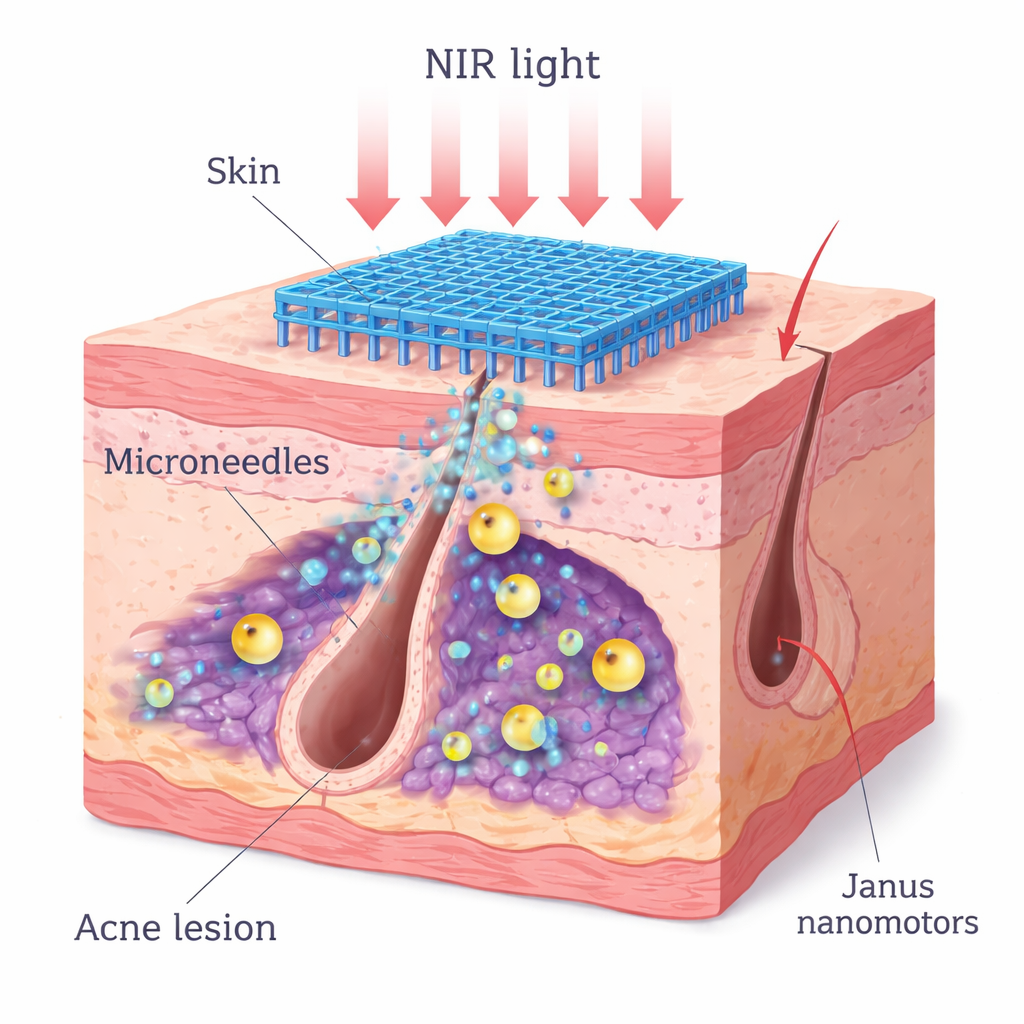
Jak trądzik przekształca się w zapalny guzek
Większość trądziku zaczyna się, gdy pory i mieszki włosowe zostają zablokowane przez sebum i martwe komórki naskórka. W tych zatkanych mieszka rozwija się bakteria Cutibacterium acnes (dawniej Propionibacterium acnes) w warunkach niskiej zawartości tlenu. Mikroby tworzą ochronne biofilmy — lepkie społeczności otoczone gęstą matrycą — które chronią je przed lekami. Karmiąc się tłuszczami skórnymi, uwalniają kwasy tłuszczowe, które dodatkowo obniżają poziom tlenu i podrażniają pobliskie komórki. Skóra reaguje produkcją sygnałów zapalnych, takich jak TNF‑α i interleukiny, a lokalne komórki odpornościowe, które zwykle utrzymują równowagę mikrobiologiczną, ulegają wyczerpaniu. W efekcie pojawiają się zaczerwienienie, obrzęk i czasem blizny charakterystyczne dla opornego trądziku.
Dlaczego zwykłe kremy i tabletki często zawodzą
Miejscowe kremy i żele mają problemy z przenikaniem przez zewnętrzną barierę skóry, a doustne antybiotyki oblewają cały organizm lekiem, by dotrzeć do niewielkiego obszaru, co zwiększa ryzyko działań niepożądanych i oporności. W dojrzałej zmianie trądzikowej gruby biofilm wokół C. acnes dodatkowo blokuje przenikanie. Nawet terapia fototermalna — wykorzystująca cząstki absorbujące światło do wytwarzania ciepła zabijającego bakterie — ma trudności, ponieważ cząstki nie mogą poruszać się głęboko w biofilmie, a nisko‑tlenowe, kwaśne środowisko sprzyja przewlekłemu zapaleniu zamiast go leczyć.
Plaster mikronakłuwający aktywowany światłem z maleńkimi silnikami
Naukowcy zaprojektowali rozpuszczalny plaster mikronakłuwający, który bezboleśnie wnika tuż pod powierzchnię skóry i uwalnia zaprojektowane nanomotory. Każdy nanomotor ma rdzeń z nadtlenku cynku (zinc peroxide), który powoli rozkłada się w warunkach kwaśnych, uwalniając nadtlenek wodoru, przekształcany następnie w tlen przez powłokę z dwutlenku manganu. Jedna strona cząstki jest pokryta warstwą absorbującą światło z polidopaminy i dwutlenku manganu, tworząc strukturę „Janusową” (dwukierunkową). Gdy na skórę pada laser o długości fali 808 nm w bliskiej podczerwieni, asymetryczne pokrycie nagrzewa jedną stronę bardziej niż drugą, tworząc gradient temperatury, który wprawia cząstkę w ruch. Ta samo‑napędzająca się mobilność pomaga nanomotorom rozprzestrzeniać się przez gęste biofilmy i przestrzenie mieszka włosowego, jednocześnie dostarczając ciepła, które osłabia obronę bakterii.
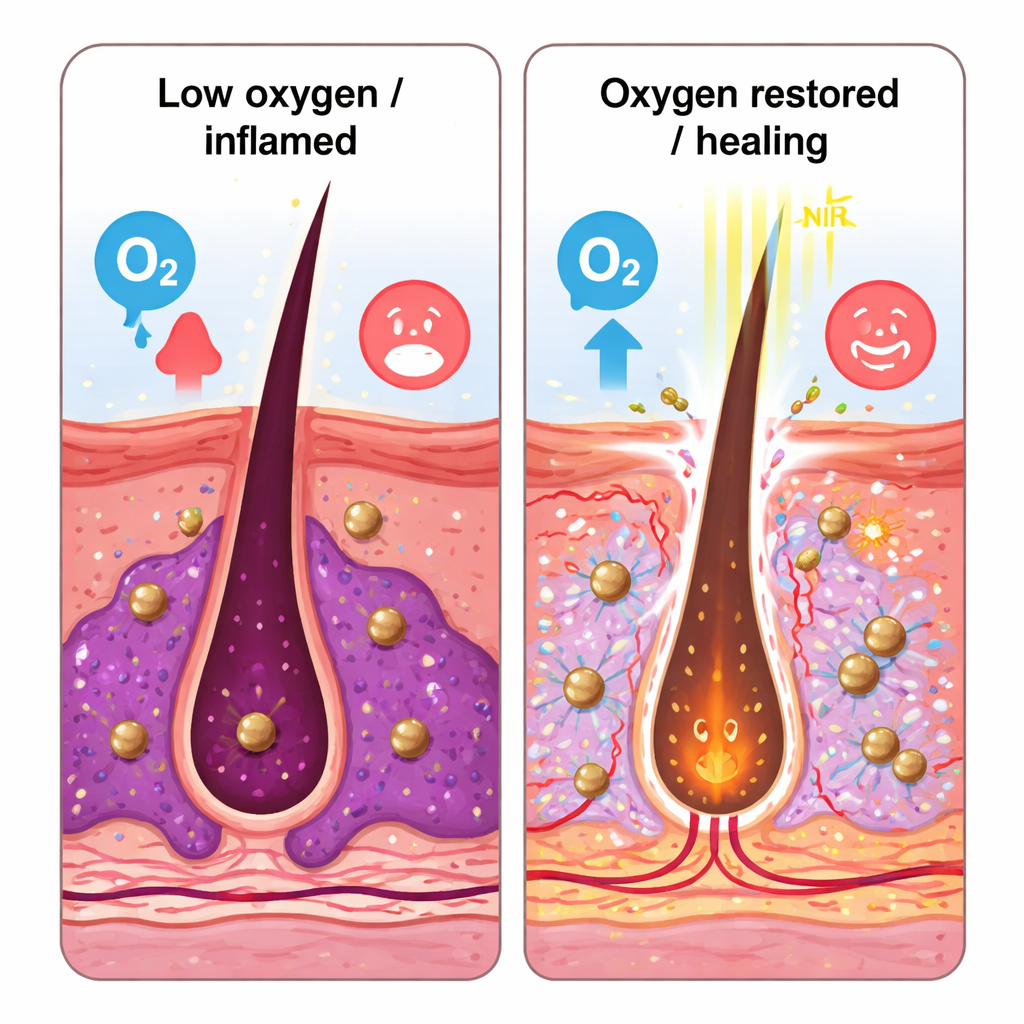
Od ławy laboratoryjnej do skóry myszy
W testach laboratoryjnych nanomotory efektywnie nagrzewały się pod światłem bliskiej podczerwieni, pozostawały stabilne w kolejnych cyklach i uwalniały więcej nadtlenku wodoru oraz tlenu w warunkach kwaśnych, przypominających biofilm. Plastry z mikronakłuć wykonane z przyjaznego skórze kwasu hialuronowego były wystarczająco wytrzymałe, by przebić skórę, ale rozpuszczały się w około pół godziny, uwalniając nanomotory do skóry właściwej. Pod wiązką światła cząstki wykazywały wyraźnie zwiększony ruch i penetrowały głębiej zarówno sztuczne biofilmy, jak i skórę świni. W hodowlach bakterii C. acnes oraz opornego Staphylococcus aureus połączenie mikronakłuć, nanomotorów i pięciominutowej ekspozycji na bliską podczerwień zredukowało masę biofilmu i przeżywalność bakterii o ponad 90 procent, powodując widoczne uszkodzenia błon mikroorganizmów i ich DNA.
Łagodzenie stanu zapalnego i przywracanie równowagi
W modelu myszy z trądzikiem, wywołanym przez wstrzyknięcie C. acnes w skórę, plaster aktywowany światłem zmniejszał rozmiar zmian i liczbę bakterii równie skutecznie jak erytromycyna, ale bez widocznego uszkodzenia tkanek. Preparaty skórne od leczonych myszy wykazywały mniej komórek zapalnych, niższe poziomy molekuł zapalnych (IL‑6, TNF‑α) oraz zmniejszoną aktywność HIF‑1α — markera niskiego tlenu. Równocześnie wzrosły markery angiogenezy i naprawy ran, a kluczowe komórki odpornościowe zwane ILC3, które były zahamowane przez infekcję, odbudowały się i produkowały więcej czynnika gojenia IL‑22. Autorzy sugerują, że dostarczając tlen i mechanicznie rozbijając biofilmy, nanomotory pomagają normalizować zarówno lokalny mikrobiom, jak i środowisko immunologiczne skóry.
Co to może oznaczać dla przyszłej opieki nad trądzikiem
Dla laika wniosek jest taki, że system plaster‑nanomotor działa jak inteligentne, zlokalizowane leczenie: delikatnie tworzy drogę przez skórę, kieruje maleńkie silniki w głąb zmiany trądzikowej i pod krótkim impulsem niewidzialnego światła dostarcza ciepło i tlen dokładnie tam, gdzie są potrzebne. U myszy podejście to usuwało infekcję, łagodziło stan zapalny i wspierało gojenie tkanek, dorównując antybiotykom bez stosowania leków ogólnoustrojowo. Choć potrzebne są badania kliniczne u ludzi i długoterminowe oceny bezpieczeństwa, praca wskazuje na nową klasę terapii trądziku łączących penetrację mechaniczną, aktywację na żądanie i samodzielną produkcję tlenu, by precyzyjniej zwalczać infekcje oparte na biofilmie i z mniejszą liczbą skutków ubocznych.
Cytowanie: Hu, Z., Gan, Y., Song, Y. et al. Near-infrared light-driven nanomotors-based microneedles for the active therapy of bacterial infected acne. Nat Commun 17, 1675 (2026). https://doi.org/10.1038/s41467-026-68376-6
Słowa kluczowe: leczenie trądziku, plaster mikronakłuwający, nanomotory, terapia bliską podczerwienią, bakteriome biofilmowe