Clear Sky Science · pl
Struktura Cryo-EM ludzkiego kompleksu ligazy ubikwitynowej COP1-DET1
Jak komórki decydują, które białka zniszczyć
W każdej komórce tysiące białek muszą być nieustannie syntetyzowane, przebudowywane lub niszczone w odpowiednim czasie. Artykuł opisuje jedno z kluczowych „urządzeń kontroli jakości” komórki — molekularny rozdrabniacz decydujący, kiedy usunąć silne regulatory genów związane z rakiem i rozwojem. Dzięki ujawnieniu jego trójwymiarowej struktury w niemal atomowej rozdzielczości autorzy pokazują, jak to urządzenie może przełączać się między nieaktywnym, „składowym” stanem a aktywną formą przetwarzającą substraty — wgląd, który w przyszłości może pomóc w projektowaniu leków regulujących jego aktywność.
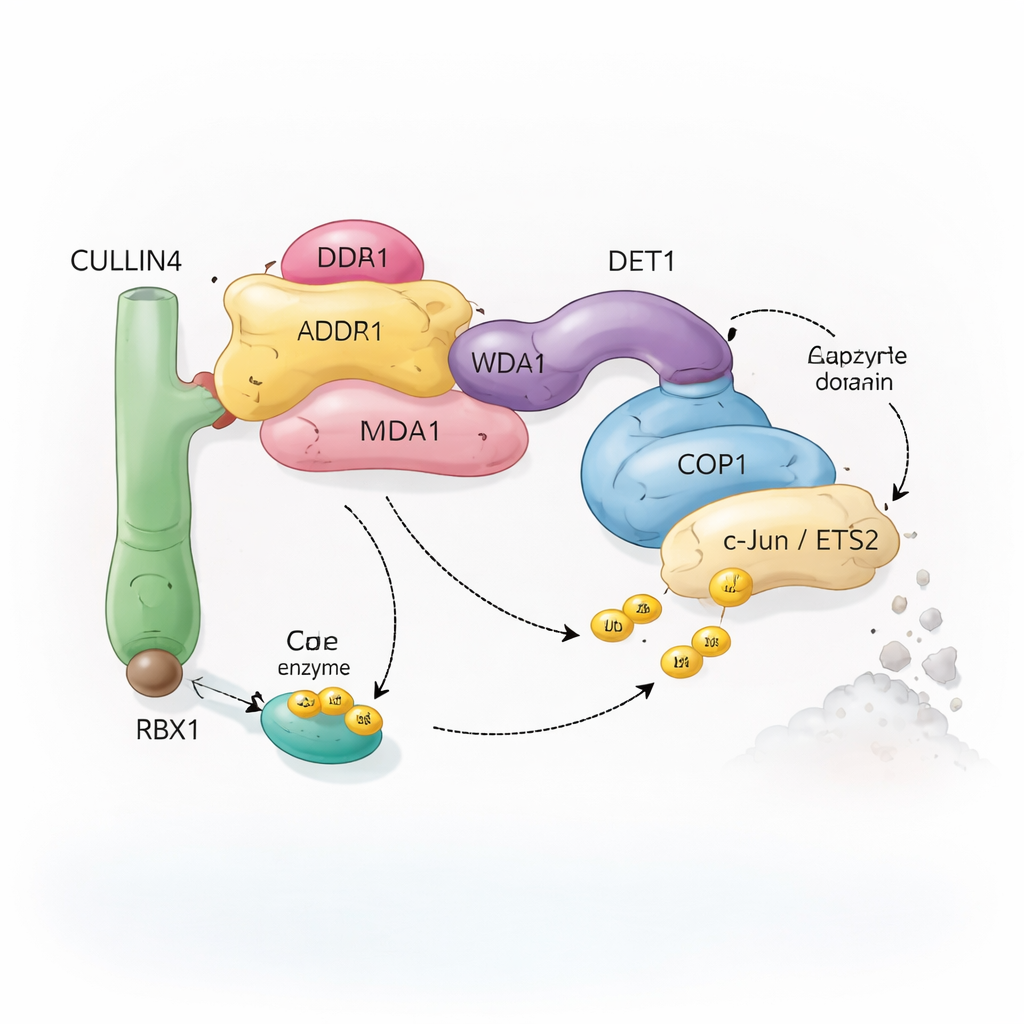
Wieloelementowa „ekipa recyklingowa” molekularna
Komórki polegają na układzie ubikwitynacji, aby oznaczać białka do recyklingu. Małe cząsteczki ubikwityny działają jak zdejmowalne flagi, które informują komórkę, czy białko ma zostać zmienione, przemieścić się czy zniszczone. Specjalne kompleksy enzymatyczne, zwane ligazami ubikwityny, przyłączają te flagi do wybranych celów. Badany tutaj kompleks skupia się wokół COP1, białka występującego od roślin po ludzi, które pomaga znakować ważne czynniki transkrypcyjne — białka kontrolujące, które geny są włączane lub wyłączane. COP1 nie działa sam: może włączać się do większego zespołu zbudowanego wokół białka rusztowaniowego zwanego CULLIN4 oraz kilku adaptorów nazwanych DDB1, DDA1 i DET1. Razem te elementy tworzą elastyczną „ekipę recyklingową”, która rozpoznaje konkretne czynniki transkrypcyjne, takie jak c‑Jun i ETS2, z których wiele bierze udział w wzroście komórek i nowotworzeniu.
Uchwycenie kompleksu w 3D
Aby zrozumieć, jak działa ta ekipa, badacze użyli krio‑mikroskopii elektronowej pojedynczych cząstek, techniki obrazowania błyskowo zamrożonych białek i odtwarzania ich kształtów w wysokiej rozdzielczości. Odtworzyli ludzki system COP1–DET1 w hodowlach komórkowych, oczyszczali kompleksy i wizualizowali kilka odrębnych stanów strukturalnych. Najpierw rozwiązali strukturę modułu DDB1–DDA1–DET1, który działa jako centralne centrum. DET1 przyjmuje nietypowy, częściowo elastyczny kształt zamiast sztywnego dysku, z wystającym „szponem”, który może chwytać enzymy partnerów. Następnie, dodając COP1 i klasę pomocniczych enzymów znanych jako E2, uchwycili większe zespoły pokazujące, jak wszystkie części do siebie pasują, ujawniając zarówno zwarte układy warstwowe, jak i bardziej otwarte układy dimerowe (z dwoma COP1).
Nieaktywny stos i aktywny dimer
Jednym z najbardziej uderzających odkryć jest ułożona warstwowo, przypominająca filament struktura złożona z powtarzających się warstw kompleksu. W każdej warstwie osiem cząsteczek COP1 splata się przez swoje segmenty helikalne, tworząc pierścień w kształcie rombu. Ich regiony rozpoznające substraty, zwane domenami WD40, zwrócone są w jednym kierunku i częściowo osłonięte przez sąsiednie warstwy. To ciasne upakowanie prawdopodobnie reprezentuje stan „wyłączony”, w którym dostęp dla białek‑celów jest ograniczony. W przeciwieństwie do tego, gdy zespół przeanalizował kompleksy ko‑ekspresowane z substratami COP1, takimi jak c‑Jun czy ETS2, zaobserwowano inną, dimerową formę: dwie cząsteczki COP1 ułożone obok siebie, z domenami WD40 zwróconymi na zewnątrz i dostępnymi do wiązania krótkich motywów „VP” występujących w wielu czynnikach transkrypcyjnych. Testy biochemiczne potwierdziły, że tylko ten dimerowy stan efektywnie wspiera budowę długich łańcuchów ubikwityny na c‑Jun.
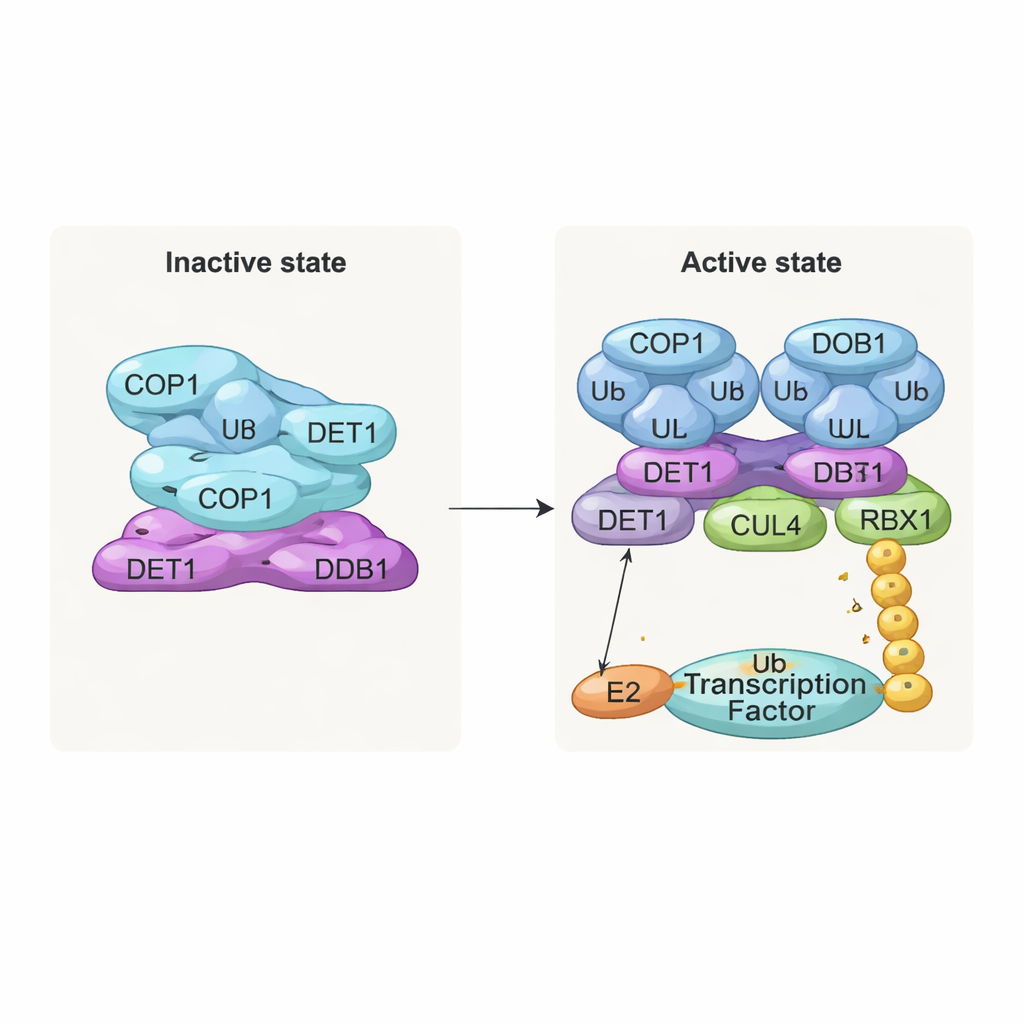
DET1 jako elastyczny most i reżyser ruchu
DET1 wyłania się jako kluczowy organizator łączący wszystkie części maszyny. Jego region N‑terminalny wsuwa się w DDB1, kotwicząc kompleks do rusztowania CULLIN4, podczas gdy jego „szpon” owija się wokół rodziny enzymów E2 zwanych Ube2e. Szczegółowe eksperymenty mutacyjne pokazują, że to DET1, a nie COP1, bezpośrednio chwyta te E2, ustawiając je blisko katalitycznego regionu RING COP1. W takim układzie Ube2e wydaje się pomagać umieścić pierwsze znaczniki ubikwityny na substracie. Drugi enzym E2, Ube2d3, jest następnie rekrutowany przez ramię CULLIN4–RBX1, aby wydłużyć te znaczniki w dłuższe łańcuchy sygnalizujące pełną degradację. Innymi słowy, DET1 działa jak elastyczny most prezentujący jednego E2 COP1, podczas gdy większe rusztowanie przyprowadza drugiego E2, by dokończył pracę.
Dlaczego to ma znaczenie dla zdrowia i chorób
Mapując te stany strukturalne i ich aktywności, badanie wyjaśnia, jak ten sam zestaw białek może przełączać się między bezczynną, warstwową formą a aktywnym dimerem, który kieruje czynniki transkrypcyjne do zniszczenia. To przełączenie jest szczególnie ważne dla czynników takich jak c‑Jun, które napędzają podziały komórek i są ściśle powiązane z rakiem przy ich nieprawidłowej regulacji. Zrozumienie, jak COP1 i DET1 współpracują — jak szpon DET1 wybiera konkretne enzymy E2, jak powierzchnia WD40 COP1 rozpoznaje substraty zawierające motyw VP i jak formuje się aktywny dimer — dostarcza planu działania na przyszłość. W dłuższej perspektywie leki stabilizujące nieaktywny stos lub faworyzujące aktywny dimer mogłyby dać badaczom nowe sposoby modulowania ścieżek kontroli genów w raku i innych chorobach, w których degradacja białek jest zaburzona.
Cytowanie: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
Słowa kluczowe: ligaza ubikwitynowa, COP1, degradacja białek, struktura cryo-EM, c-Jun