Clear Sky Science · pl
INCENP i CDCA8 przewidują odpowiedź na chemioterapię neoadiuwantową i wynik w raku płaskonabłonkowym przełyku
Dlaczego to badanie ma znaczenie dla pacjentów z rakiem
Wiele osób z nowotworami przełyku, piersi czy płuc otrzymuje silną chemioterapię przed zabiegiem chirurgicznym, aby zmniejszyć guzy. Jednak tylko około połowa tych pacjentów faktycznie odnosi korzyść; u pozostałych leki wywołują skutki uboczne bez zatrzymywania choroby. W badaniu postawiono proste, lecz kluczowe pytanie: czy można wcześniej przewidzieć, kto zareaguje na chemioterapię, i czy da się poprawić skuteczność leczenia u tych, którzy obecnie na nie nie reagują?
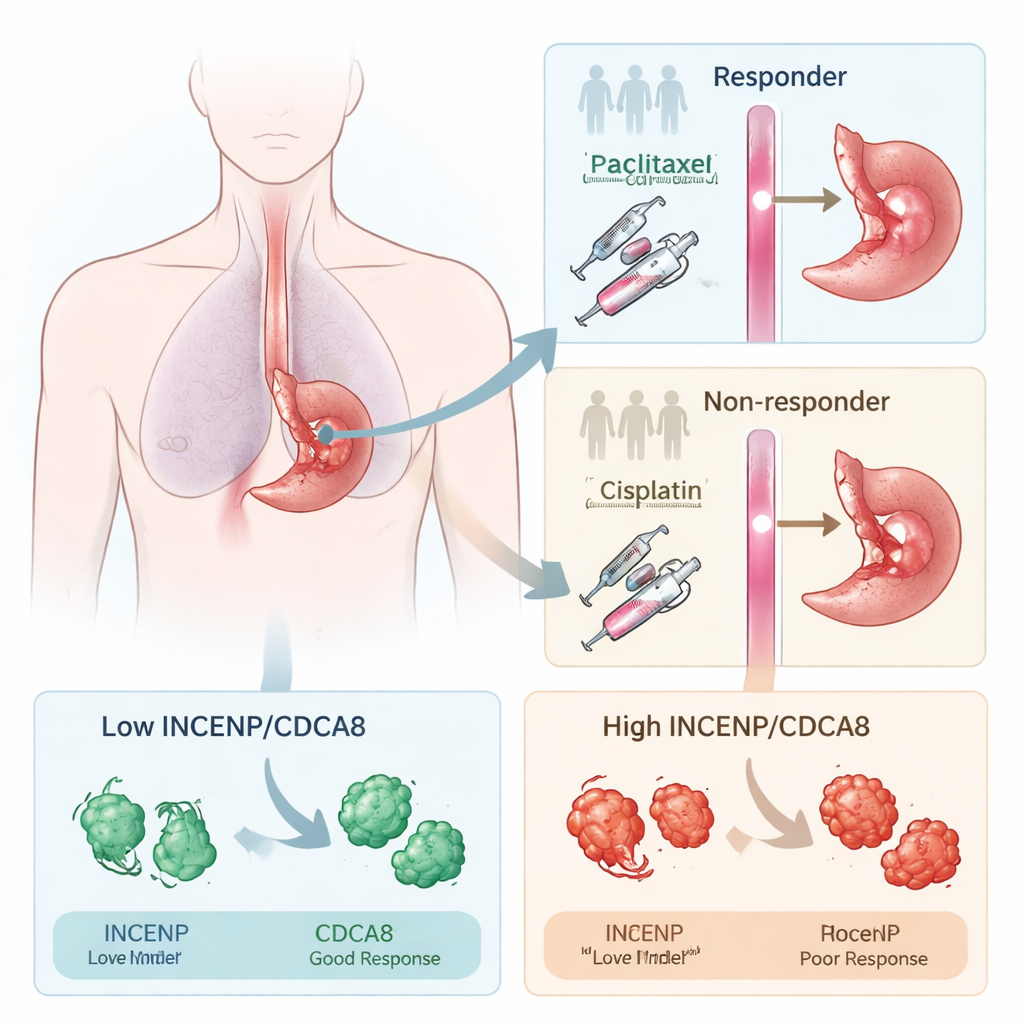
Wykrywanie osób reagujących na leczenie
Naukowcy skupili się na standardowym schemacie przedoperacyjnym łączącym paklitaksel i cisplatynę, szeroko stosowanym w różnych nowotworach. Pracując najpierw z pacjentami z rakiem płaskonabłonkowym przełyku, porównali próbki guzów od osób, których nowotwory znacznie się zmniejszyły po terapii (odpowiadający) z próbkami od tych, u których guzy prawie nie reagowały (nieodpowiadający). Przeglądając, które geny zostały włączone lub wyciszone, odkryli, że wiele różnic dotyczy procesów podziału komórkowego — procesu, który chemioterapia ma zaburzać. Dwa białka pomagające kontrolować rozdział chromosomów podczas podziału komórki, INCENP i CDCA8, wielokrotnie wyróżniały się jako znacznie bardziej obecne w guzach opornych na leczenie.
Dwa białka sygnalizujące prawdopodobną oporność
Aby sprawdzić, czy INCENP i CDCA8 są jedynie obserwatorami, czy faktycznymi sprawcami oporności, zespół zmieniał ich poziomy w hodowanych w laboratorium komórkach raka przełyku. Gdy obniżono którekolwiek z tych białek, komórki nowotworowe stały się znacznie bardziej wrażliwe na paklitaksel i cisplatynę, tworzyły mniej kolonii i wymagały dużo niższych dawek leku do ich zabicia. Gdy wymuszono nadprodukcję INCENP lub CDCA8, zaobserwowano odwrotny efekt: leki stały się mniej skuteczne. U myszy z wszczepionymi ludzkimi guzami przełyku zahamowanie tych białek sprawiło, że chemioterapia silniej zmniejszała guzy. Pacjenci, których guzy zawierały wysokie poziomy INCENP i CDCA8 przed leczeniem, mieli też większe prawdopodobieństwo progresji choroby i krótsze przeżycie, co potwierdza wartość tych białek jako sygnałów ostrzegawczych.
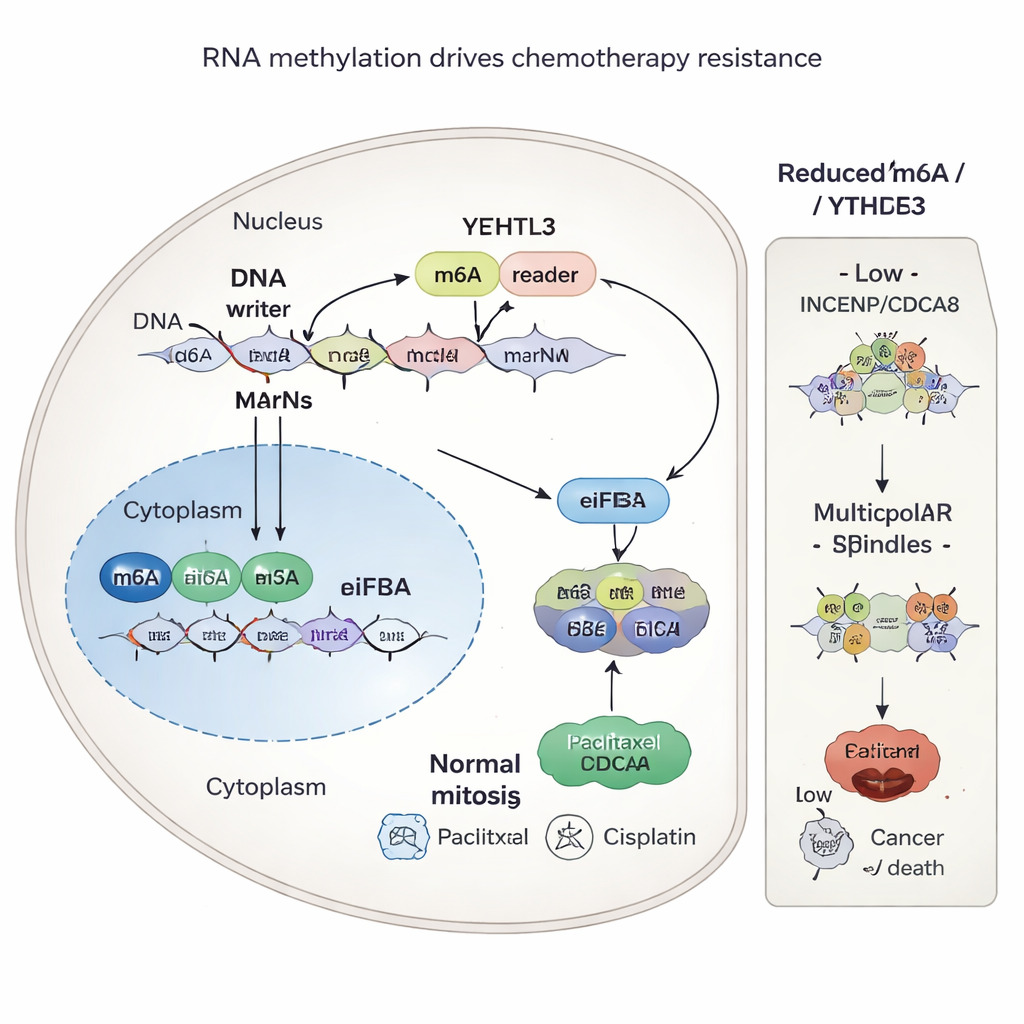
Chemiczna „łatka” na RNA, która napędza oporność
Badanie szukało dalej, dlaczego INCENP i CDCA8 występują w tak dużych ilościach w guzach opornych. Odpowiedź doprowadziła do subtelnej modyfikacji chemicznej RNA zwanej m6A, która działa jak regulator tego, jak wydajnie informacje genetyczne są odczytywane na białka. Enzym METTL3 dodaje te znaczniki m6A w konkretnych miejscach na matrycach RNA dla INCENP i CDCA8. Inne białko, YTHDF3, rozpoznaje te znaczniki i pomaga rekrutować maszynerię translacyjną komórki, zwiększając produkcję tych dwóch białek. Gdy naukowcy zmniejszyli poziomy METTL3 lub YTHDF3, albo zablokowali YTHDF3 małą cząsteczką o nazwie Ebselen, znaczniki m6A zniknęły lub zostały zignorowane, poziomy INCENP i CDCA8 spadły, a komórki nowotworowe stały się bardziej podatne na chemioterapię.
Zakłócanie podziału komórek, by wzmocnić chemioterapię
INCENP i CDCA8 są częścią większego zespołu zwanego kompleksu pasażerskiego chromosomów, który zapewnia równy podział chromosomów między komórki potomne. W komórkach opornych wysokie poziomy tych białek pomagają utrzymać uporządkowaną, dwubiegunową wrzecionę podziałową, co pozwala rakowi przetrwać uszkodzenia wywołane paklitakselem i cisplatyną. Gdy INCENP i CDCA8 są tłumione, komórki często tworzą wadliwe, wielobiegunowe wrzeciona. Ten chaos w segregacji chromosomów skłania komórki raka do śmierci, wzmacniając zabójczą siłę chemioterapii. Co istotne, zdolność INCENP i CDCA8 do ochrony komórek zależała od specyficznych miejsc m6A w ich RNA; mutacja tych miejsc usuwała oporność.
Powyżej jednego typu nowotworu
Ponieważ kombinacja paklitakselu i cisplatyny jest także stosowana w raku płuc i piersi, zespół przeanalizował także próbki biopsji od pacjentów z tymi nowotworami. We wszystkich trzech typach nowotworów osoby, których guzy miały niskie poziomy INCENP, CDCA8 i YTHDF3 przed terapią, znacznie częściej dobrze reagowały na leczenie. Analizy statystyczne wykazały, że połączenie tych trzech markerów daje szczególnie dobrą moc rozróżniania prawdopodobnych responderów od nie-responderów, sugerując praktyczny panel testów możliwy do zastosowania w różnych nowotworach.
Co to oznacza dla pacjentów i lekarzy
Mówiąc prosto, praca ta identyfikuje molekularny „odcisk palca”, który pomaga wyjaśnić, dlaczego niektóre guzy ignorują silną chemioterapię. Wysokie poziomy INCENP i CDCA8, napędzane przez system kontroli oparty na m6A z udziałem METTL3 i YTHDF3, pozwalają komórkom nowotworowym dzielić się poprawnie nawet pod kątem działania leków. Pomiar tych białek w biopsji mógłby pomóc lekarzom przewidzieć, czy połączenie paklitakselu i cisplatyny prawdopodobnie pomoże danemu pacjentowi, oszczędzając innym nieefektywnego leczenia. Równocześnie leki blokujące tę ścieżkę mogłyby być łączone ze standardową chemioterapią, by przechylić oporne guzy w kierunku śmiertelnych błędów podziału, potencjalnie poprawiając przeżycie osób z kilkoma głównymi typami nowotworów.
Cytowanie: Wang, X., Wang, T., Wang, K. et al. INCENP and CDCA8 predict neoadjuvant chemotherapy response and outcomes in esophageal squamous cell carcinoma. Nat Commun 17, 1672 (2026). https://doi.org/10.1038/s41467-026-68371-x
Słowa kluczowe: chemioterapia neoadiuwantowa, rak płaskonabłonkowy przełyku, oporność na chemioterapię, markery INCENP i CDCA8, metylacja RNA m6A