Clear Sky Science · pl
Proteazy zależne od ubikwityny K48 rozcinają białka poopuszczające ER
Jak komórki decydują, które białka zniszczyć
Nasze komórki nieustannie usuwają zużyte lub uszkodzone białka, zwłaszcza te osadzone w błonach, które pełnią funkcję bramek i czujników. Artykuł ten pokazuje, że komórki używają małej etykiety zwanej ubikwityną nie tylko jako ogólnego oznaczenia „do wyrzucenia”, lecz jako kodu, który mówi białkom błonowym dokładnie, jak zostaną rozłożone. Zrozumienie tego kodu pomaga wyjaśnić, jak komórki utrzymują zdrowie, i może nakreślić ścieżki terapeutyczne, które celowo eliminują białka powodujące choroby.
Komórkowy kod kreskowy dla usuwania białek
Komórki ozdabiają niechciane białka łańcuchami małej cząsteczki o nazwie ubikwityna. Łańcuchy te mogą być łączone na różne sposoby, trochę jak koraliki przewleczone przez różne otwory, i każdy wzorzec może sygnalizować inny los. Autorzy skupili się na białkach błonowych, które opuściły już retikulum endoplazmatyczne (ER) i przemieszczają się przez takie przedziały jak aparat Golgiego i endosomy. Zastanawiali się, czy dwa powszechne typy łańcuchów, zwane połączeniami K48 i K63, są naprawdę zamienne, czy też kierują ładunek różnymi drogami degradacji.
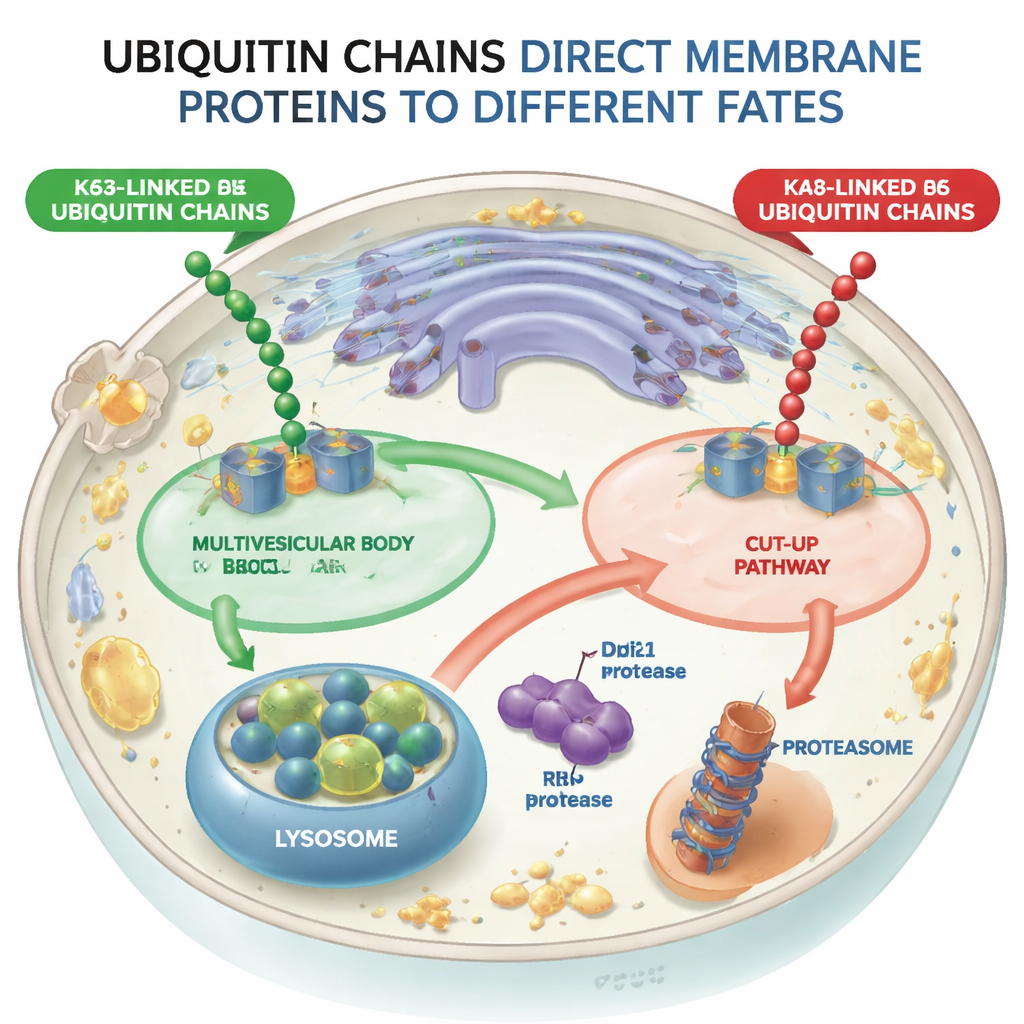
Dwie rozbieżne ścieżki dla oznaczonych białek
Używając komórek drożdży jako modelu, badacze zaprojektowali molekularne maszyny (ligazy ubikwitynowe), które mogły przyłączać albo łańcuchy typu K48, albo K63 do tego samego testowanego białka błonowego, receptora sortującego Vps10. Gdy Vps10 otrzymywał łańcuchy K63, kierowano go do pęcherzyków wewnętrznych w endosomach — struktur zwanych ciałkami wielopęcherzykowymi (multivesicular bodies), które ostatecznie łączą się z lizosomami, komórkowymi „kompartmentami trawiennymi”. Natomiast gdy Vps10 nosił łańcuchy K48, nie podążał tą wielopęcherzykową drogą. Zamiast tego był rozkładany w zupełnie inny sposób, co dowodzi, że komórka rozróżnia te dwa typy łańcuchów i że szlak multivesicular skutecznie odrzuca ładunki oznaczone K48.
Ścieżka „ROZCIĘCIE”, która kraje białka na pół
Zespół odkrył, że łańcuchy K48 wywołują drogę ścinania białek, którą nazwali CUT-UP, skrót od Cleavage of Ubiquitinated Targets by Ubiquitin-dependent Proteases. Zamiast wyciągać całe białko z błony naraz, CUT-UP tnie je na fragmenty, które następnie są dokończone przez istniejące systemy usuwania komórkowego. Jedne z kluczowych enzymów, Ddi1, unosi się w cytosolu i odcina część białka błonowego zwróconą ku cytoplazmie. Ten fragment jest potem trawiony przez proteasom, główną „niszczarkę” białek komórki. Równocześnie inny enzym, Rbd2, siedzi w samej błonie i odcina część białka skierowaną do wnętrza przedziału, uwalniając ją do przestrzeni, która ostatecznie łączy się z lizosomem. Zablokowanie Ddi1, Rbd2, proteasomu oraz enzymów lizosomalnych razem było konieczne, by w pełni uchronić Vps10 oznaczony K48 przed zniszczeniem, co potwierdza, że wszystkie te składniki współdziałają w ścieżce CUT-UP.
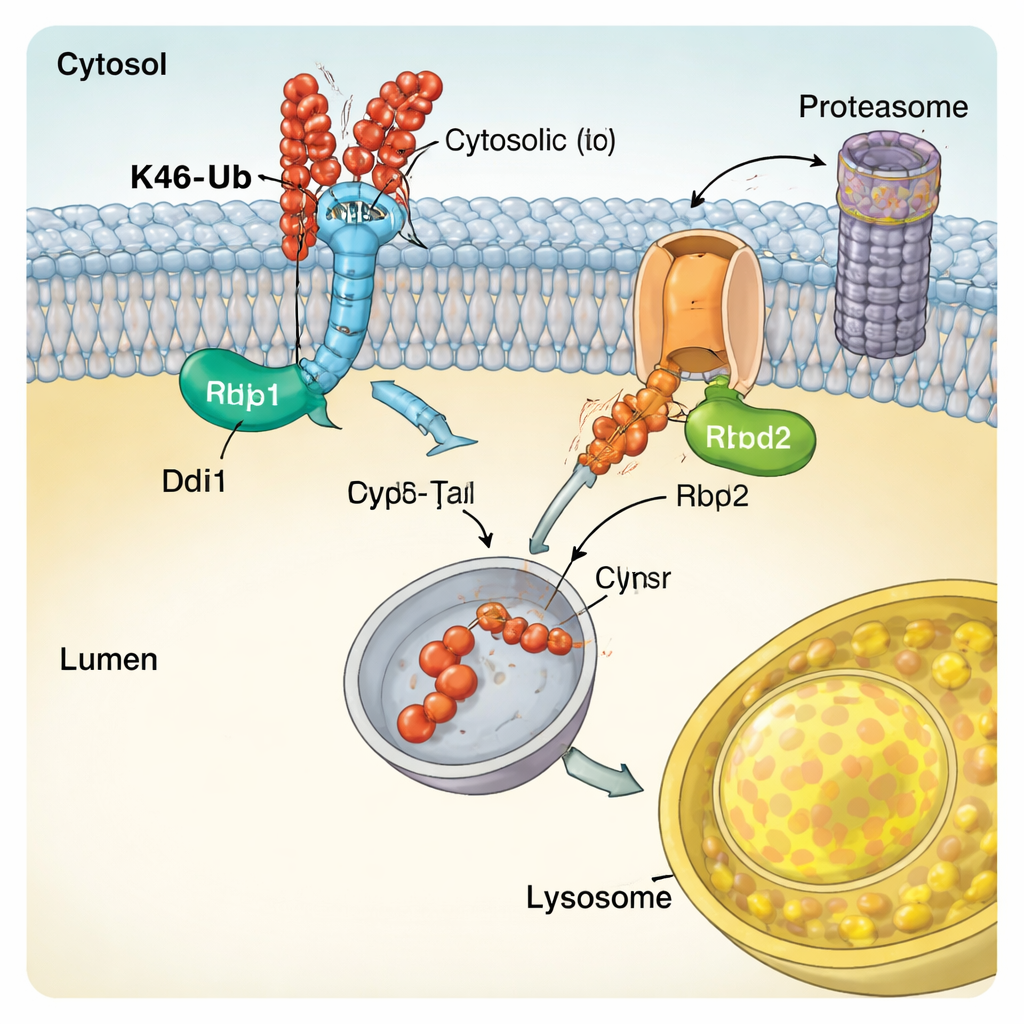
Specjalizowane enzymy odczytujące kod ubikwityny
Aby zrozumieć, jak CUT-UP rozpoznaje cele, autorzy zbadali cechy molekularne Ddi1. Pokażali, że centralne jądro katalityczne Ddi1 nie tylko przecina białka, ale potrafi też bezpośrednio wiązać ubikwitynę, a jego aktywność jest regulowana przez dodatkowe regiony, które uchwytują łańcuchy ubikwitynowe. Ddi1 wykazywał szczególne powinowactwo do łańcuchów K48, co odpowiada jego roli w CUT-UP. Rbd2 natomiast jest proteazą romboidową przechodzącą przez błonę. Badanie wykazało, że aktywne miejsce Rbd2 jest niezbędne do cięcia części Vps10 zwróconych do świetliska przedziału oraz że enzym ten przemieszcza się przez kilka przedziałów sekretoryjnych, co pozwala mu działać w wielu miejscach komórki. Podobne enzymy występują w komórkach ludzkich i wiąże się je ze schorzeniami od neurodegeneracji po nowotwory, co sugeruje, że mechanizmy podobne do CUT-UP mogą mieć szerokie znaczenie.
Dlaczego to ma znaczenie dla zdrowia i terapii
Pokazując, że różne typy łańcuchów ubikwityny kierują to samo białko błonowe w zupełnie odmienne losy — albo sortowanie do ciałek wielopęcherzykowych, albo rozcinanie mediowane przez CUT-UP — praca ta dostarcza mocnych dowodów, że komórki używają rzeczywistego „kodu ubikwityny” do precyzyjnego dostrajania usuwania białek. Odkrycie CUT-UP wyjaśnia, jak uparte białka błonowe można rozłożyć kawałek po kawałku i wskazuje Ddi1 oraz Rbd2 jako kluczowych odczytywaczy i egzekutorów tego kodu. Dla czytelników niebędących specjalistami najważniejszy wniosek jest taki, że komórki nie tylko oznaczają białka jako śmieci; precyzują także, jak te śmieci zostaną wyniesione. Gdy projektanci leków tworzą narzędzia znakujące szkodliwe białka ubikwityną, zrozumienie dróg takich jak CUT-UP będzie niezbędne do przewidzenia, jakie fragmenty powstaną i jaki to może mieć wpływ na zachowanie komórki.
Cytowanie: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
Słowa kluczowe: kod ubikwityny, degradacja białek, białka błonowe, proteasom, lizosom