Clear Sky Science · pl
Utrata sygnalizacji Fsr sprzyja tworzeniu biofilmów i pogarsza wyniki w enterokokowym zapaleniu wsierdzia
Cisi sabotażyści na zastawkach serca
Zapalenie wsierdzia to zagrażająca życiu infekcja zastawek serca, której częstość rośnie na całym świecie. W badaniu skoncentrowano się na głównym sprawcy — jelitowym bakterium Enterococcus faecalis — i zadano pytanie, dlaczego niektóre zakażenia są wyjątkowo trudne do leczenia. Odkrywając, jak te bakterie komunikują się między sobą i tworzą ochronne biofilmy na zastawkach, autorzy ujawniają, dlaczego niektóre szczepy wywołują cięższe choroby i opierają się antybiotykom, oraz dlaczego jeden system komunikacji bakteryjnej, zwany Fsr, okazuje się zaskakująco hamulcem, a nie przyspieszaczem uszkodzeń.
Jak bakterie budują twierdze w sercu
Zastawki serca zwykle są wystawione na jedne z najszybszych przepływów krwi w organizmie, ale jeśli powierzchnia zastawki zostanie uszkodzona, płytki krwi i białka krzepnięcia mogą utworzyć drobny skrzep, czyli wegetację. Ten skrzep staje się lądowiskiem dla bakterii krążących we krwi. Po przyczepieniu się bakterie się mnożą i splatają w biofilm — śliską, zorganizowaną społeczność, która chroni je przed komórkami układu odpornościowego i lekami. Zespół użył urządzeń mikroprzepływowych, by naśladować przepływ krwi w laboratorium, i modelu szczura, aby odtworzyć zapalenie wsierdzia u żywych zwierząt, co pozwoliło obserwować, jak E. faecalis adaptuje się, gdy zakażenie przechodzi od kilku rozproszonych komórek do gęstych, dojrzałych biofilmów. 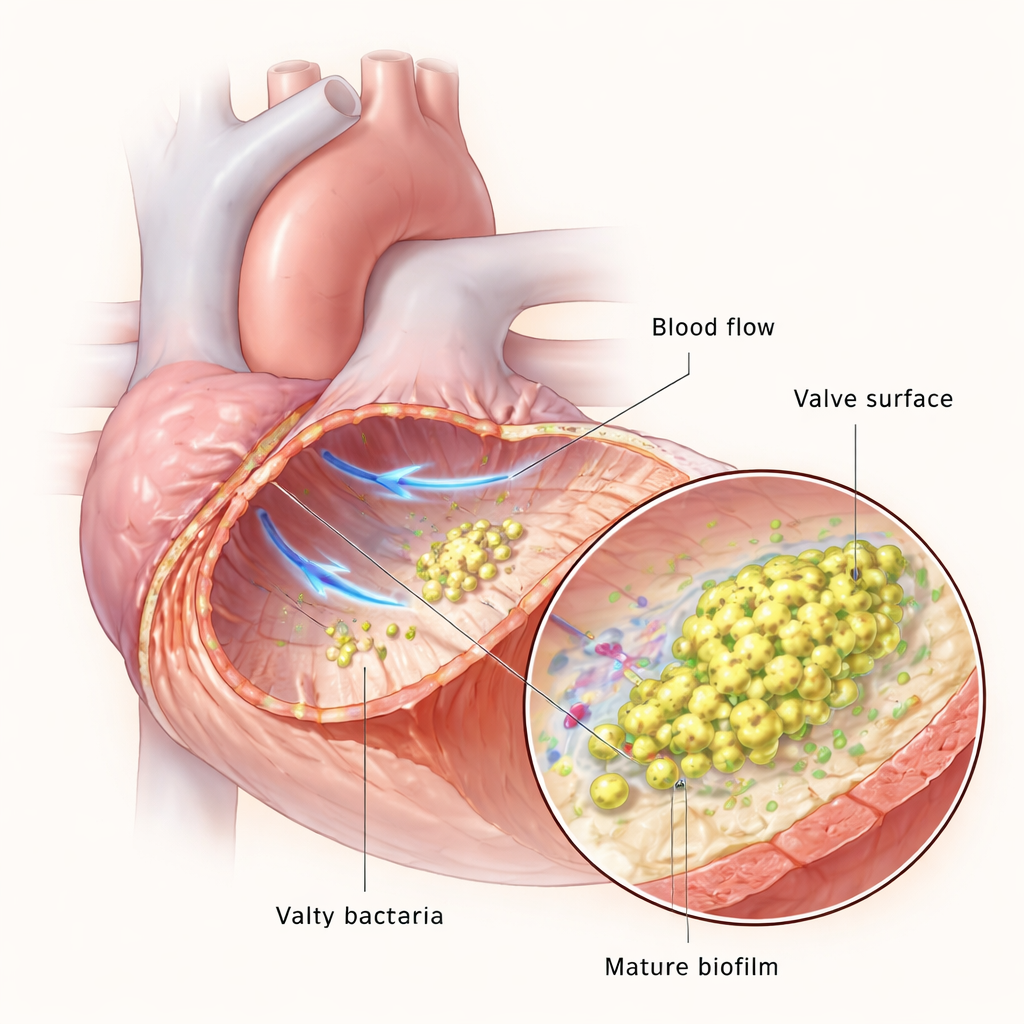
Gdy silny przepływ krwi wyłącza bakteryjny „szmer”
Bakterie często koordynują swoje zachowanie za pomocą quorum sensing — chemicznego systemu „głosowania”, który włącza lub wyłącza geny, gdy komórek jest wystarczająco dużo. Fsr to system quorum sensing używany przez E. faecalis. Ku zaskoczeniu badaczy, silny, poruszający się płyn faktycznie zmywał cząsteczki sygnałowe potrzebne do aktywacji Fsr. We wczesnym stadium zakażenia, gdy bakterie siedzą na odsłoniętej powierzchni wegetacji i odczuwają pełną siłę przepływu krwi, Fsr jest w dużej mierze uśpiony. Dopiero później, gdy mikrokolonie rosną i zanurzają się głębiej wewnątrz wegetacji — chronione przed przepływem — Fsr się aktywuje. Oznacza to, że w prawdziwym sercu quorum sensing zależy nie tylko od liczby bakterii, lecz także od ich położenia w trójwymiarowej strukturze.
Wyłączenie Fsr pozwala biofilmom bujnie rosnąć
Aby sprawdzić, co Fsr rzeczywiście wnosi do przebiegu zakażenia, zespół porównał bakterie dzikiego typu z mutantami pozbawionymi całego systemu Fsr. Początkowo obie wersje kolonizowały zastawki równie dobrze. Jednak po trzech dniach zwierzęta zakażone szczepami pozbawionymi Fsr miały większe wegetacje i znacznie więcej bakterii w nich zgęszczonych. Szczegółowe obrazy pokazały, że ich biofilmy pokrywały większą część powierzchni skrzepu, a mikrokolonie były większe. Utrata Fsr wyłączała też dwa kluczowe wydzielane enzymy, GelE i SprE, które normalnie kształtują biofilm i mogą ograniczać nadmierny wzrost. Zwierzęta zakażone mutantami pozbawionymi tylko tych enzymów także rozwijały obfitsze biofilmy, chociaż nie tak ekstremalne jak w szczepach pozbawionych całego Fsr, co sugeruje, że za zjawisko odpowiadają także inne czynniki kontrolowane przez Fsr. 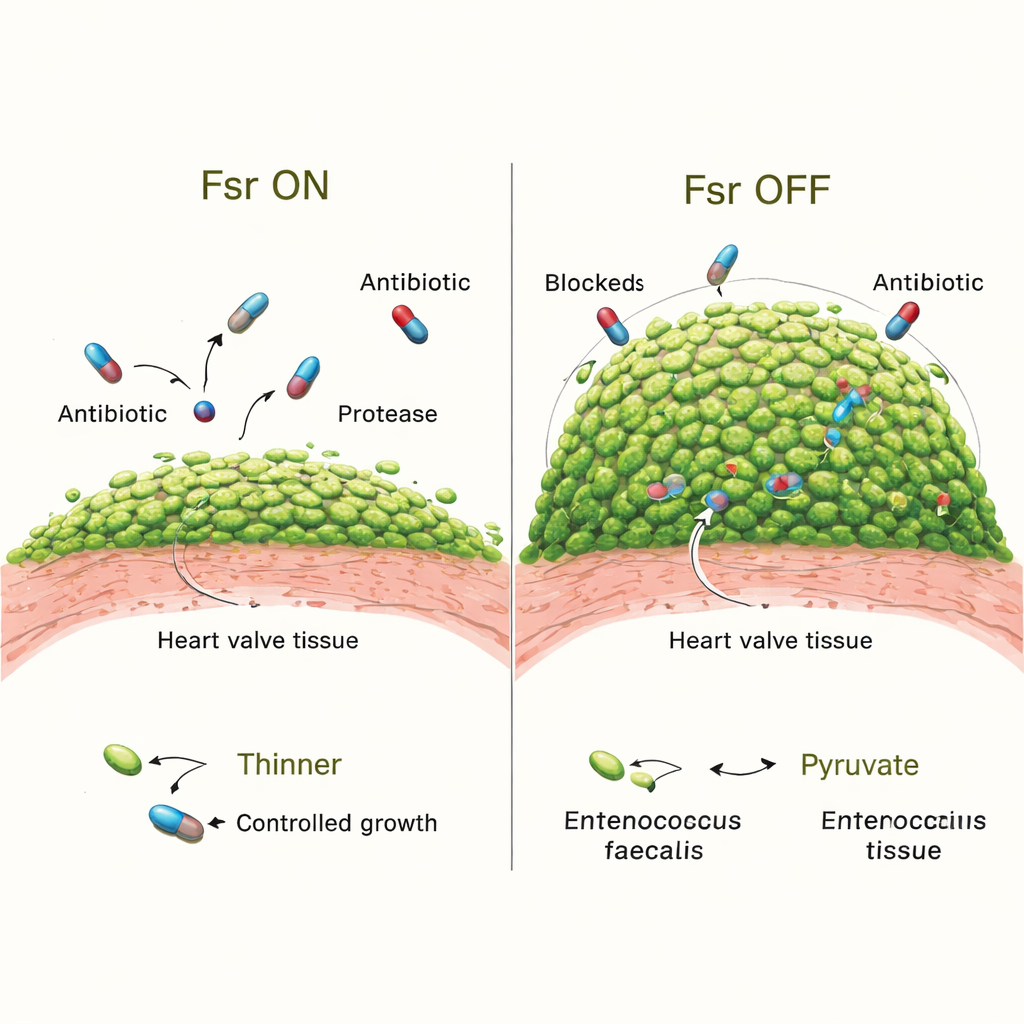
Przestawienie metabolizmu i silniejszy opór wobec antybiotyków
Profilowanie ekspresji genów bakterii wewnątrz zakażonych zastawek ujawniło, że Fsr robi znacznie więcej niż kontroluje kilka enzymów. Bez Fsr setki genów zmieniły aktywność, szczególnie te zaangażowane w pobieranie cukrów i produkcję energii. Para genów lrgA i lrgB wyróżniała się: była silnie włączona w bakteriach pozbawionych Fsr i pomagała komórkom lepiej wykorzystywać pirogronian — małą, energetyczną cząsteczkę obecna we krwi. Gdy badacze usunęli lrgAB razem z Fsr, nadmierny wzrost biofilmu zniknął, co wskazuje na kluczową rolę tej ścieżki metabolicznej w napędzaniu przerostu zakażenia. Co istotne, biofilmy bez Fsr były też trudniejsze do leczenia. U szczurów leczonych gentamycyną zakażenia szczepami dzikiego typu zmniejszały się, a liczba płytek krwi — wskaźnik ciężkości choroby — poprawiała się. Natomiast zakażenia pozbawione Fsr niemal nie reagowały na leczenie, mimo że w standardowych testach laboratoryjnych bakterie nie wykazywały większej oporności na lek.
Specyfika zapalenia zależna od gatunku
Badanie ujawniło również potencjalny sposób, w jaki te bakterie mogą wzbudzać zapalenie u ludzi. Enzym GelE potrafi przeciąć ludzki prekursor sygnału immunologicznego IL‑1β do aktywnej formy, która wywołuje odpowiedź zapalną. Co ciekawe, GelE ciął szczurzy IL‑1β inaczej — raczej rozkawałkowywał go niż aktywował — a precyzyjne „aktywujące” cięcie było nieobecne w białkach szczurów i myszy. Ten specyficzny dla gatunku efekt sugeruje, że u ludzi GelE może skupiać zapalenie bezpośrednio przy krawędzi biofilmu, co może nasilać uszkodzenie tkanek podczas zapalenia wsierdzia.
Od laboratorium do kliniki: dlaczego utrata Fsr ma znaczenie dla pacjentów
Aby sprawdzić, czy te eksperymentalne obserwacje mają znaczenie w praktyce, badacze przeanalizowali izolaty E. faecalis od 81 pacjentów z zapaleniem wsierdzia w Szwajcarii i Stanach Zjednoczonych. Prawie połowa szczepów naturalnie nie miała systemu Fsr. Pacjenci zakażeni tymi szczepami Fsr‑ujemnymi mieli dłuższe bakteriemie — więcej dni z wykrywalnymi bakteriami we krwi — i częściej trafiali do grupy o wysokiej ciężkości choroby, obejmującej opiekę intensywną, przedłużony pobyt w szpitalu, poważne zabiegi kardiologiczne lub zgon. Inne geny wirulencji nie wyjaśniały tego wzorca, wskazując bezpośrednio na utratę Fsr jako istotny marker bardziej agresywnego przebiegu choroby.
Dlaczego to ma znaczenie dla przyszłych terapii
Razem te wyniki obalają prostą ideę, że blokowanie komunikacji bakteryjnej zawsze osłabi zakażenia. W enterokokowym zapaleniu wsierdzia system Fsr w rzeczywistości powstrzymuje rozszerzanie biofilmu i zwiększa wrażliwość bakterii na antybiotyki. Gdy Fsr jest nieobecny, bakterie tworzą gęstsze biofilmy, efektywniej wykorzystują składniki odżywcze krwi i sprzyjają uporczywym, przedłużającym się zakażeniom. Dla pacjentów oznacza to, że szczepy pozbawione Fsr mogą zwiastować trudniejszy do leczenia przebieg, a terapie, które bezmyślnie wyłączają quorum sensing, mogą w tym kontekście zaszkodzić. Zamiast tego lepsze może okazać się ukierunkowanie ścieżek metabolicznych, takich jak wykorzystanie pirogronianu, albo monitorowanie statusu Fsr i GelE jako markerów prognostycznych, co może dać lepsze sposoby zarządzania tymi groźnymi infekcjami serca.
Cytowanie: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
Słowa kluczowe: zapalenie wsierdzia, bakteryjne biofilmy, quorum sensing, Enterococcus faecalis, tolerancja na antybiotyki