Clear Sky Science · pl
Zmodyfikowane VPg saRNA osiąga bezkapowy, niskoimmunogenny i precyzyjny zapis terapeutycznych białek in vivo
Pisząc nowe zasady dla leków RNA
Szczepionki oparte na informacyjnym RNA (mRNA) pomogły odwrócić bieg pandemii COVID-19, jednak wykorzystanie podobnych cząsteczek do zastępowania lub uzupełniania brakujących białek w chorobach przewlekłych jest znacznie trudniejsze. Organizm szybko usuwa obce RNA i uruchamia silne reakcje immunologiczne, a wiele istniejących projektów samopowielającego się RNA popełnia błędy podczas kopiowania. W tym badaniu opisano nowy rodzaj samopowielającego się RNA — zbudowany z elementów ludzkiego norowirusa — zaprojektowany tak, by był długotrwały, mniej zapalny i wyjątkowo dokładny, otwierając drogę do bardziej precyzyjnych i trwałych leków RNA.
Mądrzejsze RNA, które się kopiuje
Konwencjonalne leki mRNA niosą pojedynczą „instrukcję” dla białka i są odczytywane przez komórkę tylko raz, zanim ulegną rozkładowi. Samopowielające się RNA (saRNA) zawiera dodatkowe mechanizmy wirusowe pozwalające RNA kopiować się wewnątrz komórek, znacząco zwiększając produkcję przy niskiej dawce. Najlepiej zbadane systemy saRNA pochodzą od alfawirusów, ale są duże, wywołują silne odpowiedzi przeciwwirusowe i kopiują sekwencje z relatywnie niską dokładnością. Autorzy sięgnęli zamiast tego po norowirusa ludzkiego, powszechną przyczynę zapalenia żołądka i jelit. Wyizolowali kompaktowy fragment materiału genetycznego norowirusa i przebudowali go jako nośnik dla genów terapeutycznych. W jego centrum znajduje się VPg, małe białko wirusowe chemicznie przyłączone do przedniego końca RNA. VPg zastępuje zwykłą „czapeczkę” (cap) obecna na ludzkich mRNA i pozwala, by RNA było translacyjnie odczytywane przez inny zestaw czynników komórkowych, mniej wrażliwych na pewne sygnały stresowe. 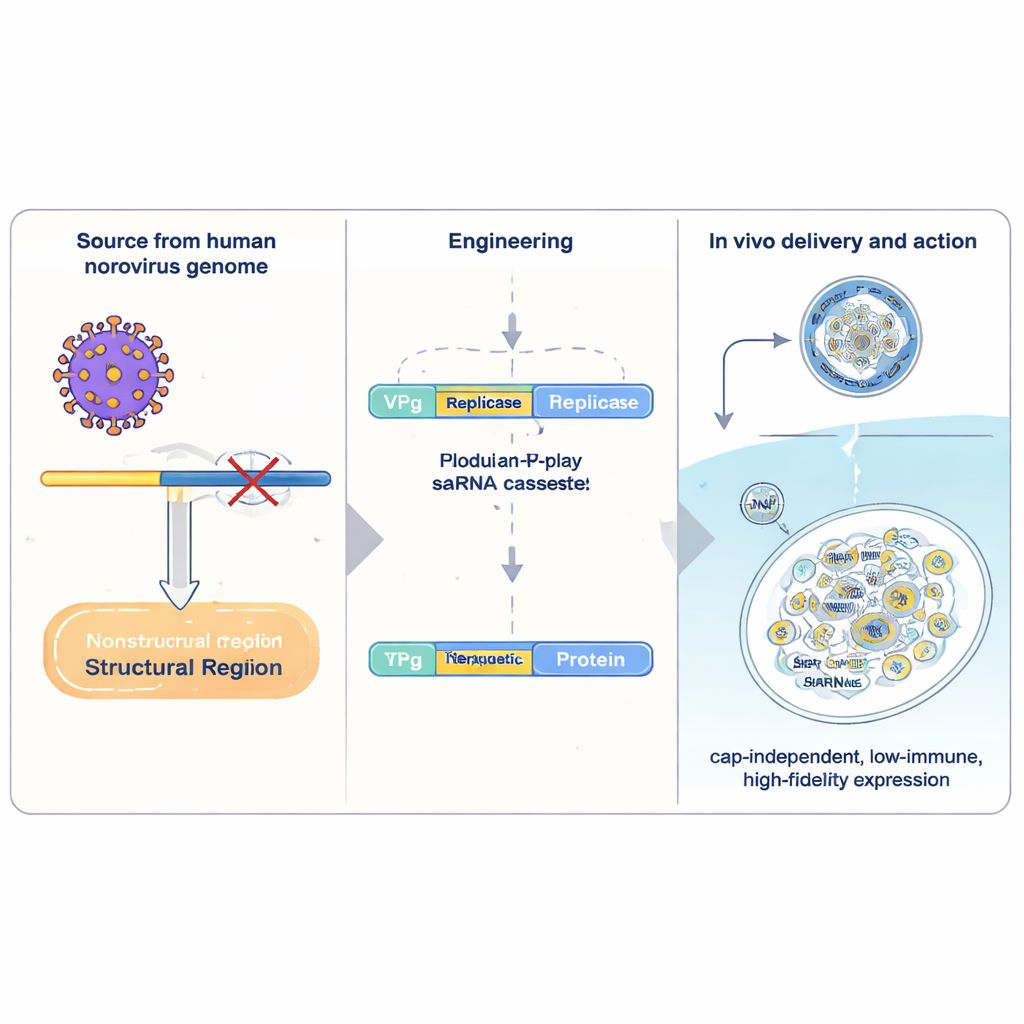
Wysoka dokładność bez wywoływania odporności
Dla terapii białkowych precyzja ma znaczenie: nawet drobne błędy kopiowania mogą zmieniać działanie leku lub tworzyć toksyczne produkty uboczne. Zespół wykazał, że gdy VPg norowirusa wiąże się z enzymem kopiującym RNA (polimerazą), spowalnia tempo, w jakim dodawane są nieprawidłowe nukleotydy, co ostro zmniejsza częstość błędów. Wyszczególnili konkretne aminokwasy w VPg, które stykają się z kluczowym obszarem kontrolnym polimerazy i wykazali, że zaburzenie tej interakcji obniża dokładność kopiowania. Klasyczne projekty saRNA jednocześnie generują duże ilości dwuniciowego RNA, molekularnego alarmu, który aktywuje mechanizmy przeciwwirusowe i wyłącza produkcję białek. Przeprojektowując polimerazę tak, by preferowała jedną, określoną formę startową powiązaną z VPg oraz reorganizując genom tak, by tylko terapeutyczny wątek był efektywnie produkowany, autorzy znacznie zredukowali powstawanie dwuniciowego RNA. Dodatkowo dostroili region ogonowy RNA, tak by VPg przyłączał się we właściwym miejscu, zapobiegając powstawaniu krótkich, niezamierzonych fragmentów, które mogłyby być tłumaczone na obce peptydy.
Działa tam, gdzie standardowe mRNA zawodzi
Nowe saRNA oparte na VPg przetestowano w wymagających modelach chorobowych, w których zwykłe mRNA z capem radzi sobie słabo. W kacheksji związanej z rakiem — zespole wyniszczenia, w którym mięśnie i tkanka tłuszczowa zanikają — kluczowe czynniki translacyjne rozpoznające standardową czapeczkę mRNA są wyłączone, co czyni mRNA zależne od cap niewydajnym. Ponieważ VPg wykorzystuje alternatywne wejście do maszynerii translacyjnej komórki, nadal napędzał produkcję hormonu głodu i metabolizmu, greliny, w modelu myszy z rakiem trzustki. Miesięczne, niskodawkowe wstrzyknięcia pomogły zachować mięśnie i tłuszcz, poprawiły apetyt i metabolizm oraz nieznacznie wydłużyły przeżycie, bez widocznej toksyczności czy oznak przewlekłej aktywacji układu odpornościowego.
Precyzyjny atak na nowotwór i łagodniejsza autoimmunizacja
Aby sprawdzić, czy wysoka wierność kopiowania rzeczywiście ma znaczenie, badacze załadowali wektor VPg skomplikowanym onkolitycznym konstruktorem GSDMDENG, zaprojektowanym tak, by tworzyć otwory w mitochondriach komórek nowotworowych i pobudzać odpowiedź immunologiczną specyficzną dla guza. Gdy ten sam konstrukt umieszczono na konwencjonalnym saRNA alfawirusa, mutacje kumulowały się w kolejnych rundach kopiowania i osłabiały selektywne właściwości zabijania raka oraz funkcje pobudzające odporność. W przeciwieństwie do tego system VPg zachował zamierzoną sekwencję, wywołał silne niszczenie komórek nowotworowych i wygenerował trwałe odpowiedzi limfocytów T, które spowolniły lub zapobiegały rozwojowi raka trzustki w modelach mysich. Na koniec zastosowano saRNA VPg w innym wyzwaniu: przewlekłej chorobie przeszczep przeciw gospodarzowi, w której komórki odpornościowe atakują płuca po przeszczepieniu szpiku kostnego. saRNA VPg kodujące aktywowane białko C zmniejszyło tworzenie szkodliwych przeciwciał, zapobiegło bliznowaceniu płuc i poprawiło oddychanie u myszy, podczas gdy porównywalny konstrukt oparty na alfawirusie wywołał silniejszą odporność wrodzoną i pogorszył wyniki.
Dlaczego to ma znaczenie dla przyszłych leków RNA
Podsumowując, praca opisuje kompaktową platformę RNA „plug-and-play”, łączącą trzy pożądane cechy: samopowielanie z wysoką wiernością, projekt minimalizujący alarmy immunologiczne oraz omijanie niektórych ograniczeń translacji standardowego mRNA. Ponieważ gen terapeutyczny jest po prostu wstawiany do stałego szkieletu opartego na norowirusie, wiele różnych białek — od hormonów po regulatory krzepnięcia i środki onkolityczne — można testować na tej samej platformie. Choć przed zastosowaniem u ludzi wciąż pozostało wiele pracy, podejście VPg saRNA wskazuje drogę ku lekom RNA, które zachowują się bardziej jak stabilne infuzje białkowe: niskodawkowe, o dłuższym działaniu i zaprojektowane do działania nawet w chorych tkankach, gdzie zwykłe wiadomości mRNA nie są niezawodnie odczytywane. 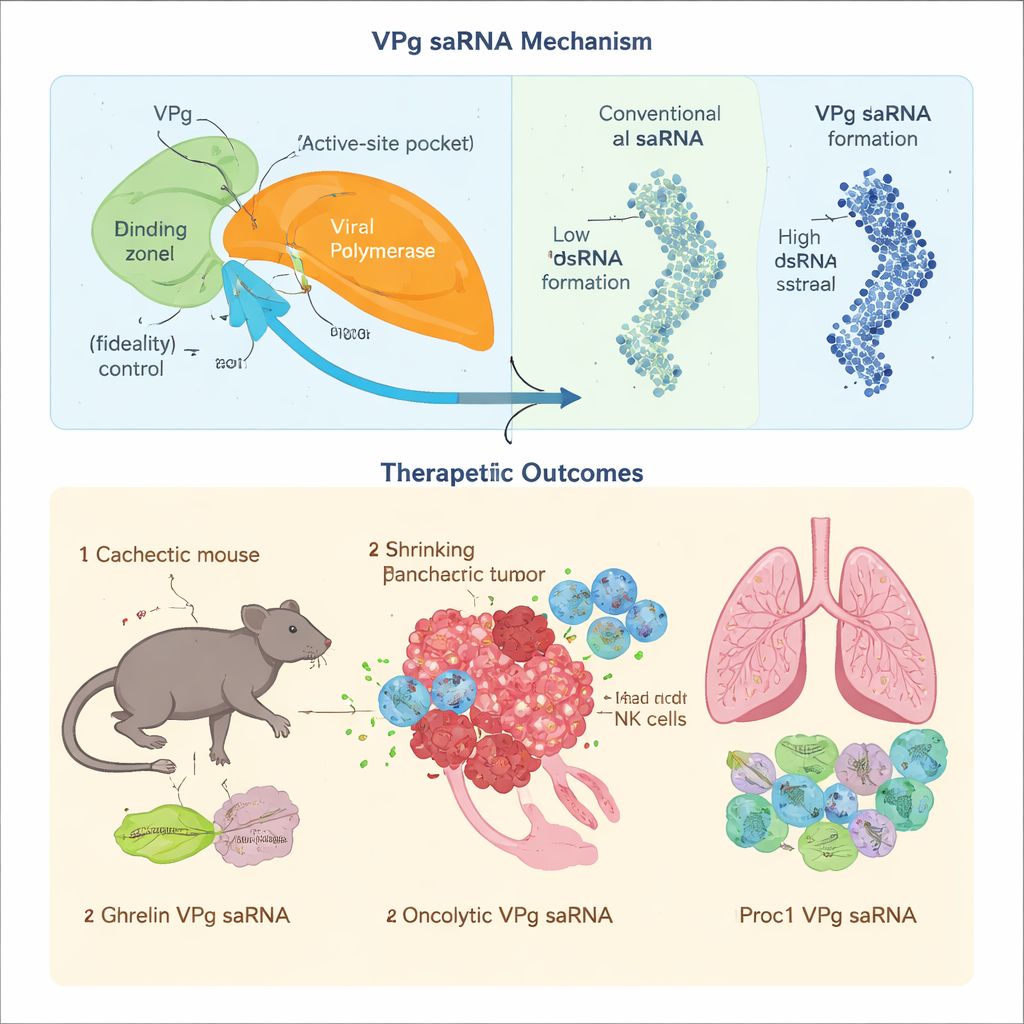
Cytowanie: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
Słowa kluczowe: samopowielające się RNA, terapie mRNA, VPg norowirusa, kacheksja nowotworowa, choroba przeszczep przeciw gospodarzowi