Clear Sky Science · pl
Rola powtórzeń o niskiej złożoności w interakcjach RNA–RNA oraz ramy uczenia głębokiego do przewidywania dimerów
Lepkie sekwencje RNA, które kształtują zachowanie komórek
W każdej komórce cząsteczki RNA ciągle się ze sobą zderzają, tworząc przelotne pary, które pomagają kontrolować, które geny są włączone, jak powstają białka i jak rozwijają się komórki. To badanie pokazuje, że wiele z tych spotkań RNA–RNA nie jest przypadkowych: kierują nimi krótkie, proste, wysoko powtarzalne sekwencje działające jak molekularne rzepy. Autorzy opracowali też narzędzie sztucznej inteligencji, które potrafi wskazać miejsca, gdzie takie pary RNA prawdopodobnie się utworzą, otwierając nowe sposoby badania funkcjonowania komórek w zdrowiu i chorobie.
Proste powtórzenia o silnym wpływie
RNA bywa opisywane jako posłaniec przenoszący informację z DNA do białek, ale pełni też funkcje rusztowania, regulatora i przewodnika. Wiele z tych ról zależy od wiązania się dwóch nici RNA. Łącząc dane z kilku dużych badań eksperymentalnych na komórkach ludzkich i mysich, autorzy pokazują, że regiony RNA zaangażowane w takie parowanie są silnie wzbogacone w to, co nazywają powtórzeniami o niskiej złożoności. To odcinki zbudowane z krótkich motywów — na przykład serii nukleotydów G i C — powtarzanych wielokrotnie. Zamiast być genomowym „śmieciem”, fragmenty te okazują się zasadniczymi miejscami przyczepu, gdzie jedno RNA może przylgnąć do wielu innych, tworząc gęste węzły interakcji w całym transkryptomie. 
Węzły RNA w rozwoju i regulacji
Gdy zespół przeanalizował, które geny niosą te bogate w powtórzenia miejsca kontaktu, wyłonił się uderzający wzorzec: wiele z nich koduje białka kontrolujące rozwój i tożsamość komórek, jak czynniki transkrypcyjne. Nawet w liniach komórkowych nowotworowych, które nie przechodzą aktywnej różnicacji, RNA powiązane z programami rozwojowymi było silnie zaangażowane w kontakty oparte na powtórzeniach. Autorzy przyjrzeli się też konkretnym długim RNA niekodującym (lncRNA), które nie kodują białek, lecz często je regulują. Na przykład cele lncRNA TINCR i innego lncRNA ważnego dla tworzenia neuronów ruchowych, Lhx1os, wykazywały nadmiar komplementarnych powtórzeń. W tych przypadkach proste powtórzenia na lncRNA są dopasowane przez komplementarne powtórzenia w ich partnerach RNA, co umożliwia stabilne parowania, mogące modulować poziomy lub translację kluczowych genów rozwojowych.
Gdzie do akcji dołączają białka i enzymy edycyjne
Te kontakty napędzane powtórzeniami rzadko działają samotnie. Autorzy nałożyli mapy wiązania białek na swoje dane o interakcjach i odkryli, że wiele miejsc kontaktowych z powtórzeniami jest także rozpoznawanych przez białka wiążące RNA zaangażowane w kontrolę translacji, degradację RNA i tworzenie cytoplazmatycznych ziarnistości, takich jak P-body i ziarnistości stresowe. Szczególnie jedno białko, STAU1, które może inicjować niszczenie swoich celów RNA, często wiąże dimerowe struktury tworzone przez powtórzenia o niskiej złożoności. Zmniejszenie poziomu STAU1 prowadziło do wyższych stężeń RNA uczestniczących w tych dimerach, zwłaszcza tych zawierających powtórzenia, co sugeruje, że parowanie RNA pośredniczone powtórzeniami może oznaczać transkrypty do kontrolowanej degradacji. Te same regiony bogate w powtórzenia przyciągają też enzymy edycyjne, takie jak ADAR1, które chemicznie modyfikują konkretne zasady w dwuniciowym RNA, co sugeruje, że powtórzenia o niskiej złożoności pomagają pozycjonować miejsca edycji, dopracowujące zachowanie RNA.
Nauczanie sieci neuronowej rozpoznawania kontaktów RNA
Standardowe programy komputerowe próbują przewidywać wiązanie RNA–RNA głównie na podstawie stabilności termodynamicznej — ile energii potrzeba, by utworzyć lub rozerwać dimer. Choć użyteczne, modele te często nie wychwytują rzeczywistych interakcji obserwowanych w komórkach, szczególnie między długimi RNA. Aby pójść dalej niż proste zasady energetyczne, autorzy wytrenowali model uczenia głębokiego nazwany RIME, który korzysta z osadzeń w stylu „modelu językowego”: numerycznych reprezentacji sekwencji RNA kodujących wzorce nauczone z ogromnych zbiorów danych kwasów nukleinowych. RIME pokazuje się pary segmentów RNA i uczy klasyfikować, czy wchodzą w interakcję, używając wielu rzeczywistych par z eksperymentów z krzyżowaniem na psoralenie jako przykładów pozytywnych oraz starannie skonstruowanych par nieinteragujących jako negatywów. 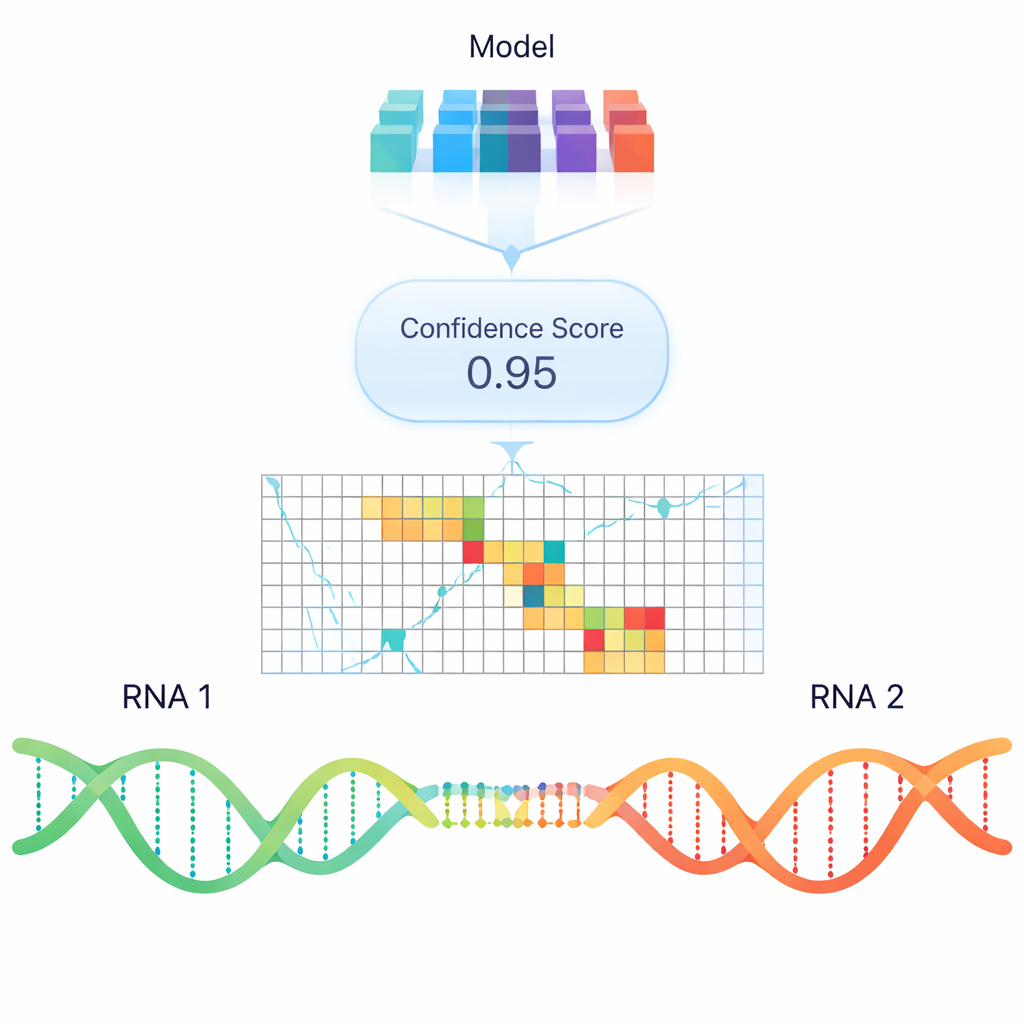
Mądrzejsze przewidywania i nowe wskazówki biologiczne
W testach porównawczych z wiodącymi narzędziami opartymi na termodynamice oraz inną metodą sieci neuronowej, RIME konsekwentnie lepiej odróżnia prawdziwe kontakty RNA–RNA od podróbek, zwłaszcza dla eksperymentalnych interakcji o wysokim zaufaniu. Model nie tylko przewiduje, czy dwa RNA się sparują, ale też zwykle wskazuje dokładne zaangażowane regiony i naturalnie uczy się, że powtórzenia o niskiej złożoności są silnymi predyktorami kontaktu. Co niezwykłe, ten sam model, trenowany tylko na interakcjach między różnymi RNA, dobrze sprawdza się także w przewidywaniu wewnętrznego parowania zasad w pojedynczej cząsteczce RNA, zgodnego zarówno z eksperymentami strukturalnymi, jak i klasycznymi algorytmami fałdowania. Dla regulatorów niekodujących, takich jak TINCR, NORAD i SMaRT, RIME skutecznie odnajduje znane funkcjonalne miejsca interakcji i sugeruje dodatkowe kandydackie regiony.
Dlaczego to ma znaczenie
Dla czytelnika popularnonaukowego kluczowa wiadomość jest taka, że krótkie, powtarzalne odcinki w RNA — kiedyś łatwe do zlekceważenia jako bezużyteczny szum — działają jako centralne punkty połączeń w sieci RNA komórki. Pomagają one łączyć RNA, przyciągać białka regulatorowe i enzymy edycyjne oraz są szeroko wykorzystywane w szlakach kontrolujących rozwój komórek i reakcję na stres. Nowy model RIME daje badaczom potężne narzędzie do przeszukiwania genomów w poszukiwaniu tych partnerstw RNA–RNA, w tym tych, które mogą się rozregulować w chorobach neurologicznych i innych związanych z ekspansjami powtórzeń. W istocie praca ta pokazuje, że zrozumienie — i przewidywanie — jak proste powtórzenia RNA do siebie przylegają, może odsłonić ukryte warstwy regulacji genów.
Cytowanie: Setti, A., Bini, G., Pellegrini, F. et al. The role of low-complexity repeats in RNA–RNA interactions and a deep learning framework for duplex prediction. Nat Commun 17, 1637 (2026). https://doi.org/10.1038/s41467-026-68356-w
Słowa kluczowe: Interakcje RNA–RNA, powtórzenia o niskiej złożoności, długie RNA niekodujące, uczenie głębokie, regulacja genów