Clear Sky Science · pl
Usuwanie pośrednich komórek nabłonka pęcherzykowego prowadzone przez sygnaturę transkryptomiczną łagodzi włóknienie płuc u myszy
Dlaczego bliznowacenie płuc ma znaczenie
Włóknienie płuc to poważna choroba, w której delikatne pęcherzyki oddechowe stopniowo zamieniają się w sztywne tkanki bliznowate, przez co każdy oddech staje się wysiłkiem. Lekarze wiedzą, że to bliznowacenie zaczyna się, gdy normalne procesy naprawcze wymykają się spod kontroli, ale nie było jasne, które konkretne komórki są za to odpowiedzialne ani jak je usunąć, nie uszkadzając zdrowej tkanki płucnej. W tym badaniu przeanalizowano nowy sposób „odczytywania” molekularnych komunikatów wewnątrz komórek płuc, wykorzystania tych informacji do identyfikacji szkodliwych komórek przejściowych i selektywnego ich eliminowania, aby zmniejszyć bliznowacenie u myszy.
Komórki przyłapane podczas błędnej naprawy
Po urazie płuc specjalne komórki produkujące surfaktant, zwane komórkami typu II, zwykle się namnażają, a następnie dojrzewają do cienkich komórek typu I, które wyścielają pęcherzyki i umożliwiają przejście tlenu do krwi. W przebiegu włóknienia wiele z tych komórek utknęło w stanie pośrednim, zamiast ukończyć tę przemianę. Poprzednie badania z wykorzystaniem sekwencjonowania RNA pojedynczych komórek wykryły te komórki pośrednie zarówno u myszy, jak i u ludzi, ale nie było jasne, czy są one jedynie obserwatorami, czy kluczowymi sprawcami choroby. Autorzy skupili się na mysiej populacji komórek przejściowych nazwanej Krt8+ alveolar differentiation intermediates oraz na ich ludzkich odpowiednikach znanych jako aberrant basaloid cells, które występują w dużych liczbach w przebarwionych płucach.
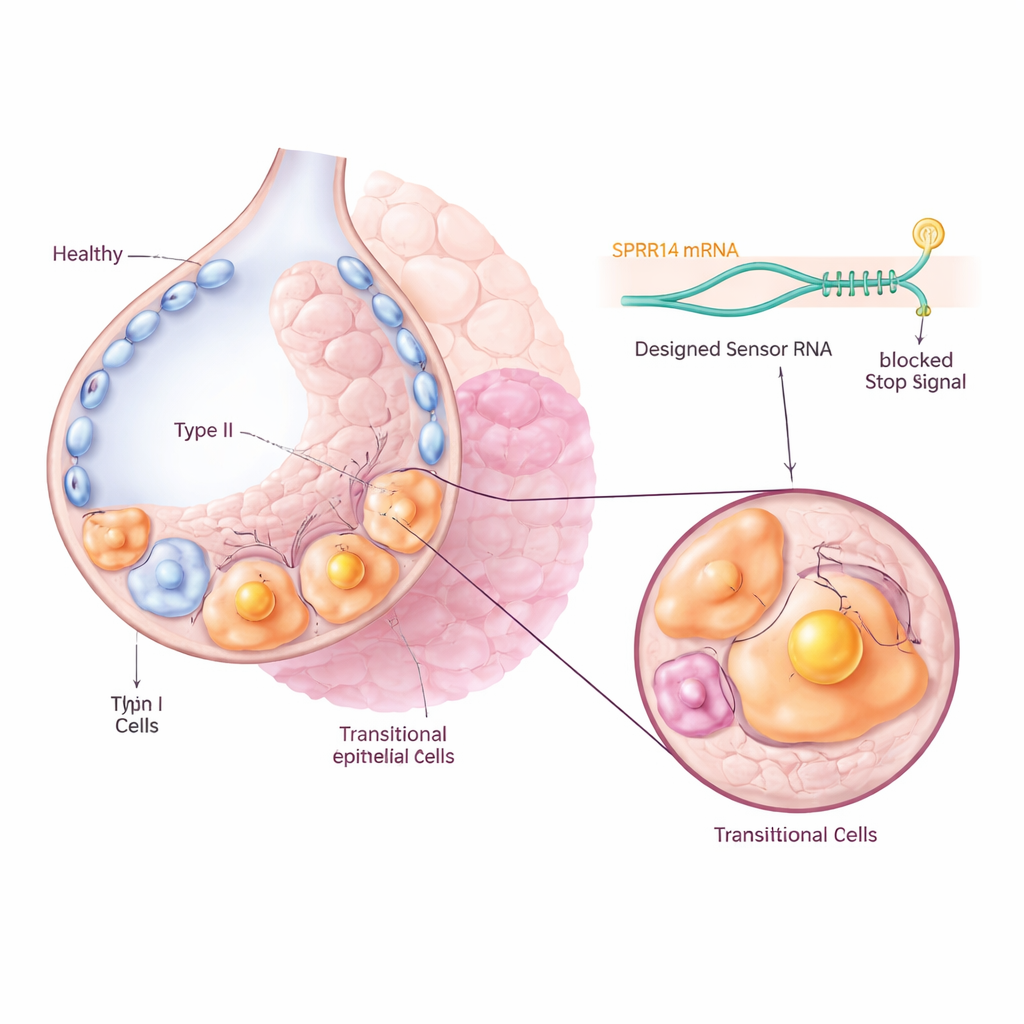
Znajdowanie unikalnej molekularnej plakietki
Aby celować w te problematyczne komórki, nie dotykając zdrowych sąsiadów, zespół najpierw przeszukał obszerne zbiory danych ekspresji genów w poszukiwaniu markera silnie i specyficznie włączonego w populacji przejściowej. Zidentyfikowali cząsteczkę o nazwie SPRR1A jako wyróżniającą się „plakietkę”: była ona wyraźnie wzbogacona w komórkach Krt8+ w włókniejących płucach myszy oraz w komórkach KRT5-/KRT17+ aberrant basaloid u pacjentów z idiopatycznym włóknieniem płuc, lecz w dużej mierze nieobecna w normalnych komórkach płuc. Mikroskopia tkanek płuc zarówno mysich, jak i ludzkich potwierdziła, że SPRR1A pojawia się głównie w uszkodzonych, przebudowanych obszarach, a nie w zdrowych pęcherzykach, co sugeruje, że może służyć jako precyzyjny uchwyt do identyfikacji sprawczych komórek.
Programowanie komórek za pomocą sensora RNA
Naukowcy użyli następnie niedawno opracowanej technologii o nazwie CellREADR, która działa jak wewnętrzny sensor molekularny. Zaprojektowali krótkie sekwencje RNA, które mogą komplementarnie parować się z RNA SPRR1A wewnątrz komórki. Gdy sensor wykryje SPRR1A, uruchamia produkcję dołączonego białka efektorowego, takiego jak znacznik fluorescencyjny lub receptor czyniący komórkę wrażliwą na lek. U myszy wirusy posłużyły do dostarczenia tych konstrukcji sensor–efektor do komórek płuc. Tylko komórki aktywnie produkujące SPRR1A włączyły sygnał fluorescencyjny, co pozwoliło zespołowi śledzić i izolować komórki przejściowe bezpośrednio z włókniejących płuc. Sekwencjonowanie pojedynczych komórek wykazało, że oznakowane komórki ściśle odpowiadały znanej sygnaturze genowej komórek przejściowych, potwierdzając, że sensor RNA celnie lokalizuje zamierzoną populację.
Wyłączanie szkodliwych pośredników
Następnie efektor został zmieniony z nieszkodliwego białka fluorescencyjnego na receptor toksyny błoniczej, aby komórki pozytywne na SPRR1A można było selektywnie zabić poprzez podanie toksyny błoniczej. Synchronizując leczenie z szczytową obecnością komórek przejściowych po chemicznym uszkodzeniu płuc, autorzy byli w stanie usunąć około jednej trzeciej tej populacji. To ukierunkowane wyeliminowanie doprowadziło do wyraźnie mniejszego bliznowacenia płuc: zaobserwowano zmniejszone gromadzenie kolagenu, niższe poziomy białek związanych z włóknieniem oraz pęcherzyki o bardziej normalnym wyglądzie. Szczegółowe analizy wykazały, że większość komórek pozytywnych na SPRR1A nosiła cechy stanu przypominającego stres i starzenie, z niewielką podgrupą zdolną do intensywnej proliferacji, co sugeruje, że te komórki przejściowe zarówno nie naprawiają prawidłowo tkanki, jak i przyczyniają się do podtrzymywania procesu włóknienia.
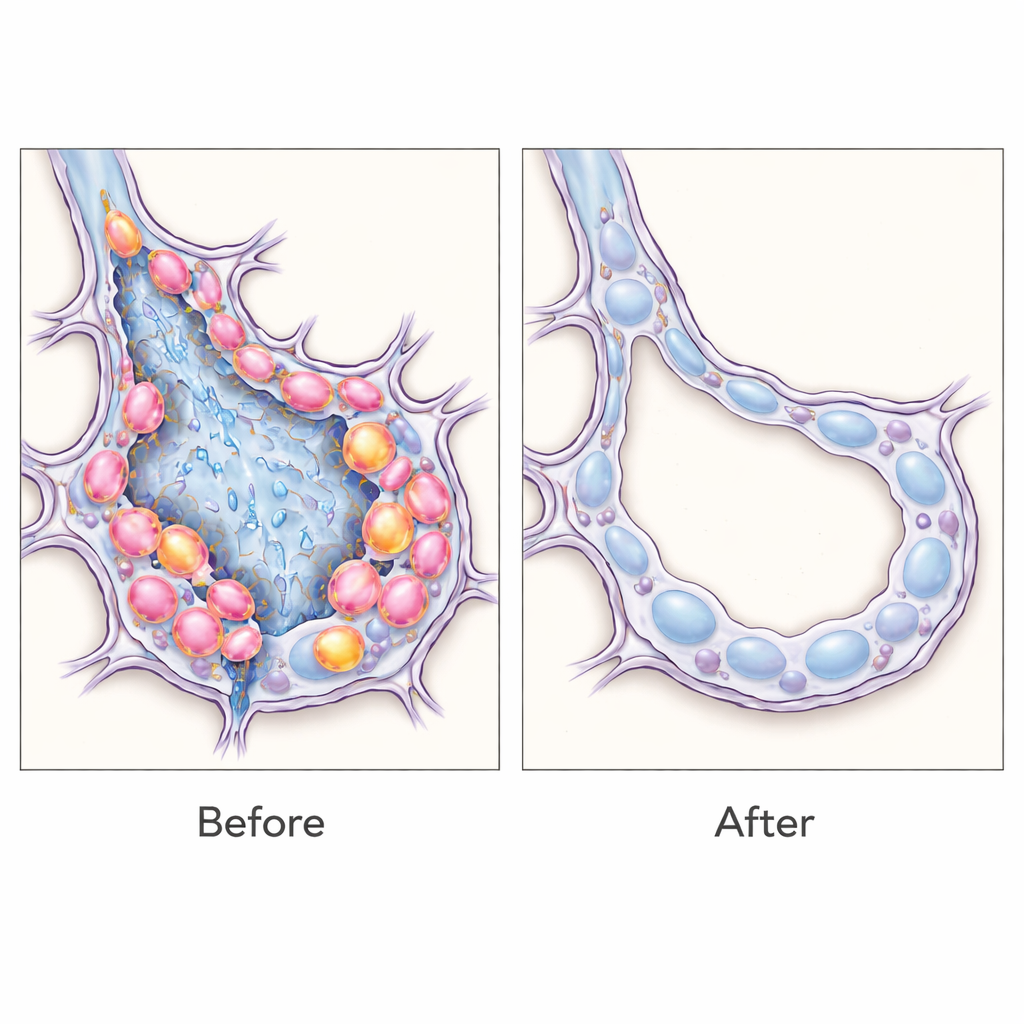
Co to oznacza dla przyszłych terapii
Wyniki te wskazują, że komórki nabłonkowe w stanie przejściowym nie są tylko markerami, lecz aktywnymi sprawcami włóknienia płuc, i że ich selektywne usuwanie może przechylić równowagę z powrotem w kierunku zdrowszej architektury płuc u myszy. Szerzej, praca demonstruje elastyczną strategię: poprzez „odczytywanie” komórkowo-specyficznych sygnatur RNA badacze mogą oznaczać, badać, a nawet eliminować precyzyjnie zdefiniowane populacje komórek w żywej tkance bez potrzeby tworzenia za każdym razem specjalnych linii zwierzęcych. Chociaż przed bezpiecznym zastosowaniem takich narzędzi wykrywających RNA u ludzi wciąż pozostaje wiele pracy, podejście to otwiera drogę do terapii precyzyjnych, które celują w dokładne typy komórek przeszkadzające w gojeniu przy przewlekłym bliznowaceniu płuc i potencjalnie innych chorobach włóknieniowych.
Cytowanie: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
Słowa kluczowe: włóknienie płuc, komórki nabłonka pęcherzykowego, sekwencjonowanie RNA pojedynczych komórek, technologia wykrywania RNA, senescencja komórkowa