Clear Sky Science · pl
Atlas pojedynczych jąder migdałowatego centralnego ujawnia dynamikę chromatyny i transkrypcji genów w ludzkim zaburzeniu używania alkoholu
Dlaczego te badania mają znaczenie w życiu codziennym
Zaburzenie używania alkoholu (AUD) dotyka miliony ludzi i ich rodzin, a mimo to wciąż wiemy zaskakująco niewiele o tym, co przewlekłe intensywne picie robi z ludzkim mózgiem na poziomie pojedynczych komórek. To badanie skupia się na jednym niewielkim, lecz kluczowym obszarze — centralnym migdałowatym, węźle odpowiedzialnym za strach, stres i motywację — aby zmapować, jak alkohol przekształca komórki mózgowe i ich systemy kontroli genetycznej. Łącząc najnowocześniejsze sekwencjonowanie „pojedynczych komórek” z badaniami genetycznymi ryzyka uzależnienia, autorzy zaczynają wyjaśniać, dlaczego niektórzy ludzie są bardziej podatni na AUD i jak alkohol pozostawia trwałe molekularne blizny w mózgu.
Uważne spojrzenie na mały węzeł mózgowy
Centralne migdałowate jest kluczową stacją wyjściową w sieci emocji i stresu mózgu i silnie wiąże się z łagodzeniem lęku, głodem alkoholowym i kompulsywnym piciem. W tym badaniu naukowcy przeanalizowali około 175 000 pojedynczych jąder komórkowych pobranych pośmiertnie z centralnego migdałowatego 50 osób — 22 z historią zaburzenia używania alkoholu i 28 bez AUD. Korzystając z technologii, która odczytuje jednocześnie aktywność genów (RNA) i dostępność chromatyny (jak „otwarta” lub „zamknięta” jest DNA) w tej samej komórce, zbudowali szczegółowy atlas wszystkich głównych typów komórek tego regionu, w tym kilku rodzajów neuronów i komórek wspomagających, takich jak astrocyty i mikroglej. Stwierdzili, że neurony hamujące — które tłumią lub kształtują aktywność mózgu — są szczególnie licznie obecne w centralnym migdałowatym i wydają się być szczególnie dotknięte u osób z AUD. 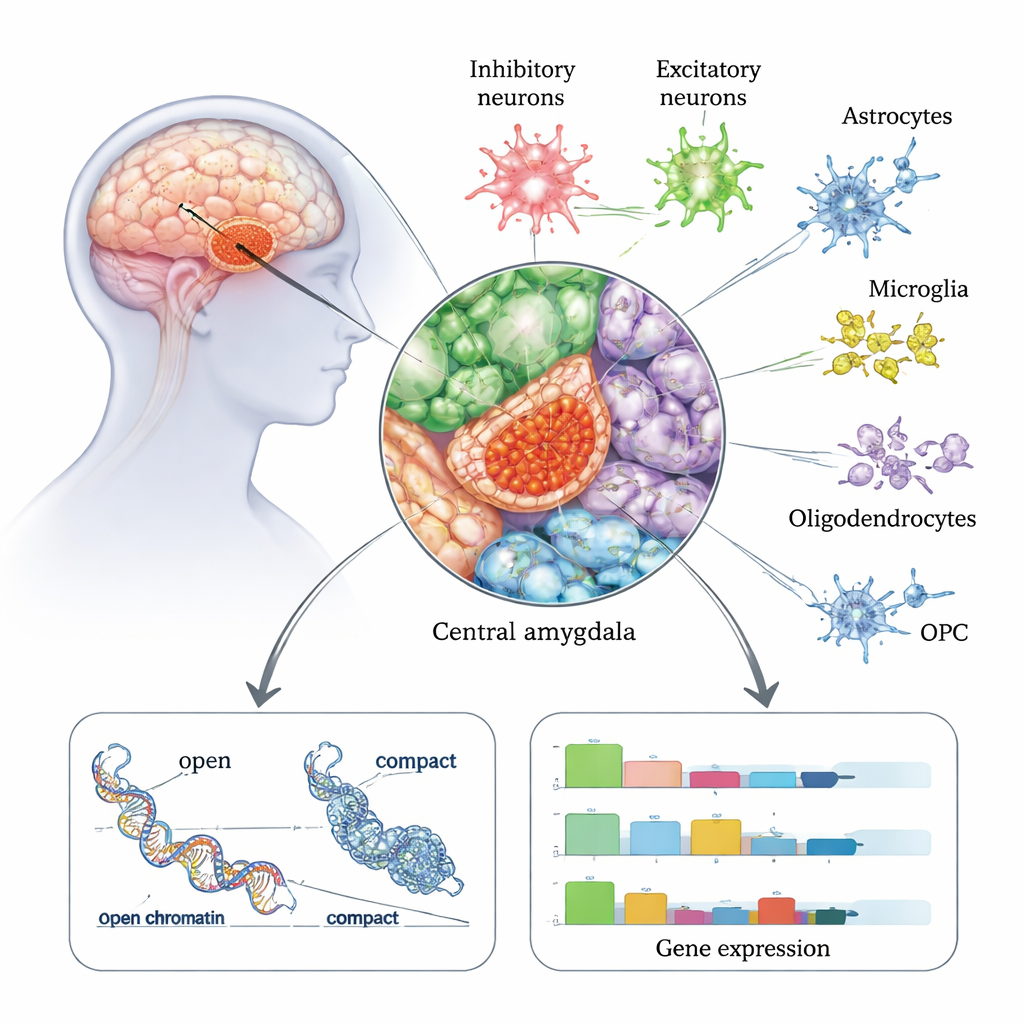
Które komórki i geny zmieniają się w zaburzeniu używania alkoholu?
Zespół systematycznie porównał aktywność genów u osób z AUD i bez niego, typ komórki po typie komórki. Odkryli ponad 1800 genów, których aktywność była zmieniona w konkretnych populacjach komórek, przy czym największe przesunięcia występowały w neuronach hamujących, a następnie w neuronach pobudzających i astrocytach. Jeden podtyp neuronów hamujących oznaczony peptydem proenkefaliną (PENK) wykazywał szczególnie silne zmiany. Wiele z dotkniętych genów bierze udział w komunikacji między komórkami mózgowymi, zwłaszcza w równowadze między pobudzającym glutaminianem a hamującym GABA. Na przykład gen GABRA2, który pomaga budować główny typ receptora GABA, był podwyższony w pewnych neuronach hamujących, podczas gdy GRM8, receptor glutaminianowy, oraz NCAM1, cząsteczka adhezji komórkowej ważna dla synaps, zmieniały się w przeciwnych kierunkach w różnych podtypach neuronów. Te wzorce sugerują, że precyzyjne dostrojenie pobudzenia i hamowania w centralnym migdałowatym jest zaburzone w AUD.
Przełączniki kontroli w mózgu: chromatyna i elementy regulacyjne
Geny nie działają samodzielnie; są kontrolowane przez odcinki DNA, które funkcjonują jak przełączniki i ściemniacze. Patrząc na chromatynę — sposób pakowania DNA — badacze zidentyfikowali ponad pół miliona kandydatów na elementy regulacyjne i powiązali je z pobliskimi genami w sposób specyficzny dla typu komórki. Niemal połowa tych elementów była unikatowa dla jednego typu komórki, co podkreśla wyspecjalizowanie różnych komórek mózgowych. Wiele elementów regulacyjnych zmienionych w AUD było połączonych z genami zaangażowanymi w gospodarkę wapniową i sygnalizację glutaminianową, takimi jak CALN1, gen wiążący wapń, silnie aktywny w neuronach. W neuronach hamujących CALN1 wykazywał zarówno zwiększoną ekspresję, jak i gęste skupiska pętli regulacyjnych, co sugeruje, że ekspozycja na alkohol przekształca lokalną architekturę DNA kontrolującą ten gen. 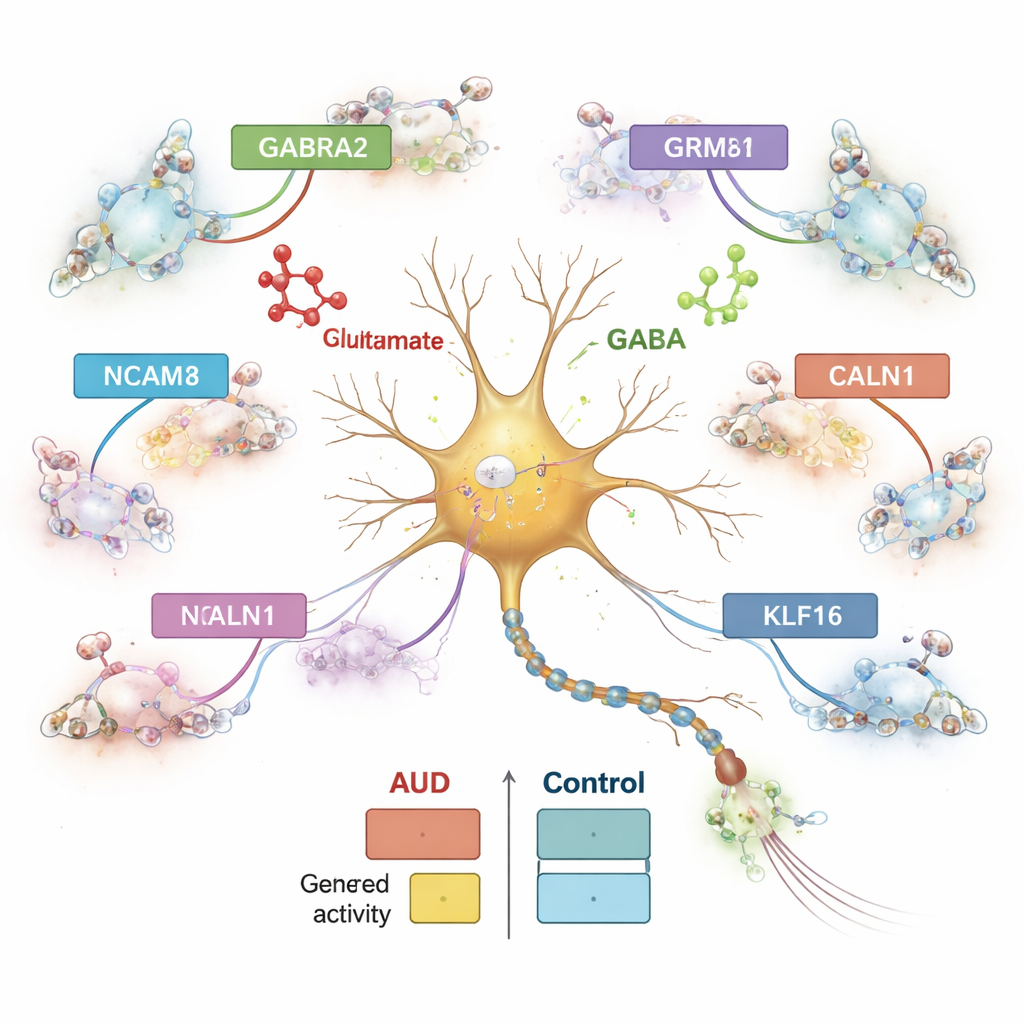
Od genów ryzyka do prawdziwych zmian w mózgu
Badania genetyczne zidentyfikowały wiele wariantów DNA zwiększających ryzyko rozwoju problemów z alkoholem, ale gdzie i jak działają w mózgu pozostawało niejasne. Nakładając swoje mapy pojedynczych komórek na duże badania asocjacyjne obejmujące cały genom dotyczące problematycznego używania alkoholu, autorzy odkryli, że geny ryzyka są nieproporcjonalnie aktywne i dysregulowane w neuronach centralnego migdałowatego, szczególnie w neuronach hamujących. Wskazali ponad 200 prawdopodobnych wariantów ryzyka leżących wewnątrz elementów regulacyjnych otwartych w określonych typach komórek. Niektóre z nich znajdowały się w genach już związanych z uzależnieniem, takich jak CACNA1C i DRD2, które pomagają kontrolować pobudliwość neuronów i sygnalizację dopaminergiczną. Inne, w tym SEMA6D i NF1, pojawiły się jako nowe kandydatury. Zespół zidentyfikował także rodzinę czynników transkrypcyjnych zwanych czynnikami Kruppela (zwłaszcza KLF16), które wydają się koordynować szerokie zmiany w genach związanych z wapniem i glutaminianem, i potwierdził części tej sieci regulacyjnej w modelu myszy po ostrej ekspozycji na alkohol.
Co to oznacza dla zrozumienia i leczenia AUD
Mówiąc wprost, to badanie pokazuje, że zaburzenie używania alkoholu nie jest jedynie rozproszonym problemem mózgowym, lecz wysoko zorganizowanym zaburzeniem skupionym w określonych typach komórek i szlakach molekularnych w krytycznym węźle emocjonalnym. Neurony hamujące centralnego migdałowatego, wraz z astrocytami i innymi komórkami wspomagającymi, wykazują skoordynowane zmiany w aktywności genów i w DNA‑owych przełącznikach kontrolujących te geny — szczególnie w systemach zarządzających sygnałami glutaminianu, GABA i wapnia. Łącząc te zmiany komórkowe z wariantami ryzyka genetycznego, praca ta oferuje mapę drogową łączącą odziedziczoną podatność z konkretnymi zdarzeniami molekularnymi w mózgu. Z czasem takie mapy specyficzne dla typów komórek mogą ukierunkować rozwój precyzyjniejszych terapii przywracających równowagę pobudzenia i hamowania, zamiast działać szeroko na cały mózg.
Cytowanie: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
Słowa kluczowe: zaburzenie używania alkoholu, migdałowate centralne, genomika pojedynczych komórek, neurony hamujące, regulacja genów