Clear Sky Science · pl
Od tworzenia kompleksu TDP-43/RNA do chorobowo powiązanej agregacji TDP-43: podejście strukturalne i komórkowe
Dlaczego to białko mózgowe ma znaczenie
Choroby neurodegeneracyjne, takie jak stwardnienie zanikowe boczne (ALS) i otępienie czołowo-skroniowe, często charakteryzują się skupiskami źle złożonych białek wewnątrz komórek nerwowych. Jednym z najczęstszych „winowajców” jest białko o nazwie TDP-43, które normalnie pomaga w przetwarzaniu RNA — roboczej kopii naszych genów. W tym badaniu zadano kluczowe pytanie: co TDP-43 robi w zdrowych komórkach i co idzie nie tak, że użyteczny pomocnik RNA zamienia się w toksyczne białko tworzące agregaty?
Jak TDP-43 działa w zdrowych komórkach nerwowych
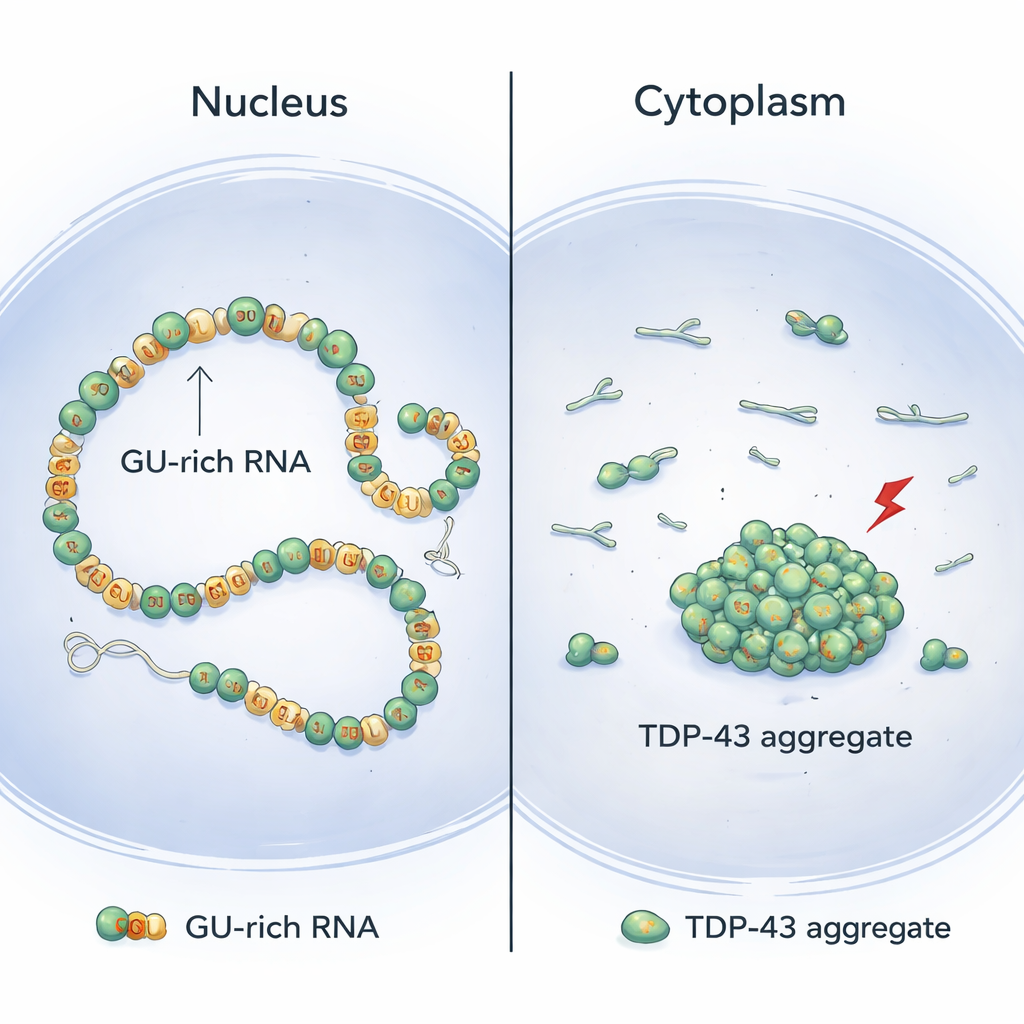
TDP-43 zwykle znajduje się w jądrze komórkowym, gdzie wiąże długie odcinki RNA bogate w powtarzające się motywy „GU”. Łącząc biologię strukturalną i eksperymenty komórkowe, autorzy pokazują, że cząsteczki TDP-43 układają się kooperatywnie wzdłuż tych regionów bogatych w GU, tworząc gładkie, ciągłe łańcuchy na RNA. W takim ułożeniu przednia część białka — domena N‑terminalna — pozostaje fizycznie rozdzielona między sąsiednimi cząsteczkami. Dzięki temu te fragmenty N‑terminalne pozostają dostępne, by sięgać i łączyć odległe sekcje bogate w GU tego samego RNA, delikatnie pętląc i kompaktując długie introny (niekodujące odcinki w obrębie genów) bez tworzenia grudek.
Wbudowana przeciąganina wewnątrz białka
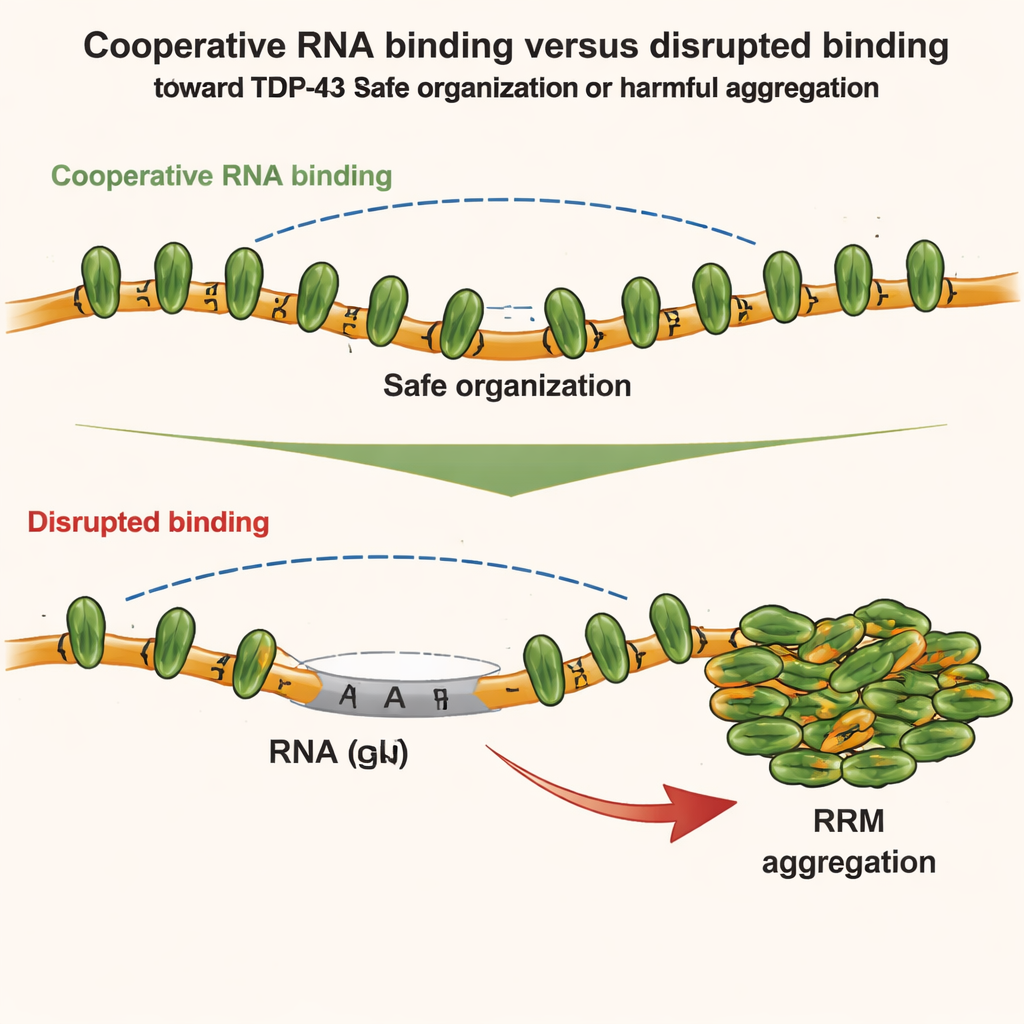
Zespół następnie zbadał, jak różne części TDP-43 konkurują lub współpracują ze sobą. Skupili się na dwóch regionach: domenie N‑terminalnej, która może przylegać do innych domen N‑terminalnych, oraz centralnych modułach wiążących RNA, które napędzają kooperatywne wiązanie wzdłuż RNA bogatego w GU. Korzystając z czułych technik, takich jak spektroskopia NMR, kalorymetria i dyfrakcja rentgenowska przy małym kącie, odkryli, że gdy TDP-43 wiąże RNA kooperatywnie, geometria łańcucha osłabia bezpośrednie kontakty N‑terminalne między sąsiednimi cząsteczkami. Innymi słowy, silne kooperatywne wiązanie RNA hamuje lokalne interakcje N‑terminalne. Jednak gdy ta kooperatywność zostaje zaburzona — na przykład przez wprowadzenie odcinków niebędących GU do RNA lub przez mutacje TDP-43 — regiony N‑terminalne sąsiednich białek zbliżają się do siebie i mogą się teraz ze sobą połączyć.
Od pomocnej kompaktacji do szkodliwego zlewania się
Wnioski strukturalne przetestowano w żywych komórkach. Autorzy wykorzystali zmodyfikowane systemy komórkowe, by śledzić, jak różne mutanty TDP-43 mieszają się lub rozdzielają wewnątrz sztucznych, bogatych w RNA przedziałów. Stwierdzili, że zarówno kooperatywne wiązanie z RNA, jak i interakcje N‑terminalne pomagają organizować TDP-43 w wyższej rzędowości strukturalnej, ale w różny sposób. Kooperatywne wiązanie układa białka wzdłuż regionów bogatych w GU, podczas gdy kontakty N‑terminalne łączą odległe klastry. Jednak w warunkach łagodnego stresu oksydacyjnego sytuacja się zmienia. Chemiczny czynnik stresowy (arsenit) powoduje specyficzne modyfikacje chemiczne — acetylację — w centralnych motywach wiążących RNA, co zwiększa ich skłonność do przylegania. Jeśli kooperatywne wiązanie z RNA jest nienaruszone, TDP-43 pozostaje w większości rozpuszczalny. Gdy jednak kooperatywność jest osłabiona, połączenia N‑terminalne między pobliskimi cząsteczkami TDP-43 działają jak rusztowanie, które zbliża acetylowane rdzenie i sprzyja nieodwracalnej agregacji.
Dlaczego TDP-43 bardziej zlewa się w cytoplazmie
Model wyłaniający się z tej pracy pomaga wyjaśnić, dlaczego agregaty TDP-43 często występują w cytoplazmie chorych neuronów, a nie w jądrze. W jądrze długie introny zawierające liczne powtórzenia GU są powszechne, co sprzyja ciągłemu, kooperatywnemu wiązaniu utrzymującemu ryzykowne kontakty N‑terminalne między sąsiadami na niskim poziomie i pozwalającemu na bezpieczne pętlowanie na duże odległości. Natomiast w cytoplazmie dojrzałe RNA mają znacznie mniej odcinków bogatych w GU. To powoduje, że wiązanie TDP-43 jest bardziej nieciągłe i mniej kooperatywne, zwiększając prawdopodobieństwo, że sąsiednie domeny N‑terminalne wejdą w interakcję i stworzą warunki do agregacji po wystąpieniu zmian chemicznych wywołanych stresem. Potwierdzając ten pogląd, sztuczne dostarczenie dodatkowych intronów bogatych w GU w jądrze zmniejszyło agregację TDP-43 pod wpływem stresu.
Co to oznacza dla przyszłych terapii
Mówiąc wprost, badanie przedstawia TDP-43 jako białko balansujące między użyteczną organizacją RNA a szkodliwym zlewaniem się, gdzie kooperatywne wiązanie z RNA bogatym w GU działa jak mechanizm zabezpieczający. Gdy ta siatka bezpieczeństwa zawiedzie — z powodu zmienionych sekwencji RNA, mutacji białka lub stresu komórkowego — te same domeny, które normalnie kompaktują długie segmenty RNA, mogą zamiast tego napędzać powstawanie toksycznych agregatów. Dla osób niezaznajomionych z dziedziną kluczowy wniosek jest taki, że utrzymanie właściwych interakcji między TDP-43 a RNA może być obiecującą strategią zapobiegania lub spowalniania zlewania się białka obserwowanego w ALS i pokrewnych chorobach mózgu.
Cytowanie: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
Słowa kluczowe: agregacja TDP-43, białka wiążące RNA, ALS, interakcje białko–RNA, neurodegeneracja