Clear Sky Science · pl
Atomowa precyzja w inżynierii ligandów nanocząstek złota za pomocą międzyfazowego transferu masy
Dlaczego maleńkie cząstki złota mają znaczenie dla zdrowia
Obrazowanie medyczne coraz częściej polega na nanocząstkach — maleńkich cząstkach kilka tysięcy razy mniejszych niż ludzki włos — które oświetlają narządy i guzy głęboko w ciele. Badanie to pokazuje, jak naukowcy potrafią teraz dopracować zewnętrzną powłokę ultrasmallnych cząstek złota niemal atom po atomie, tak aby ten sam świecący rdzeń można było skierować do różnych narządów, szczególnie przesuwając akumulację z wątroby i śledziony w stronę nerek. Taka kontrola może pomóc zaprojektować bezpieczniejsze środki kontrastowe i nośniki leków, które trafiają dokładnie tam, gdzie chce lekarz, i są usuwane z organizmu w bardziej uporządkowany sposób.
Wyzwanie: ubieranie maleńkich klastrów złota
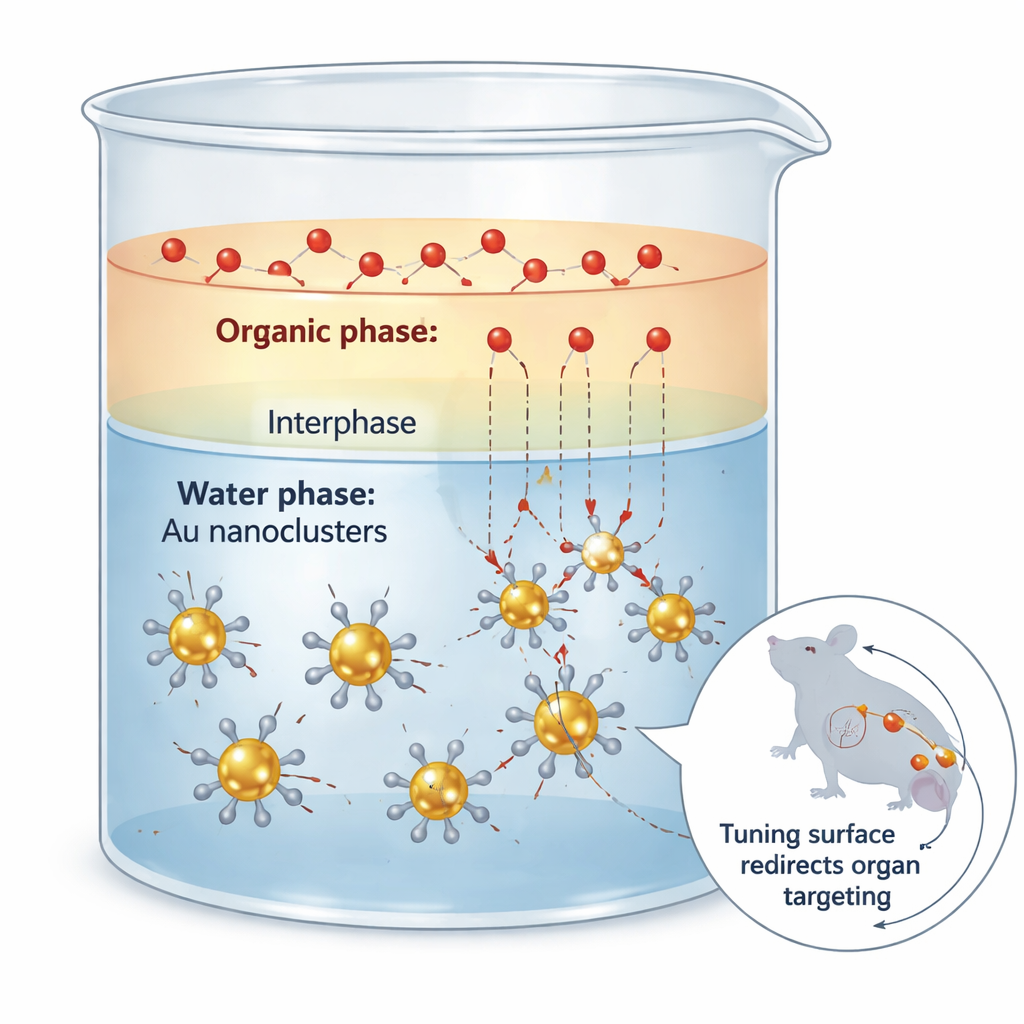
Nanoklustery złota to ultramałe cząstki, które zachowują się bardziej jak duże cząsteczki niż ziarna metalu. Mogą emitować światło w tzw. oknie bliskiej podczerwieni II, które penetruje tkanki głęboko i daje ostre obrazy przy niskim tle sygnału. Jednak niemal wszystko, co decyduje o zachowaniu tych klastrów w organizmie — gdzie się przemieszczają, jak długo krążą i jak są usuwane — zależy nie od złota, lecz od organicznych ligandów, czyli „powłoki” przyczepionej do ich powierzchni. Tradycyjne sposoby zmiany tej powłoki często przypominają grubą operację: reakcja przebiega zbyt szybko, powłoka staje się nierówna, a rdzeń złota może zostać częściowo „przeżarty”, co niszczy zarówno strukturę, jak i właściwości optyczne.
Spowalnianie ruchu między dwoma cieczami
Naukowcy rozwiązali ten problem, wykorzystując prostą koncepcję fizyczną: opór transferu masy na granicy między dwiema cieczami, które nie mieszają się całkowicie. Umieścili klastry złota w wodzie, a nadchodzące ligandy zawierające siarkę w rozpuszczalniku organicznym, takim jak octan etylu. W cienkiej strefie, gdzie obie cieczy częściowo się mieszają, ligandy powoli dyfundują w kierunku klastrów i wymieniają się z pierwotną powłoką. Dokładne pomiary kinetyki wykazały, że niepożądane „trawienie” rdzenia złota jest niezwykle czułe na stężenie ligandów, podczas gdy pożądana wymiana jest na to znacznie mniej wrażliwa. Dzięki dwufazowemu układowi, utrzymującemu niskie, lecz ciągle uzupełniane poziomy wolnych ligandów, zespół zredukował trawienie około sześćdziesięciokrotnie, zachowując jednocześnie dużą część użytecznej szybkości wymiany.
Budowanie precyzyjnego zestawu molekularnego
Dzięki tej międzyfazowo wspomaganej metodzie autorzy zdołali wymienić ligandy powierzchniowe na modelowym klastrze złota Au25 w sposób wysoko kontrolowany. Zaczęli od klastrów chronionych przez ujemnie naładowany ligand kwasu sulfonowego i podstawili różne nowe ligandy tiolowe niosące grupy karboksylowe, aminowe, hydroksylowe, nitrowe oraz hydrofobowe pierścienie aromatyczne. Spektrometria mas ujawniła czyste, dobrze zdefiniowane mieszaniny, takie jak klastry Au25 z określoną liczbą każdego typu ligandu, zamiast szerokich, nieuporządkowanych rozkładów. Metoda zadziałała także dla innych wielkości klastrów i rodzin ligandów, co sugeruje, że jest to ogólna strategia tworzenia trwałych, szytych na miarę nanoklustrów złota do różnych zastosowań.
Skierowanie nanocząstek z wątroby do nerek
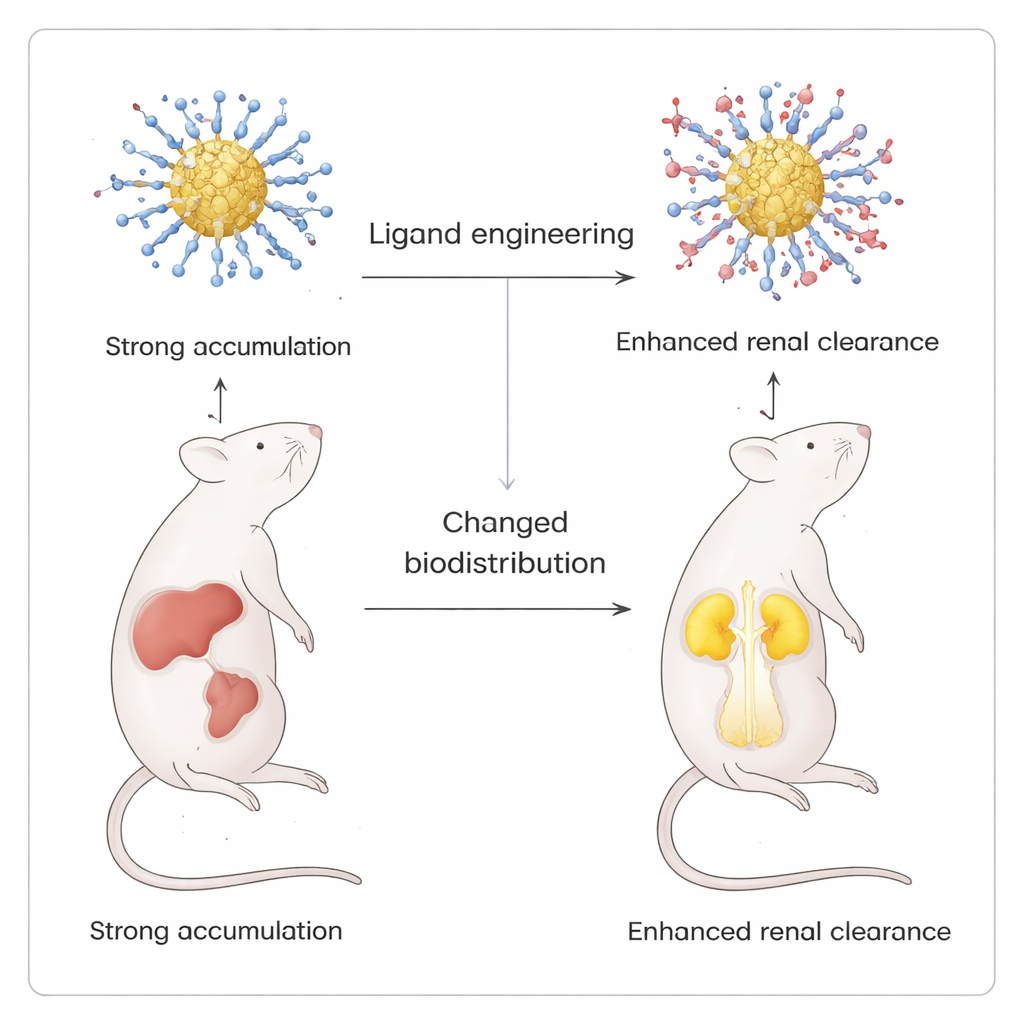
Najbardziej uderzający test tej precyzji pochodził z doświadczeń obrazowania in vivo na myszach. Poprzez stopniowe wprowadzanie dodatnio naładowanego ligandu, p-aminotiofenolu, do w przeciwnym razie ujemnie naładowanej powłoki, zespół stworzył serię klastrów, których całkowity ładunek powierzchniowy przesuwał się od silnie ujemnego do bliskiego zwitterjonowemu (zrównoważone grupy dodatnie i ujemne). Wszystkie wersje świeciły podobnie w testach laboratoryjnych, ale ich biodystrybucja u myszy różniła się dramatycznie. Klastry o wyraźnie ujemnym ładunku gromadziły się głównie w wątrobie i śledzionie. W miarę dodawania większej liczby dodatnich ligandów, w tych narządach pojawiało się mniej sygnału, a więcej w nerkach i pęcherzu, co wskazuje na zwiększone wydalanie nerkowe. Gdy zamiast aminy użyto neutralnego ligandu hydroksylowego, przesunięcie to nie wystąpiło, podkreślając szczególną rolę ładunków dodatnich w przekierowywaniu cząstek.
Co to znaczy dla przyszłych leków
Dla osób niezaznajomionych z tematem kluczowy wniosek jest taki, że naukowcy znaleźli sposób na „ubieranie” świecących nanoklustrów złota w molekularne powłoki, które można dostrajać niemal jedna cząsteczka na raz, bez uszkadzania cząstki bazowej. Używając łagodnego układu dwóch cieczy, mogą kontrolować zarówno chemię, jak i ostateczny los tych cząstek w organizmie. Ten poziom kontroli umożliwia projektowanie środków kontrastowych i potencjalnych nośników leków, które wyświetlają konkretne narządy, a następnie są usuwane przez nerki zamiast zalegać w wątrobie i śledzionie, torując drogę do bezpieczniejszej i bardziej przewidywalnej nanomedycyny.
Cytowanie: Zhang, B., Xiao, F., Song, X. et al. Atomically precise ligand engineering of gold nanoparticles via interphase mass transfer. Nat Commun 17, 1630 (2026). https://doi.org/10.1038/s41467-026-68345-z
Słowa kluczowe: nanoklustery złota, inżynieria ligandów, obrazowanie biologiczne, nanomedycyna, biodystrybucja