Clear Sky Science · pl
Aktywność DOT1L ogranicza szybkość elongacji transkrypcji i sprzyja zatrzymaniom RNAPII, aby ułatwić mutagenezę przez AID
Jak nasze komórki odpornościowe dopracowują ryzykowne edycje DNA
Nasz układ odpornościowy wytwarza silne przeciwciała, celowo wprowadzając mutacje w własnym DNA — ryzykowna strategia, która czasem może sprzyjać nowotworom. To badanie stawia pozornie proste pytanie o duże konsekwencje: co kontroluje, gdzie i jak efektywnie zachodzą te celowe mutacje? Odpowiedź koncentruje się wokół białka o nazwie DOT1L, które reguluje prędkość „czytania” genów w komórkach B i dzięki temu pomaga skierować maszynerię mutacyjną we właściwe miejsca.
Włączanie mutacji, by ulepszyć przeciwciała
Gdy komórki B napotkają infekcję, ulepszają swoje przeciwciała na dwa sposoby. Wprowadzają drobne zmiany w regionie wiążącym przeciwciała, aby poprawić ich powinowactwo do patogenów, oraz wymieniają fragment Fc, by zmienić sposób, w jaki układ odpornościowy reaguje. Oba procesy rozpoczynają się od enzymu AID, który naciina i modyfikuje DNA w aktywnie transkrybowanych genach. Chociaż AID jest niezbędny dla prawidłowej odporności, może też atakować inne geny, tworząc niebezpieczne przerwania prowadzące do nowotworów krwi. Wcześniejsze prace pokazały, że AID preferuje geny intensywnie transkrybowane i regulowane przez potężne przełączniki DNA zwane super-enhancerami, lecz to nie wyjaśniało w pełni, dlaczego tylko wybrana podgrupa genów jest rzeczywiście podatna.
Znacznik chromatyny wskazujący geny wrażliwe na AID
Autorzy skupili się na białkach znajdujących się w pobliżu AID w jądrze komórkowym. Przy użyciu techniki znakowania na zasadzie bliskości w komórkach ludzkich odkryli, że AID gromadzi się w sąsiedztwie DOT1L — enzymu, który umieszcza specyficzny znacznik na białkach histonowych, wokół których owinięty jest DNA. Ten znacznik, chemiczna modyfikacja histonu H3 w pozycji K79, występuje na aktywnych genach. W komórkach B myszy geny często mutowane przez AID — w tym geny przeciwciał oraz poza-cele związane z rakiem — nosiły szczególnie wysokie poziomy tych znaków wytwarzanych przez DOT1L. Gdy badacze wyłączyli DOT1L w liniach komórkowych B lub zablokowali jego aktywność lekiem, zmniejszyło się przełączanie klas przeciwciał, podobnie jak przerwania DNA wywoływane przez AID oraz fuzje sprzyjające nowotworom między genami przeciwciał a genem wzrostu cMyc. Co istotne, wymagane było katalityczne działanie DOT1L, nie tylko jego obecność: mutanty, które nie potrafiły umieszczać tego znaku na histonie, nie przywracały normalnego przełączania klas przeciwciał.
Spowalnianie czytnika genów, by dać czas AID
Początkowo wydaje się to nielogiczne, bo DOT1L kojarzy się z aktywnymi genami, a jednak jego usunięcie nie powodowało po prostu ich wyciszenia. Stosując metodę rejestracji świeżo powstających RNA, zespół odkrył, że komórki B pozbawione DOT1L faktycznie wytwarzały więcej transkryptów naciennych w wielu genach oznaczonych przez DOT1L — mimo że nieco mniej enzymu odczytującego geny, polimerazy RNA II, było związane z tymi genami. Łącząc dane o nowo syntetyzowanych RNA z mapami zajęcia polimerazy, badacze wywnioskowali, że w normalnych warunkach znaki histonowe DOT1L działają jak delikatne spowalniacze. Zwężają polimerazę podczas przemieszczania się wzdłuż genu i wydłużają krótkie zatrzymania blisko początku oraz w obrębie ciała genów oznaczonych przez DOT1L. Bez DOT1L polimeraza porusza się szybciej i krócej się zatrzymuje. Ponieważ AID potrzebuje krótkich okien, kiedy DNA jest odsłonięte i polimeraza się waha, to przyspieszenie paradoksalnie zmniejsza zdolność AID do przyłączenia się i wykonania swojej funkcji, nawet gdy ogólna transkrypcja wzrasta.
Oddzielenie aktywności genów od ryzyka mutacji
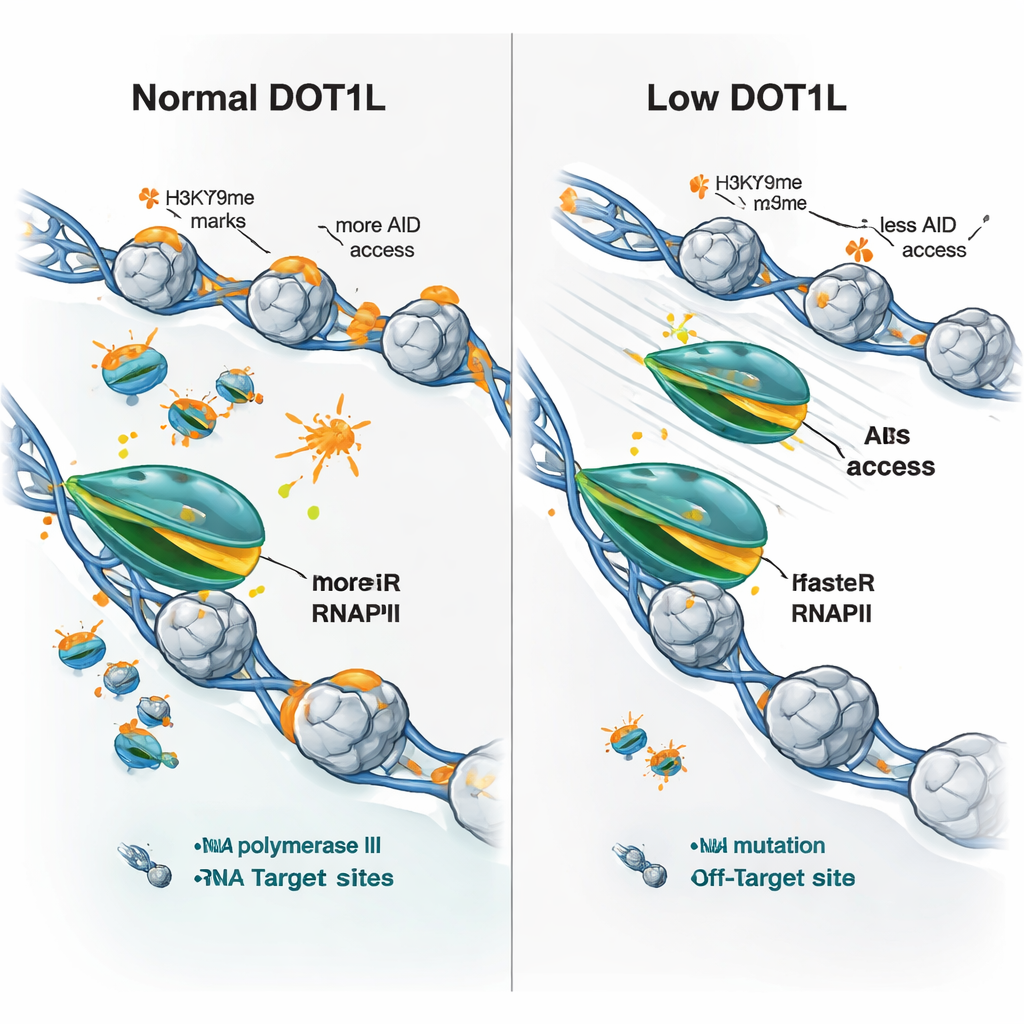
Następnie badacze zapytali, czy te zmiany prędkości mogą wyjaśnić mieszany wzorzec ekspresji genów obserwowany po utracie DOT1L — niektóre geny rosną, inne maleją. Stwierdzili, że praktycznie wszystkie geny oznaczone przez DOT1L miały jedną cechę w komórkach typu knockout: szybszą elongację przez polimerazę RNA II. Efekt zależał jednak od stanu wyjściowego. Wolne, słabo eksprymowane geny miały tendencję do produkcji większej ilości RNA, gdy polimeraza przyspieszała, natomiast wysoko aktywne, długie geny z już szybką polimerazą czasami produkowały mniej — prawdopodobnie dlatego, że zbyt szybkie przejście zakłócało efektywne przetwarzanie lub ukończenie transkryptu. Co kluczowe, zarówno w genach przeciwciał, jak i klasycznych poza-celach AID, utrata DOT1L prowadziła do szybszego poruszania się polimerazy, mniejszej liczby dowodów „zastoju” polimerazy i istotnie zmniejszonego zajęcia przez AID, nawet gdy same geny nie były osłabione.
Dlaczego to ma znaczenie dla odporności i nowotworów
Razem te wyniki przedstawiają DOT1L jako subtelnego kontrolera ruchu dla maszynerii czytającej geny w komórkach B. Poprzez instalowanie specyficznych znaków na histonach DOT1L nieznacznie spowalnia polimerazę RNA II i wydłuża jej zatrzymania, tworząc środowisko transkrypcyjne, w którym AID może produktywnie działać na genach przeciwciał — i niestety na ograniczonej grupie innych wrażliwych genów — wprowadzając mutacje. Gdy DOT1L jest brakujący lub zahamowany, polimeraza przemyka szybciej, pozostawiając AID mniej okazji do działania, co osłabia dywersyfikację przeciwciał i jednocześnie obniża ryzyko niektórych szkodliwych rearanżacji. To mechanistyczne wyjaśnienie tłumaczy, dlaczego utrata DOT1L może zarówno zwiększać, jak i zmniejszać ekspresję genów, i łączy precyzyjną kontrolę prędkości transkrypcji z miejscami, w których nasz układ odpornościowy odważa się przepisać własne DNA.
Cytowanie: Subramani, P.G., Seija, N., Ridani, J. et al. DOT1L activity limits transcription elongation velocity and favors RNAPII pausing to facilitate mutagenesis by AID. Nat Commun 17, 1623 (2026). https://doi.org/10.1038/s41467-026-68332-4
Słowa kluczowe: dywersyfikacja przeciwciał, enzym AID, DOT1L, transkrypcja genów, limfocyty B