Clear Sky Science · pl
Obliczeniowe projektowanie uniwersalnych cyklopropanaz o stereodivergentej selektywności
Dlaczego małe struktury z trzema pierścieniami mają znaczenie dla leków
Cyklopropany — trzyatomowe pierścienie węgla — to niewielkie, naprężone elementy budulcowe, które mogą dramatycznie zmieniać zachowanie leku w organizmie. Dokładne rozmieszczenie atomów w przestrzeni (stereochemia) może przesądzić, czy cząsteczka stanie się użytecznym lekiem, czy też nieaktywnym bądź nawet szkodliwym „sobowtórem”. Artykuł opisuje strategię obliczeniową do projektowania enzymów, które potrafią wiarygodnie wytwarzać wszystkie cztery możliwe formy 3D tych pierścieni z tych samych substratów wyjściowych, otwierając drogę do szybszego i „czystszego” badania kandydatów na leki.
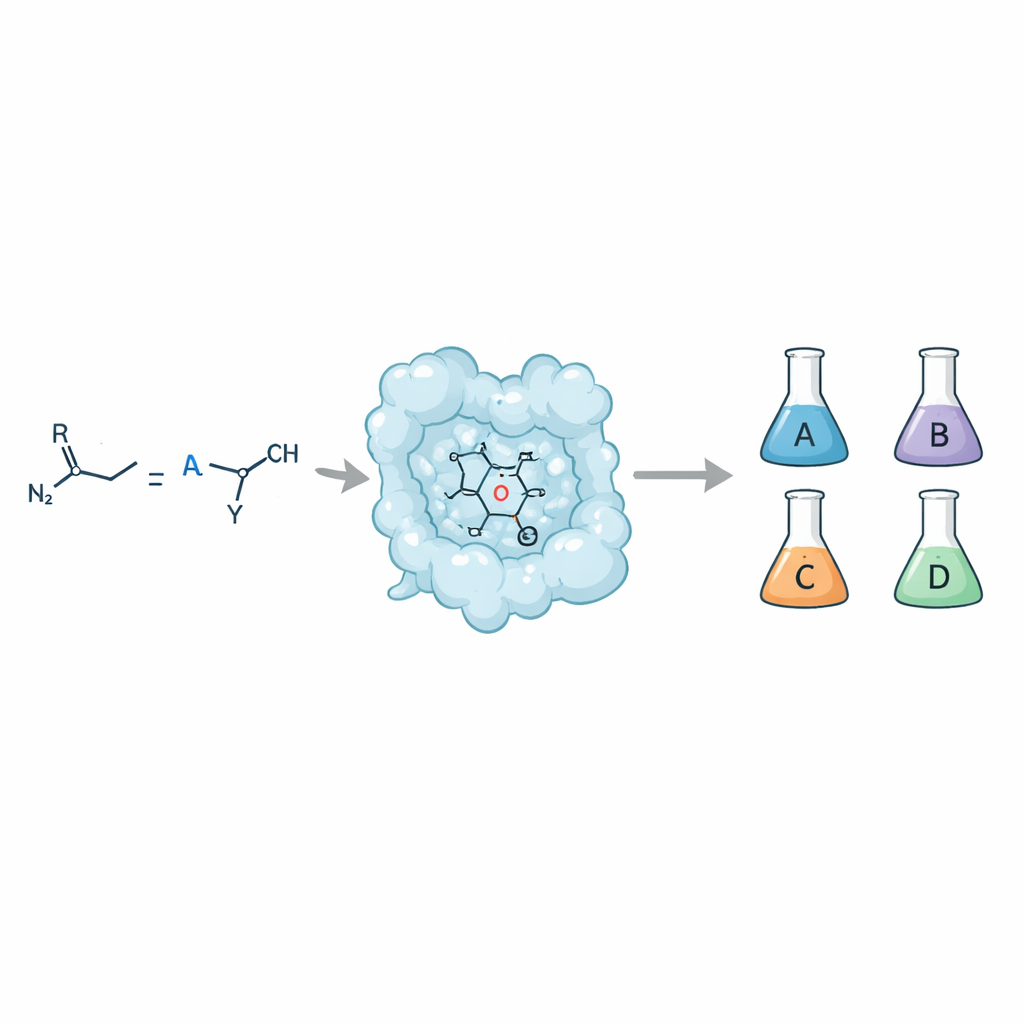
Z jednego przepisu do czterech różnych rezultatów
Gdy prosty podwójny związek (olefin) reaguje z dawcą karbenów, takim jak związek diazowy, powstaje pierścień cyklopropanowy. Ten pierścień może jednak przyjąć cztery odrębne formy stereochemiczne — te same atomy, inaczej ułożone w przestrzeni. Chemicy potrzebują dostępu do każdej z tych form, ponieważ różnie oddziałują z celami biologicznymi i wpływają na istotne właściwości leku, takie jak wchłanianie, metabolizm czy bezpieczeństwo. Tradycyjne katalizatory małocząsteczkowe czasem zapewniają taką kontrolę, ale osiągnięcie tego za pomocą enzymów — naturalnych katalizatorów — było trudne, szczególnie gdy celem jest zarówno wysoka selektywność, jak i tolerancja wobec wielu różnych substratów.
Projektowanie enzymów na ekranie komputera
Autorzy opracowali mechanistyczny, wielostanowy przepływ obliczeniowy, aby rozwiązać ten problem. Najpierw wykorzystali obliczenia chemii kwantowej do modelowania ulotnych stanów przejściowych — struktur o wysokiej energii na ścieżce reakcji — prowadzących do powstania każdej z czterech stereizomerów cyklopropanu. Te modele umieszczono następnie w centrach aktywnych różnych białek zawierających hem, a oprogramowanie do projektowania białek Rosetta posłużyło do oceny, jak dobrze każde białko stabilizuje lub destabilizuje dany stan przejściowy. Kluczowe było to, że wynik projektowania nagradzał mutacje, które jednocześnie sprzyjały pożądanemu stanowi przejściowemu (projekt pozytywny) i utrudniały konkurencyjne stany (projekt negatywny), skutecznie „ucząc” enzym preferowania jednego produktu 3D kosztem innych.
Budowa kompletnego zestawu enzymów
Stosując to podejście, zespół stworzył rodzinę „generalistycznych” cyklopropanaz. Rozpoczynając od mioglobiny, przeprojektowali jej centrum aktywne, uzyskując warianty, które wytwarzają trans-(1R,2R) cyklopropan z bardzo wysoką selektywnością i dobrą aktywnością dla ponad 20 różnych olefin, w tym wymagających substratów nieaktywowanych i ubogich elektronowo. Wcześniej zaprojektowana mioglobina dostarczała już komplementarny produkt trans-(1S,2S). Aby uzyskać dwa produkty cis, autorzy zwrócili się do innych białek hemowych. Przeprojektowali bakteryjne białko P450cam, uzyskując warianty selektywnie dające cis-(1S,2R), a także zaadaptowali ludzką indoloaminę 2,3-dioksygenazę-1 (IDO1) — wcześniej nieużywaną w chemii karbenów — aby faworyzowała produkt cis-(1R,2S). W sumie te cztery biokatalizatory potrafią dostarczyć każdy stereizomer tego samego zestawu produktów cyklopropanowych, często z kontrolą obu aspektów stereochemicznych (diastereo- i enancjoselektywność) sięgającą do 99%.
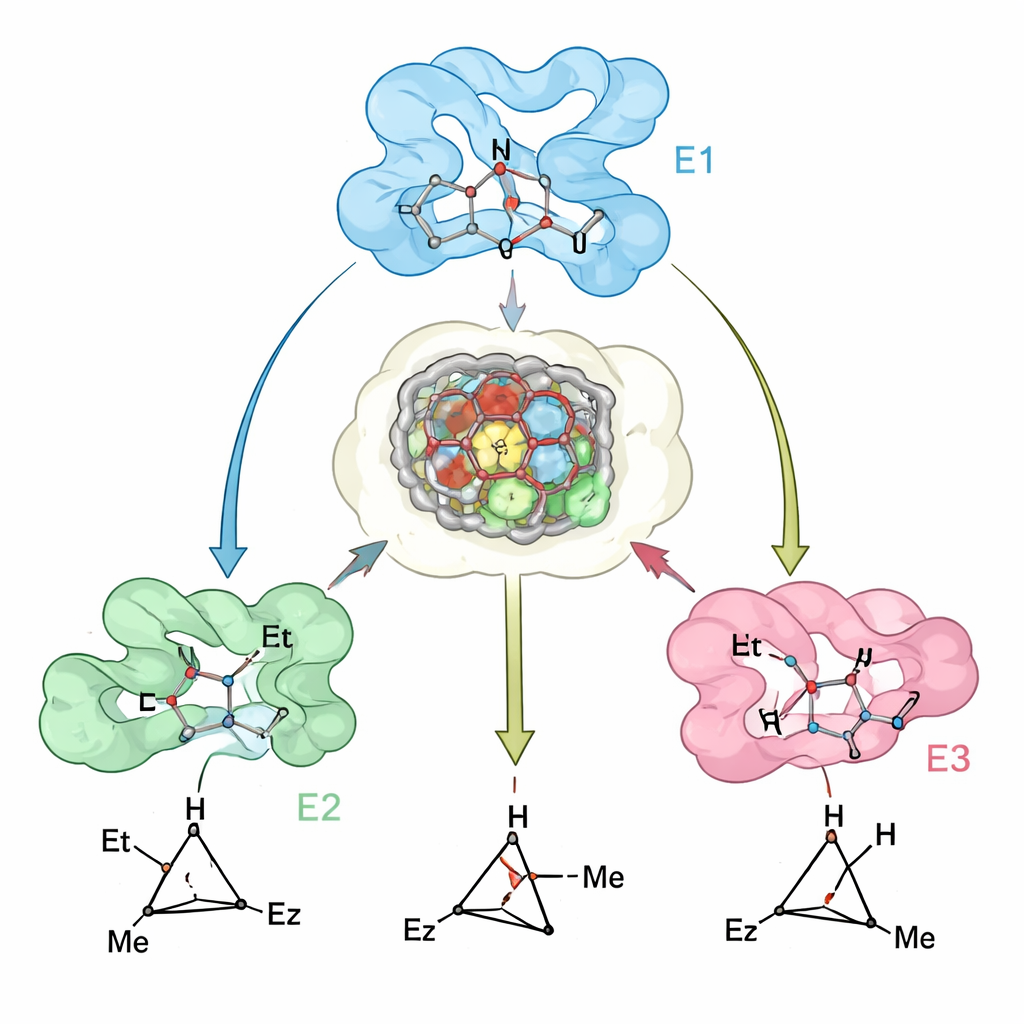
Jak projektowanie ma się do rzeczywistości
Aby sprawdzić, jak dobrze ich modele obliczeniowe odzwierciedlają rzeczywiste enzymy, badacze rozwiązywali struktury krystaliczne kluczowego wariantu mioglobiny i porównywali je z przewidywanymi strukturami. Zgodność była bliska, a dane eksperymentalne uwypukliły subtelną, ale istotną cechę: centrum aktywne białka jest wstępnie zorganizowane tak, aby przyjąć preferowany stan przejściowy, podczas gdy niewielkie przesunięcia pobliskich pętli i helis sprawiają, że wiązanie „błędnego” stanu przejściowego jest energetycznie niekorzystne. Tam, gdzie przewidywania były mniej dokładne — na przykład dla kilku masywnych substratów — rozbieżności można było przypisać ruchom szkieletu, które nie zostały w pełni uchwycone w modelowaniu, co wskazuje klarowne kierunki poprawy metod projektowania.
Co to oznacza dla przyszłych leków i katalizatorów
Łącząc modelowanie stanów przejściowych oparte na fizyce z inteligentnym przeprojektowaniem białek, praca ta pokazuje, że wyniki stereochemiczne reakcji katalizowanych przez enzymy można zaprogramować z wyprzedzeniem, zamiast odkrywać je jedynie metodą prób i błędów ewolucji. Powstały zestaw cyklopropanaz daje chemikom praktyczny sposób na otrzymanie kompletnych zestawów stereizomerów cyklopropanu z szerokiego zakresu olefin wyjściowych, znacząco upraszczając badania zależności struktura–aktywność w odkrywaniu leków i syntezie związków naturalnych. Ta sama strategia powinna być przystosowalna do innych typów enzymów i klas reakcji, przyspieszając tworzenie biokatalizatorów zapewniających precyzyjną kontrolę 3D nad złożonymi cząsteczkami.
Cytowanie: Shen, Z., Siriboe, M.G., Ren, X. et al. Computational design of generalist cyclopropanases with stereodivergent selectivity. Nat Commun 17, 1620 (2026). https://doi.org/10.1038/s41467-026-68327-1
Słowa kluczowe: biokataliza, cyklopropanacja, projektowanie enzymów, stereochemia, białka hemowe